よむ、つかう、まなぶ。
【資料1-1】成分情報等 (14 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_70651.html |
| 出典情報 | 医療用から要指導・一般用への転用に関する評価検討会議(第35回 2/20)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
11.2 その他の副作用
1~5%
未満
過敏症
口腔・呼吸器 嗄声
0.1~1%未満
咽喉頭の刺激感、口腔
カ ン ジ ダ 症 、咳 嗽 、感
染、
肺炎
消化器
循環器
動 悸 、不 整 脈( 心 房 細
動、
上室性頻脈、
期外収
縮等)
、
頻脈、
血圧上昇
その他
味覚異常、気管
支痙攣注)
悪心
頭痛、
振戦、
神経過敏
内分泌
頻度不明
発疹、
蕁麻疹、
接触性皮
膚炎、血管浮腫等の過
敏症状
精神神経系
筋・骨格系
0.1%未満
情緒不安、 激越、
抑うつ、
行
めまい、睡 動障害
眠障害
狭心症
筋痙攣
図1 単回吸入投与後の血漿中ブデソニド濃度
(14例の平均値±標準偏差)
高血糖
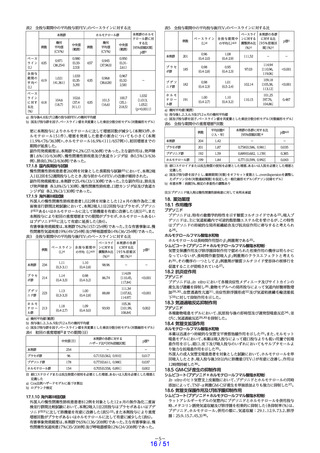
表1 単回吸入投与後のブデソニドの薬物動態パラメータ
(14例の平均値±標準
偏差)
皮膚挫傷
注)
短時間作動型吸入β2刺激剤を投与するなどの適切な処置を行うこと。
13. 過量投与
ブデソニド
(µg)
Cmax
(nmol/L)
Tmax
(min)
AUC0-∞
(nmol・h/L)
t1/2
(h)
640
10.3±2.37
5.36±1.34
14.0±1.93
3.09±0.49
13.1 症状
ブデソニドの過量投与により副腎皮質系機能が低下することがあ
る。
ホルモテロールフマル酸塩水和物の過量投与により、
動悸、
頻脈、
不整脈、
振戦、
頭痛及び筋痙攣等、
β刺激剤の薬理学的作用による全
身作用が発現する可能性がある。
また、
重篤な症状として、
血圧低下、
代謝性アシドーシス、
低カリウム血症、
高血糖、
心室性不整脈あるい
は心停止等が発現する可能性がある。
[8.7参照]
13.2 処置
副腎皮質系機能の低下がみられた場合には患者の症状を観察しなが
ら徐々に減量するなど適切な処置を行うこと。
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 吸入前
本剤の投与にあたって、
吸入器の操作法、
吸入法等を十分に説明する
こと。
(1) 患者に本剤を交付する際には、
包装中に添付している患者用説明
文書を渡し、
使用方法を指導すること。
(2) 初めて本剤を投与する患者には、
本剤が十分に気道に到達するよ
う吸入方法をよく説明したうえ、
吸入の訓練をさせること。
14.1.2 吸入時
本剤は口腔内への吸入投与のみに使用すること。
14.1.3 吸入後
口腔カンジダ症又は嗄声の予防のため、
本剤吸入後に、
うがいを実施
するよう患者を指導すること。
ただし、
うがいが困難な患者には、
う
がいではなく口腔内をすすぐよう指導すること。
14.1.4 保管時
(1) 使用後は必ずキャップ
(カバー)
を閉めて保管すること。
(2) マウスピースの外側を週に1~2回乾燥した布で清拭すること
(水
洗いはしないこと)
。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 外国における疫学調査で、
吸入ステロイド剤投与によりまれに
白内障が発現するとの報告がある。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人男性
(14例)
に本剤4吸入
(ブデソニド:640µg、
ホルモテロールフマル
酸塩水和物:18µg)
を単回吸入投与したとき、
ブデソニド及びホルモテロール
はいずれも速やかに最高血漿中濃度
(Cmax)
に達した。
消失半減期
(t1/2)
はブデ
ソニドで約3時間、
ホルモテロールで約6時間であった1)。
図2 単回吸入投与後の血漿中ホルモテロール濃度
(14例の平均値±標準偏差)
表2 単回吸入投与後のホルモテロールの薬物動態パラメータ
(14例の平均値±
標準偏差)
ホルモテロールフマル
酸塩水和物
(µg)
Cmax
(pmol/L)
Tmax
(min)
AUC0-∞
(pmol・h/L)
t1/2
(h)
18
175±56.4
5.00±0.00
329±81.0
6.14±2.66
16.1.2 反復投与
健康成人男性
(11~12例)
に本剤2吸入
(ブデソニド:320µg、
ホルモテロール
フマル酸塩水和物:9µg)
または4吸入
(ブデソニド:640µg、
ホルモテロール
フマル酸塩水和物:18µg)
を1日2回7日間反復投与したとき、
ブデソニド及び
ホルモテロールはそれぞれ投与後10分以内、
投与後5分にCmaxに達した。
t1/2は
ブデソニドで約3.5時間、
ホルモテロールで約5~7時間であった。
ブデソニド及
びホルモテロールのCmax及び血漿中濃度-時間曲線下面積
(AUC)
は投与量に
ほぼ比例して増加した。
ブデソニド及びホルモテロールともに反復投与による
薬物動態の変化は認められなかった1)。
16.3 分布
ヒト血漿蛋白質との結合率はブデソニドで約90% 2) 、ホルモテロールで約
50%3)であった
(in vitro 試験)
。
分布容積はブデソニドで約3L/kg4)、
ホルモテ
ロールで約5L/kg5)であった。
16.4 代謝
ブデソニド
ブデソニドの血漿及び尿中の主代謝物は、
16α-ヒドロキシプレドニゾロン及
び6β-ヒドロキシブデソニドであり、
尿中に未変化体は検出されなかった6)。
ブ
デソニドの代謝にはCYP3A4が関与する7)
(in vitro 試験)
。
ホルモテロール
ヒト血漿及び尿中の主代謝物は、
ホルモテロールのグルクロン酸抱合体であっ
た。
尿中にはO -脱メチル化体のグルクロン酸抱合体も認められた8)。
ホルモテ
ロールのO -脱メチル化反応には主としてCYP2D6及びCYP2Cが関与する9)
(in vitro 試験)
。
-3-
14 / 51
1~5%
未満
過敏症
口腔・呼吸器 嗄声
0.1~1%未満
咽喉頭の刺激感、口腔
カ ン ジ ダ 症 、咳 嗽 、感
染、
肺炎
消化器
循環器
動 悸 、不 整 脈( 心 房 細
動、
上室性頻脈、
期外収
縮等)
、
頻脈、
血圧上昇
その他
味覚異常、気管
支痙攣注)
悪心
頭痛、
振戦、
神経過敏
内分泌
頻度不明
発疹、
蕁麻疹、
接触性皮
膚炎、血管浮腫等の過
敏症状
精神神経系
筋・骨格系
0.1%未満
情緒不安、 激越、
抑うつ、
行
めまい、睡 動障害
眠障害
狭心症
筋痙攣
図1 単回吸入投与後の血漿中ブデソニド濃度
(14例の平均値±標準偏差)
高血糖
表1 単回吸入投与後のブデソニドの薬物動態パラメータ
(14例の平均値±標準
偏差)
皮膚挫傷
注)
短時間作動型吸入β2刺激剤を投与するなどの適切な処置を行うこと。
13. 過量投与
ブデソニド
(µg)
Cmax
(nmol/L)
Tmax
(min)
AUC0-∞
(nmol・h/L)
t1/2
(h)
640
10.3±2.37
5.36±1.34
14.0±1.93
3.09±0.49
13.1 症状
ブデソニドの過量投与により副腎皮質系機能が低下することがあ
る。
ホルモテロールフマル酸塩水和物の過量投与により、
動悸、
頻脈、
不整脈、
振戦、
頭痛及び筋痙攣等、
β刺激剤の薬理学的作用による全
身作用が発現する可能性がある。
また、
重篤な症状として、
血圧低下、
代謝性アシドーシス、
低カリウム血症、
高血糖、
心室性不整脈あるい
は心停止等が発現する可能性がある。
[8.7参照]
13.2 処置
副腎皮質系機能の低下がみられた場合には患者の症状を観察しなが
ら徐々に減量するなど適切な処置を行うこと。
14. 適用上の注意
14.1 薬剤交付時の注意
14.1.1 吸入前
本剤の投与にあたって、
吸入器の操作法、
吸入法等を十分に説明する
こと。
(1) 患者に本剤を交付する際には、
包装中に添付している患者用説明
文書を渡し、
使用方法を指導すること。
(2) 初めて本剤を投与する患者には、
本剤が十分に気道に到達するよ
う吸入方法をよく説明したうえ、
吸入の訓練をさせること。
14.1.2 吸入時
本剤は口腔内への吸入投与のみに使用すること。
14.1.3 吸入後
口腔カンジダ症又は嗄声の予防のため、
本剤吸入後に、
うがいを実施
するよう患者を指導すること。
ただし、
うがいが困難な患者には、
う
がいではなく口腔内をすすぐよう指導すること。
14.1.4 保管時
(1) 使用後は必ずキャップ
(カバー)
を閉めて保管すること。
(2) マウスピースの外側を週に1~2回乾燥した布で清拭すること
(水
洗いはしないこと)
。
15. その他の注意
15.1 臨床使用に基づく情報
15.1.1 外国における疫学調査で、
吸入ステロイド剤投与によりまれに
白内障が発現するとの報告がある。
16. 薬物動態
16.1 血中濃度
16.1.1 単回投与
健康成人男性
(14例)
に本剤4吸入
(ブデソニド:640µg、
ホルモテロールフマル
酸塩水和物:18µg)
を単回吸入投与したとき、
ブデソニド及びホルモテロール
はいずれも速やかに最高血漿中濃度
(Cmax)
に達した。
消失半減期
(t1/2)
はブデ
ソニドで約3時間、
ホルモテロールで約6時間であった1)。
図2 単回吸入投与後の血漿中ホルモテロール濃度
(14例の平均値±標準偏差)
表2 単回吸入投与後のホルモテロールの薬物動態パラメータ
(14例の平均値±
標準偏差)
ホルモテロールフマル
酸塩水和物
(µg)
Cmax
(pmol/L)
Tmax
(min)
AUC0-∞
(pmol・h/L)
t1/2
(h)
18
175±56.4
5.00±0.00
329±81.0
6.14±2.66
16.1.2 反復投与
健康成人男性
(11~12例)
に本剤2吸入
(ブデソニド:320µg、
ホルモテロール
フマル酸塩水和物:9µg)
または4吸入
(ブデソニド:640µg、
ホルモテロール
フマル酸塩水和物:18µg)
を1日2回7日間反復投与したとき、
ブデソニド及び
ホルモテロールはそれぞれ投与後10分以内、
投与後5分にCmaxに達した。
t1/2は
ブデソニドで約3.5時間、
ホルモテロールで約5~7時間であった。
ブデソニド及
びホルモテロールのCmax及び血漿中濃度-時間曲線下面積
(AUC)
は投与量に
ほぼ比例して増加した。
ブデソニド及びホルモテロールともに反復投与による
薬物動態の変化は認められなかった1)。
16.3 分布
ヒト血漿蛋白質との結合率はブデソニドで約90% 2) 、ホルモテロールで約
50%3)であった
(in vitro 試験)
。
分布容積はブデソニドで約3L/kg4)、
ホルモテ
ロールで約5L/kg5)であった。
16.4 代謝
ブデソニド
ブデソニドの血漿及び尿中の主代謝物は、
16α-ヒドロキシプレドニゾロン及
び6β-ヒドロキシブデソニドであり、
尿中に未変化体は検出されなかった6)。
ブ
デソニドの代謝にはCYP3A4が関与する7)
(in vitro 試験)
。
ホルモテロール
ヒト血漿及び尿中の主代謝物は、
ホルモテロールのグルクロン酸抱合体であっ
た。
尿中にはO -脱メチル化体のグルクロン酸抱合体も認められた8)。
ホルモテ
ロールのO -脱メチル化反応には主としてCYP2D6及びCYP2Cが関与する9)
(in vitro 試験)
。
-3-
14 / 51