よむ、つかう、まなぶ。
参考資料1_治験・臨床試験の推進に関する今後の方向性について 2025年版とりまとめ 参考資料集 (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_58747.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第43回 6/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
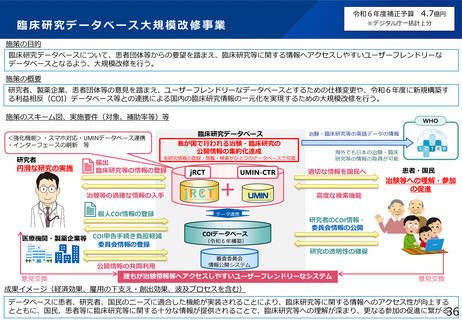
令和6年度補正予算
国際共同治験ワンストップ相談窓口事業
2.7億円
② 対策の柱との関係
① 施策の目的
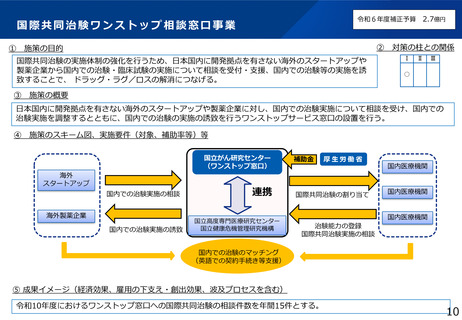
国際共同治験の実施体制の強化を行うため、日本国内に開発拠点を有さない海外のスタートアップや
製薬企業から国内での治験・臨床試験の実施について相談を受付・支援、国内での治験等の実施を誘
致することで、 ドラッグ・ラグ/ロスの解消につなげる。
Ⅰ
Ⅱ
Ⅲ
○
③ 施策の概要
日本国内に開発拠点を有さない海外のスタートアップや製薬企業に対し、国内での治験実施について相談を受け、国内での
治験実施を調整するとともに、国内での治験の実施の誘致を行うワンストップサービス窓口の設置を行う。
④ 施策のスキーム図、実施要件(対象、補助率等)等
国立がん研究センター
(ワンストップ窓口)
海外
スタートアップ
国内での治験実施の相談
海外製薬企業
国内での治験実施の誘致
連携
国立高度専門医療研究センター
国立健康危機管理研究機構
補助金
厚生労働省
国際共同治験の割り当て
国内医療機関
国内医療機関
国内医療機関
治験能力の登録
国際共同治験実施の相談
国内での治験のマッチング
(英語での契約手続き等支援)
⑤ 成果イメージ(経済効果、雇用の下支え・創出効果、波及プロセスを含む)
令和10年度におけるワンストップ窓口への国際共同治験の相談件数を年間15件とする。
10
国際共同治験ワンストップ相談窓口事業
2.7億円
② 対策の柱との関係
① 施策の目的
国際共同治験の実施体制の強化を行うため、日本国内に開発拠点を有さない海外のスタートアップや
製薬企業から国内での治験・臨床試験の実施について相談を受付・支援、国内での治験等の実施を誘
致することで、 ドラッグ・ラグ/ロスの解消につなげる。
Ⅰ
Ⅱ
Ⅲ
○
③ 施策の概要
日本国内に開発拠点を有さない海外のスタートアップや製薬企業に対し、国内での治験実施について相談を受け、国内での
治験実施を調整するとともに、国内での治験の実施の誘致を行うワンストップサービス窓口の設置を行う。
④ 施策のスキーム図、実施要件(対象、補助率等)等
国立がん研究センター
(ワンストップ窓口)
海外
スタートアップ
国内での治験実施の相談
海外製薬企業
国内での治験実施の誘致
連携
国立高度専門医療研究センター
国立健康危機管理研究機構
補助金
厚生労働省
国際共同治験の割り当て
国内医療機関
国内医療機関
国内医療機関
治験能力の登録
国際共同治験実施の相談
国内での治験のマッチング
(英語での契約手続き等支援)
⑤ 成果イメージ(経済効果、雇用の下支え・創出効果、波及プロセスを含む)
令和10年度におけるワンストップ窓口への国際共同治験の相談件数を年間15件とする。
10