よむ、つかう、まなぶ。
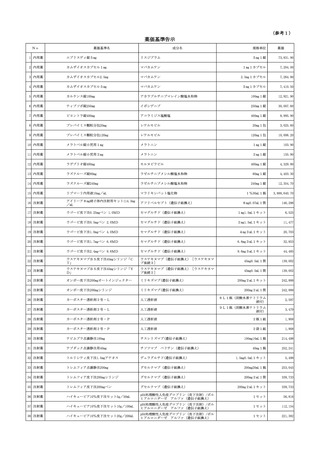
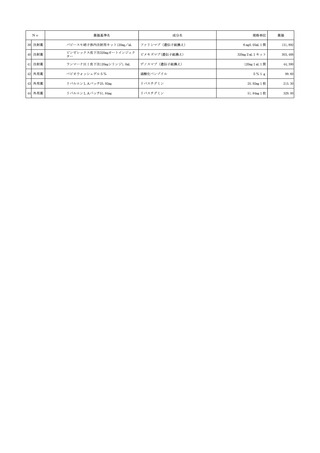
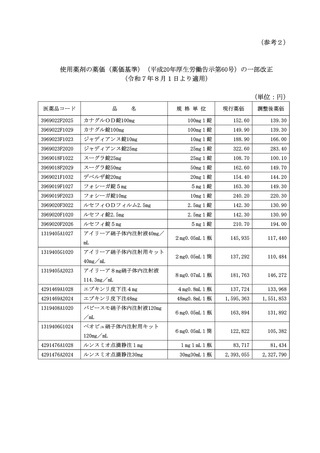
使用薬剤の薬価(薬価基準)の一部改正等について 保医発0520第1号令和7年5月20日 (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/content/12404000/001490789.pdf |
| 出典情報 | 使用薬剤の薬価(薬価基準)の一部改正等について(5/20付 通知)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
検査施設における検査により、EGFR 遺伝子変異が確認された患者に投与すること。」
とされているので、EGFR 遺伝子変異陽性を確認した検査の実施年月日を診療報酬明
細書に記載すること。
なお、当該検査を実施した月のみ実施年月日を記載すること。ただし、本剤の初
回投与に当たっては、必ず当該検査の実施年月日を記載すること。
(6) プレバイミス顆粒分包 20mg、同顆粒分包 120mg
本製剤は、既に薬価収載後1年以上経過している「プレバイミス錠 240mg」と有効
成分が同一であり、今般、既収載品において小児における用法・用量が追加された
ことに伴い、当該用法・用量に必要となる製剤として承認された剤形追加医薬品で
あることから、掲示事項等告示第 10 第2号(一)に規定する新医薬品に係る投薬期
間制限(14 日間を限度とする。)は適用されないものであること。
(7) リバルエンLAパッチ 25.92mg 及び同LAパッチ 51.84mg
① 本製剤の用法及び用量に「原則として開始時は4日間貼付し、1枚を3~4日
ごとに1回(週2回)貼り替える。」、並びに用法及び用量に関連する使用上の
注意に「本剤の1回あたりの貼付枚数は原則1枚とし、貼付期間は4日間を超え
ないこと。」と記載されていることから、3~4日につき1枚(週2枚)を使用
した場合に限り算定できるものであること。
② 本製剤の効能・効果は「軽度及び中等度のアルツハイマー型認知症における認
知症症状の進行抑制」であることから、軽度及び中等度のアルツハイマー型認知
症であることが確認された患者に対して使用した場合に限り算定できるものであ
ること。
5
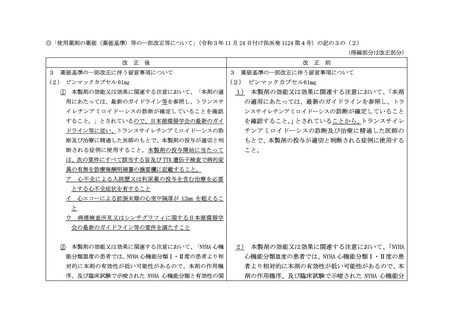
関係通知の一部改正について
(1) 「医薬品医療機器等法上の効能・効果等の変更に伴う留意事項の一部改正等につ
いて」(平成 31 年3月 26 日付け保医発 0326 第1号)の記の1を次のように改め
る。
ビンダケルカプセル 20mg
(1) 本製剤の効能又は効果に関連する注意において、
「本剤の適用にあたっては、
最新のガイドライン等を参照し、トランスサイレチンアミロイドーシスの診断
が確定していることを確認すること。」とされているので、日本循環器学会の
最新のガイドライン等に従い、トランスサイレチンアミロイドーシスの診断及
び治療に精通した医師のもとで、本製剤の投与が適切と判断される症例に使用
すること。
(2) トランスサイレチン型心アミロイドーシス(野生型及び変異型)
① 本製剤の投与開始に当たっては、次の要件にすべて該当する旨及び TTR 遺
伝子検査で病的変異の有無を診療報酬明細書の摘要欄に記載すること。
ア 心不全による入院歴又は利尿薬の投与を含む治療を必要とする心不全症
状を有すること
イ 心エコーによる拡張末期の心室中隔厚が 12mm を超えること
とされているので、EGFR 遺伝子変異陽性を確認した検査の実施年月日を診療報酬明
細書に記載すること。
なお、当該検査を実施した月のみ実施年月日を記載すること。ただし、本剤の初
回投与に当たっては、必ず当該検査の実施年月日を記載すること。
(6) プレバイミス顆粒分包 20mg、同顆粒分包 120mg
本製剤は、既に薬価収載後1年以上経過している「プレバイミス錠 240mg」と有効
成分が同一であり、今般、既収載品において小児における用法・用量が追加された
ことに伴い、当該用法・用量に必要となる製剤として承認された剤形追加医薬品で
あることから、掲示事項等告示第 10 第2号(一)に規定する新医薬品に係る投薬期
間制限(14 日間を限度とする。)は適用されないものであること。
(7) リバルエンLAパッチ 25.92mg 及び同LAパッチ 51.84mg
① 本製剤の用法及び用量に「原則として開始時は4日間貼付し、1枚を3~4日
ごとに1回(週2回)貼り替える。」、並びに用法及び用量に関連する使用上の
注意に「本剤の1回あたりの貼付枚数は原則1枚とし、貼付期間は4日間を超え
ないこと。」と記載されていることから、3~4日につき1枚(週2枚)を使用
した場合に限り算定できるものであること。
② 本製剤の効能・効果は「軽度及び中等度のアルツハイマー型認知症における認
知症症状の進行抑制」であることから、軽度及び中等度のアルツハイマー型認知
症であることが確認された患者に対して使用した場合に限り算定できるものであ
ること。
5
関係通知の一部改正について
(1) 「医薬品医療機器等法上の効能・効果等の変更に伴う留意事項の一部改正等につ
いて」(平成 31 年3月 26 日付け保医発 0326 第1号)の記の1を次のように改め
る。
ビンダケルカプセル 20mg
(1) 本製剤の効能又は効果に関連する注意において、
「本剤の適用にあたっては、
最新のガイドライン等を参照し、トランスサイレチンアミロイドーシスの診断
が確定していることを確認すること。」とされているので、日本循環器学会の
最新のガイドライン等に従い、トランスサイレチンアミロイドーシスの診断及
び治療に精通した医師のもとで、本製剤の投与が適切と判断される症例に使用
すること。
(2) トランスサイレチン型心アミロイドーシス(野生型及び変異型)
① 本製剤の投与開始に当たっては、次の要件にすべて該当する旨及び TTR 遺
伝子検査で病的変異の有無を診療報酬明細書の摘要欄に記載すること。
ア 心不全による入院歴又は利尿薬の投与を含む治療を必要とする心不全症
状を有すること
イ 心エコーによる拡張末期の心室中隔厚が 12mm を超えること