よむ、つかう、まなぶ。
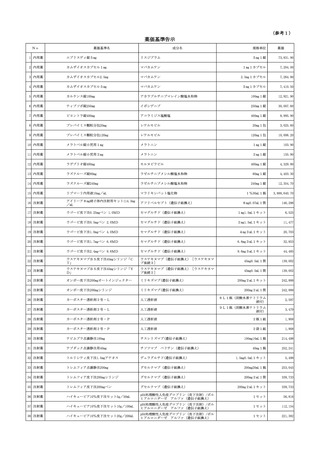
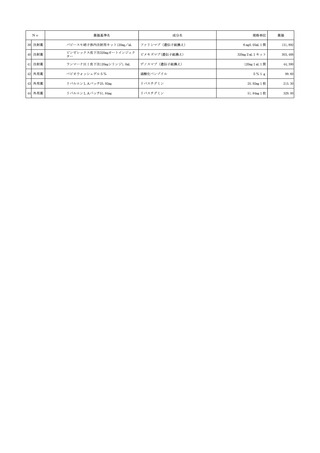
使用薬剤の薬価(薬価基準)の一部改正等について 保医発0520第1号令和7年5月20日 (2 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/content/12404000/001490789.pdf |
| 出典情報 | 使用薬剤の薬価(薬価基準)の一部改正等について(5/20付 通知)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
(3) 「薬価算定の基準について」(令和6年2月 14 日付け保医発 0214 第1号)第3
章第 11 節1の規定に該当し、費用対効果評価が実施された品目(外用薬4品目)に
ついて、その評価結果に基づき、価格調整を行ったものであること。
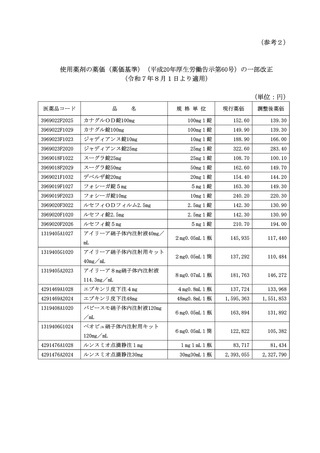
(4)
効能変更等が承認された既収載品であって、「薬価算定の基準について」(令和6
年2月 14 日付け保医発 0214 第1号)第3章第4節4に規定する要件に該当する既
収載品(内用薬 12 品目及び注射薬5品目)について、市場拡大再算定を適用し、薬
価の改定を行ったものであること。
(5)
(3)及び(4)による価格調整後又は改定後の薬価は、令和7年8月1日から
適用されるものであり、それまでは従来の薬価が適用されること。
2
掲示事項等告示の一部改正について
新医薬品(医薬品医療機器等法第 14 条の4第1項第1号に規定する新医薬品をいう。)
については、掲示事項等告示第 10 第2号(1)に規定する新医薬品に係る投薬期間制限
(14 日分を限度とする。)が適用されるが、新たに当該制限の例外とした新医薬品は、
次のとおりであること。
・リブマーリ内用液 10mg/mL
3
薬価基準の一部改正に伴う留意事項について
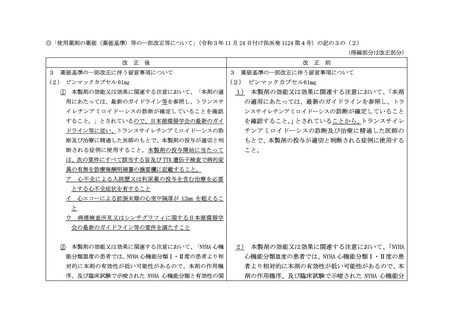
(1) カムザイオスカプセル1mg、同カプセル 2.5mg 及び同カプセル5mg
① 本製剤の効能又は効果に関連する注意において、「症候性の閉塞性肥大型心筋
症患者に投与すること。」及び「「17.臨床成績」の項の内容を熟知し、臨床試験
に組み入れられた患者の背景(前治療、併用薬、左室駆出率等)を十分理解した
上で、最新のガイドライン等を参照し、適応患者を選択すること。」とされてい
るので、使用に当たっては十分留意すること。
② 本製剤の用法及び用量に関連する注意において、「投与開始前に心エコー検査
により左室駆出率(LVEF)を評価し、LVEF が 55%未満の患者には投与を開始しな
いこと。」とされているので、投与開始に当たっては、左室駆出率の計測年月日
及び左室駆出率の値を診療報酬明細書の摘要欄に記載すること。なお、他の医療
機関で左室駆出率を測定した場合には、当該測定結果及び医療機関名を記載する
ことで差し支えない。
(2) ビヨントラ錠 400mg
① 本製剤の効能又は効果に関連する注意において、「本剤の適用にあたっては、
最新のガイドライン等を参照し、トランスサイレチンアミロイドーシスの診断が
確定していることを確認すること。」とされているので、日本循環器学会の最新
のガイドライン等に従い、トランスサイレチンアミロイドーシスの診断及び治療
に精通した医師のもとで、本製剤の投与が適切と判断される症例に使用すること。
章第 11 節1の規定に該当し、費用対効果評価が実施された品目(外用薬4品目)に
ついて、その評価結果に基づき、価格調整を行ったものであること。
(4)
効能変更等が承認された既収載品であって、「薬価算定の基準について」(令和6
年2月 14 日付け保医発 0214 第1号)第3章第4節4に規定する要件に該当する既
収載品(内用薬 12 品目及び注射薬5品目)について、市場拡大再算定を適用し、薬
価の改定を行ったものであること。
(5)
(3)及び(4)による価格調整後又は改定後の薬価は、令和7年8月1日から
適用されるものであり、それまでは従来の薬価が適用されること。
2
掲示事項等告示の一部改正について
新医薬品(医薬品医療機器等法第 14 条の4第1項第1号に規定する新医薬品をいう。)
については、掲示事項等告示第 10 第2号(1)に規定する新医薬品に係る投薬期間制限
(14 日分を限度とする。)が適用されるが、新たに当該制限の例外とした新医薬品は、
次のとおりであること。
・リブマーリ内用液 10mg/mL
3
薬価基準の一部改正に伴う留意事項について
(1) カムザイオスカプセル1mg、同カプセル 2.5mg 及び同カプセル5mg
① 本製剤の効能又は効果に関連する注意において、「症候性の閉塞性肥大型心筋
症患者に投与すること。」及び「「17.臨床成績」の項の内容を熟知し、臨床試験
に組み入れられた患者の背景(前治療、併用薬、左室駆出率等)を十分理解した
上で、最新のガイドライン等を参照し、適応患者を選択すること。」とされてい
るので、使用に当たっては十分留意すること。
② 本製剤の用法及び用量に関連する注意において、「投与開始前に心エコー検査
により左室駆出率(LVEF)を評価し、LVEF が 55%未満の患者には投与を開始しな
いこと。」とされているので、投与開始に当たっては、左室駆出率の計測年月日
及び左室駆出率の値を診療報酬明細書の摘要欄に記載すること。なお、他の医療
機関で左室駆出率を測定した場合には、当該測定結果及び医療機関名を記載する
ことで差し支えない。
(2) ビヨントラ錠 400mg
① 本製剤の効能又は効果に関連する注意において、「本剤の適用にあたっては、
最新のガイドライン等を参照し、トランスサイレチンアミロイドーシスの診断が
確定していることを確認すること。」とされているので、日本循環器学会の最新
のガイドライン等に従い、トランスサイレチンアミロイドーシスの診断及び治療
に精通した医師のもとで、本製剤の投与が適切と判断される症例に使用すること。