よむ、つかう、まなぶ。
資料2-3 外国での新たな措置の報告状況[1.1MB] (46 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_38901.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第3回 3/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
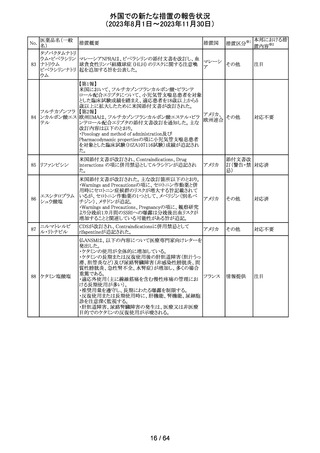
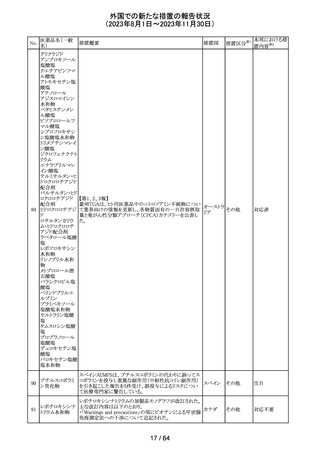
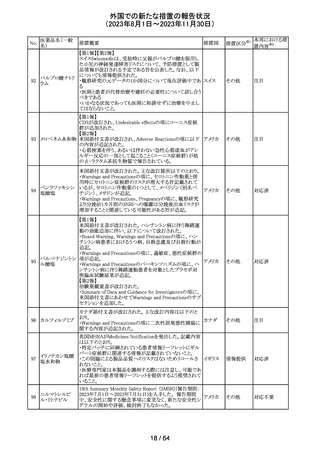
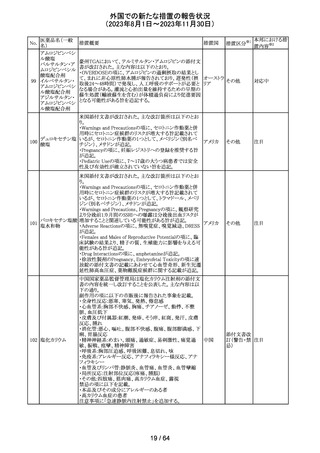
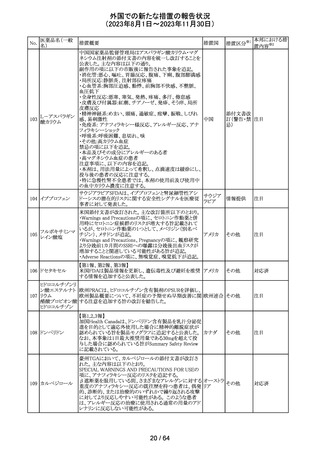
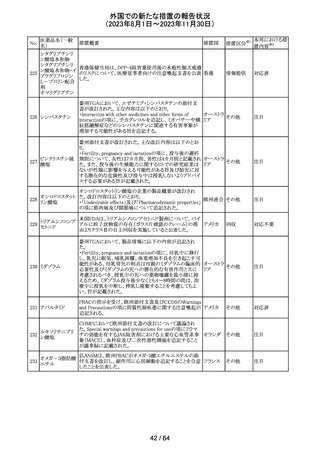
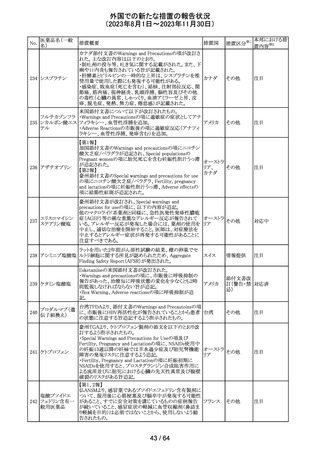
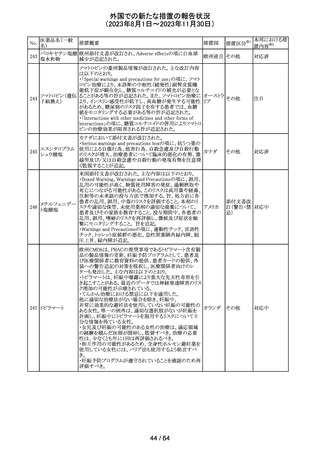
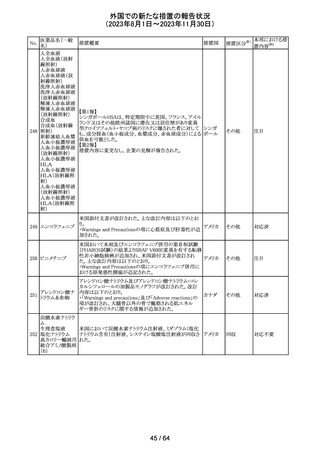
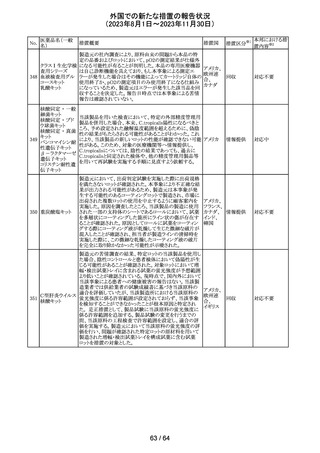
外国での新たな措置の報告状況
(2023年8月1日~2023年11月30日)
No.
医薬品名(一般
名)
措置概要
措置国
米国添付文書が改訂された。主な内容は以下のとおり。
・Boxed Warning、Warnings and Precautionsの項に、誤用、
乱用の可能性が高く、物質使用障害の発症、過剰摂取や
死亡につながる可能性がある。このリスクは高用量や経鼻、
注射等の未承認の投与方法で増加する。処方前に各患者
リスデキサンフェ の乱用、誤用、中毒のリスクを評価すること。本剤のリスクや
253
アメリカ
タミンメシル酸塩 適切な保管、未使用薬剤の適切な廃棄について、患者及
びその家族を教育すること。投与期間中、各患者の乱用、
誤用、嗜癖のリスクを再評価し、徴候及び症状を頻繁にモ
ニタリングすること。が追記。
・Warnings and Precautionsの項に、運動性チック、言語性
チック、トゥレット症候群の悪化が追記。
254 バクロフェン
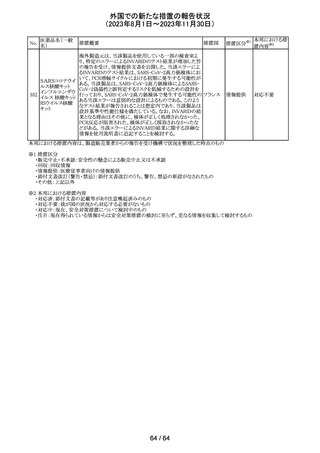
措置区分※1
本邦における措
置内容※2
添付文書改
訂(警告・禁 対応済
忌)
豪TGAより、経口バクロフェンにおけるアルコール依存症患
者に対する適応外使用での過量投与リスクについて医療 オーストラ
その他
専門家へ注意喚起された。うつ病又は過去の自殺未遂歴 リア
のある患者についてはより厳重な監視が必要である。
注目
CCDSが改訂された。主な改訂内容は以下のとおり。
ドキソルビシン塩 ・Special Warnings and Precautions for Use及びPost255
アメリカ
酸塩
Marketing Adverse Reactionsの項に間質性肺疾患が追記
された。
その他
対応済
CCDSが改訂された。
・Posology and method of administrationの項に経口カプセ
ル剤の服用方法として、食道刺激の可能性を避けるため
に、コップ一杯の水とともに服用し、服用後30分は横になら
ないことを推奨する旨、追記。
クリンダマイシンリ
・Special warnings and precautions for useの項に、経口カ
ン酸エステル
256
プセル剤への注意として、食道炎及び食道潰瘍のリスクが アメリカ
クリンダマイシン
あるため、投与ガイダンスを遵守することが重要である旨、
塩酸塩
追記。
・Special warnings and precautions for useの項に、静注製
剤への注意として、ボーラスとして原液で静脈内に注入さ
れるべきではなく、少なくとも10-60 分かけて投与するべき
である旨、追記。
その他
注目
257
ジャマイカで配布された添付文書に誤った適応症(HER2
ペルツズマブ(遺
陽性乳癌の術後薬物療法)が含まれていた旨が医療関係 スイス
伝子組換え)
者に通知された。
情報提供
対応不要
258
米国FDAは、無菌性保証欠如のためフェニレフリン/塩化
トロピカミド・フェ
ナトリウム含有バイアル製剤、点眼薬について、クラスⅡの アメリカ
ニレフリン塩酸塩
自主回収を実施していると公表した。
回収
対応不要
ドネペジル塩酸
塩
259 リバスチグミン
ガランタミン臭化
水素酸塩
ニュージーランドMedSafeは、QT延長及びTorsade de
pointesのリスクを記載するため、アセチルコチンエステラー
ニュー
ゼ阻害剤のデータシートのSpecial warnings and
ジーラン その他
precautions for use、Interaction with other medicines and
ド
other forms of interactionの項を改訂すべきであると勧告し
た。
ベバシズマブ(遺
特定ロットのベバシズマブ製品について回収が行われてい
260 伝子組換え)[後
アメリカ
る。
続4]
回収
PRACは急性汎発性発疹性膿疱症との関連があるとして、
欧州添付文書の改訂が必要と判断した。欧州添付文書の
Undesirable effectsの項に急性汎発性発疹性膿疱症が追 欧州連
ゲムシタビン塩酸
261
記される予定。また、他の重篤薬疹であるスティーヴンス・ 合、
その他
塩
ジョンソン症候群及び中毒性表皮壊死融解症についてゲ オランダ
ムシタビンの欧州添付文書のUndesirable effectsの項に記
載済みであることが言及されている。
262
ファリシマブ(遺
伝子組換え)
米国添付文書が改訂された。主な内容は以下のとおり。
・Warnings and Precautions、Adverse Reactionsの項に、網 アメリカ
膜血管炎、網膜血管閉塞が追記。
46 / 64
その他
対応済
対応不要
注目
対応中
(2023年8月1日~2023年11月30日)
No.
医薬品名(一般
名)
措置概要
措置国
米国添付文書が改訂された。主な内容は以下のとおり。
・Boxed Warning、Warnings and Precautionsの項に、誤用、
乱用の可能性が高く、物質使用障害の発症、過剰摂取や
死亡につながる可能性がある。このリスクは高用量や経鼻、
注射等の未承認の投与方法で増加する。処方前に各患者
リスデキサンフェ の乱用、誤用、中毒のリスクを評価すること。本剤のリスクや
253
アメリカ
タミンメシル酸塩 適切な保管、未使用薬剤の適切な廃棄について、患者及
びその家族を教育すること。投与期間中、各患者の乱用、
誤用、嗜癖のリスクを再評価し、徴候及び症状を頻繁にモ
ニタリングすること。が追記。
・Warnings and Precautionsの項に、運動性チック、言語性
チック、トゥレット症候群の悪化が追記。
254 バクロフェン
措置区分※1
本邦における措
置内容※2
添付文書改
訂(警告・禁 対応済
忌)
豪TGAより、経口バクロフェンにおけるアルコール依存症患
者に対する適応外使用での過量投与リスクについて医療 オーストラ
その他
専門家へ注意喚起された。うつ病又は過去の自殺未遂歴 リア
のある患者についてはより厳重な監視が必要である。
注目
CCDSが改訂された。主な改訂内容は以下のとおり。
ドキソルビシン塩 ・Special Warnings and Precautions for Use及びPost255
アメリカ
酸塩
Marketing Adverse Reactionsの項に間質性肺疾患が追記
された。
その他
対応済
CCDSが改訂された。
・Posology and method of administrationの項に経口カプセ
ル剤の服用方法として、食道刺激の可能性を避けるため
に、コップ一杯の水とともに服用し、服用後30分は横になら
ないことを推奨する旨、追記。
クリンダマイシンリ
・Special warnings and precautions for useの項に、経口カ
ン酸エステル
256
プセル剤への注意として、食道炎及び食道潰瘍のリスクが アメリカ
クリンダマイシン
あるため、投与ガイダンスを遵守することが重要である旨、
塩酸塩
追記。
・Special warnings and precautions for useの項に、静注製
剤への注意として、ボーラスとして原液で静脈内に注入さ
れるべきではなく、少なくとも10-60 分かけて投与するべき
である旨、追記。
その他
注目
257
ジャマイカで配布された添付文書に誤った適応症(HER2
ペルツズマブ(遺
陽性乳癌の術後薬物療法)が含まれていた旨が医療関係 スイス
伝子組換え)
者に通知された。
情報提供
対応不要
258
米国FDAは、無菌性保証欠如のためフェニレフリン/塩化
トロピカミド・フェ
ナトリウム含有バイアル製剤、点眼薬について、クラスⅡの アメリカ
ニレフリン塩酸塩
自主回収を実施していると公表した。
回収
対応不要
ドネペジル塩酸
塩
259 リバスチグミン
ガランタミン臭化
水素酸塩
ニュージーランドMedSafeは、QT延長及びTorsade de
pointesのリスクを記載するため、アセチルコチンエステラー
ニュー
ゼ阻害剤のデータシートのSpecial warnings and
ジーラン その他
precautions for use、Interaction with other medicines and
ド
other forms of interactionの項を改訂すべきであると勧告し
た。
ベバシズマブ(遺
特定ロットのベバシズマブ製品について回収が行われてい
260 伝子組換え)[後
アメリカ
る。
続4]
回収
PRACは急性汎発性発疹性膿疱症との関連があるとして、
欧州添付文書の改訂が必要と判断した。欧州添付文書の
Undesirable effectsの項に急性汎発性発疹性膿疱症が追 欧州連
ゲムシタビン塩酸
261
記される予定。また、他の重篤薬疹であるスティーヴンス・ 合、
その他
塩
ジョンソン症候群及び中毒性表皮壊死融解症についてゲ オランダ
ムシタビンの欧州添付文書のUndesirable effectsの項に記
載済みであることが言及されている。
262
ファリシマブ(遺
伝子組換え)
米国添付文書が改訂された。主な内容は以下のとおり。
・Warnings and Precautions、Adverse Reactionsの項に、網 アメリカ
膜血管炎、網膜血管閉塞が追記。
46 / 64
その他
対応済
対応不要
注目
対応中