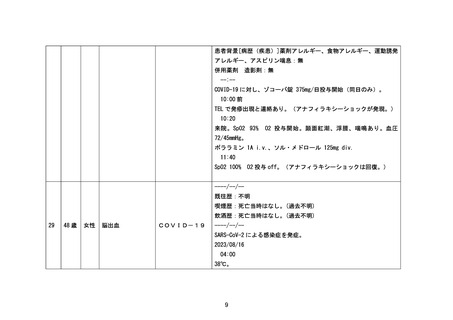
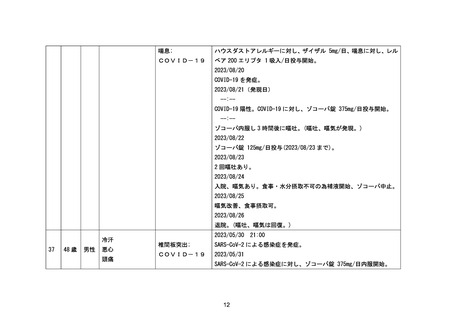
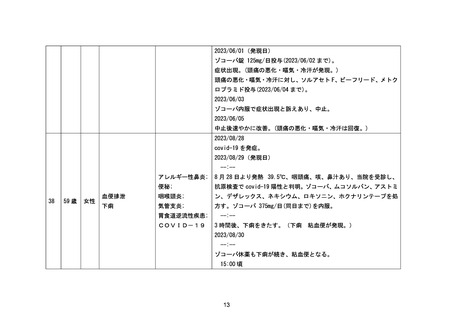
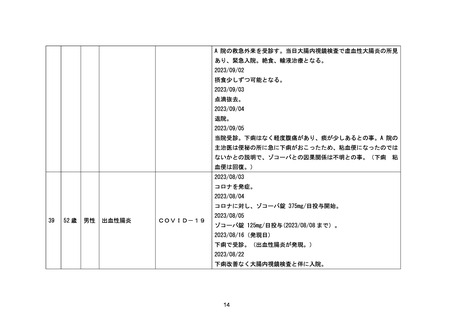
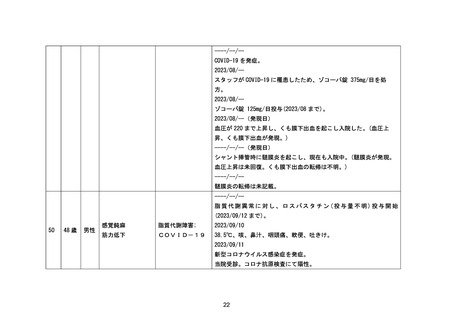
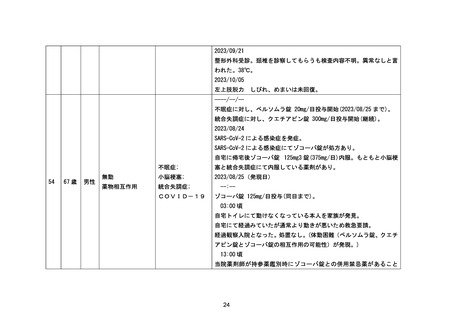
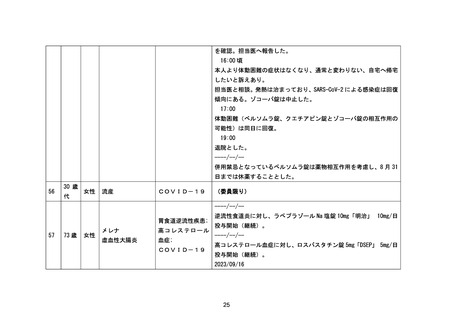
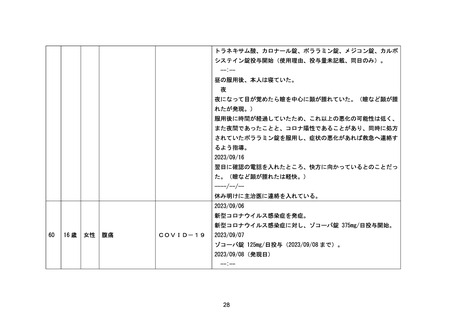
資料1-3-2 緊急承認された医薬品の市販後安全対策について [9.2MB] (92 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_38901.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和5年度第3回 3/22)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
中等度以上の肝機能障害患者での安全性
重要な不足情報とした理由:
中等度以上の肝機能障害患者での投与経験はなく、これらの患者に投与した際に本剤の血中
濃度が上昇する可能性があり、それに伴い安全性上の懸念が生じる可能性は否定できないこ
とから、中等度以上の肝機能障害患者での安全性を設定した。
医薬品安全性監視活動の内容及びその選択理由:
【内容】
・ 通常の医薬品安全性監視活動
・ 追加の医薬品安全性監視活動として、肝機能障害を有する被験者を対象とした臨床薬理試
験を実施する。
【選択理由】
上記医薬品安全性監視活動によって、肝機能障害を有する者の薬物動態を評価するため。
リスク最小化活動の内容及びその選択理由:
【内容】
・ 通常のリスク最小化活動として、電子添文の「9.3 肝機能障害患者」の項及び患者向医薬
品ガイドに記載して注意喚起を行う。
【選択理由】
肝機能障害を有する患者への投与に関する十分な情報がないこと、中等度以上の肝機能障害
患者では本剤の血中濃度が上昇する可能性があることを医療従事者及び患者に提供し、適正
使用に関する理解を促すため。
- 5 -
92