よむ、つかう、まなぶ。
03【資料1-1】新型コロナワクチンの接種について (23 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_31559.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会(第45回 3/7)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
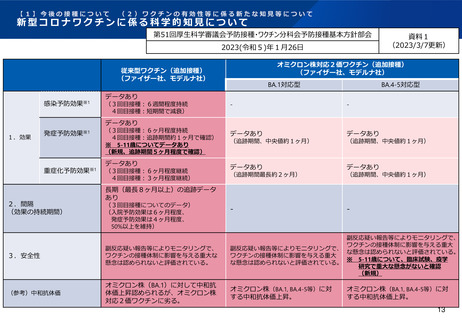
【1】今後の接種について
(3)小児に対する接種について
①
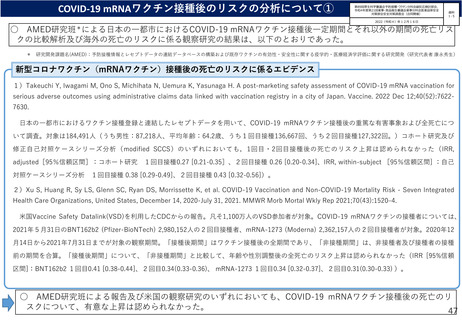
オミクロン株対応2価ワクチンの有効性、安全性及び諸外国等の状況について
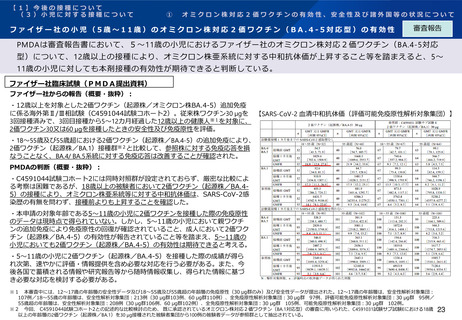
ファイザー社の小児(5歳~11歳)のオミクロン株対応2価ワクチン(BA.4-5対応型)の有効性
審査報告
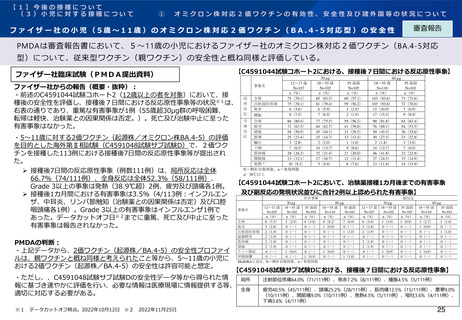
PMDAは審査報告書において、5~11歳の小児におけるファイザー社のオミクロン株対応2価ワクチン(BA.4-5対応
型)について、12歳以上の接種により、オミクロン株亜系統に対する中和抗体価が上昇すること等を踏まえると、5~
11歳の小児に対しても本剤接種の有効性が期待できると判断している。
ファイザー社臨床試験(PMDA提出資料)
ファイザー社からの報告(概要・抜粋):
・12歳以上を対象とした2価ワクチン(起源株/オミクロン株BA.4-5)追加免疫
に係る海外第Ⅱ/Ⅲ相試験(C4591044試験コホート2)。従来株ワクチン30 µgを 【SARS-CoV-2 血清中和抗体価(評価可能免疫原性解析対象集団)】
3回接種済みで、3回目接種から5~12カ月経過した12歳以上の健康人※1を対象に、
2価ワクチン30又は60 µgを接種したときの安全性及び免疫原性を評価。
・18~55歳及び55歳超における2価ワクチン(起源株/BA.4-5)の追加免疫により、
2価ワクチン(起源株/BA.1)接種群※2と比較して、参照株に対する免疫応答を損
なうことなく、BA.4/ BA.5系統に対する免疫応答は改善することが確認された。
PMDAの判断(概要・抜粋):
・C4591044試験コホート2には同時対照群が設定されておらず、厳密な比較によ
る考察は困難であるが、18歳以上の被験者において2価ワクチン(起源株/BA.45)の接種により、オミクロン株亜系統等に対する中和抗体価は、SARS-CoV-2感
染歴の有無を問わず、接種前よりも上昇することを確認した。
・本申請の対象年齢である5~11歳の小児に2価ワクチンを接種した際の免疫原性
のデータは現時点で得られていない。しかし、5~11歳の小児において親ワクチ
ンの追加免疫により免疫原性の回復が確認されていること、成人において2価ワク
チン(起源株/BA.4-5)の有効性が報告されていること等を踏まえ、5~11歳の
小児においても2価ワクチン(起源株/BA.4-5)の有効性は期待できると考える。
・5~11歳の小児に2価ワクチン(起源株/BA.4-5)を接種した際の成績が得ら
れ次第、速やかに評価・情報提供を含め必要な対応を行う必要がある。また、今
後各国で蓄積される情報や研究報告等から随時情報収集し、得られた情報に基づ
き必要な対応を検討する必要がある。
※1 本審査中には、12~17歳の年齢層の安全性データ及び18~55歳及び55歳超の年齢層の免疫原性(30 µg群のみ)及び安全性データが提出された。12~17歳の年齢層は、安全性解析対象集団:
107例/18~55歳の年齢層は、安全性解析対象集団:213例(30 μg群103例、60 μg群110例)、全免疫原性解析対象集団:30 μg群 97例、評価可能免疫原性解析対象集団:30 μg群 95例/
55歳超の年齢層は、安全性解析対象集団:208例(30 μg群106例、60 μg群102例)、全免疫原性解析対象集団:30 μg群 105例、可能免疫原性解析対象集団:30 μg群 102例。
※2 今回、 C4591044試験コホート2との記述的な比較検討のため、 既に承認されているオミクロン株対応2価ワクチン(BA.1対応型)の審査に用いられた、C4591031試験サブ試験Eにおける18歳
以上の年齢層の2価ワクチン(起源株/BA.1)を30 μg接種された被験者集団から100例の被験者データが参照群として抽出されている。
23
(3)小児に対する接種について
①
オミクロン株対応2価ワクチンの有効性、安全性及び諸外国等の状況について
ファイザー社の小児(5歳~11歳)のオミクロン株対応2価ワクチン(BA.4-5対応型)の有効性
審査報告
PMDAは審査報告書において、5~11歳の小児におけるファイザー社のオミクロン株対応2価ワクチン(BA.4-5対応
型)について、12歳以上の接種により、オミクロン株亜系統に対する中和抗体価が上昇すること等を踏まえると、5~
11歳の小児に対しても本剤接種の有効性が期待できると判断している。
ファイザー社臨床試験(PMDA提出資料)
ファイザー社からの報告(概要・抜粋):
・12歳以上を対象とした2価ワクチン(起源株/オミクロン株BA.4-5)追加免疫
に係る海外第Ⅱ/Ⅲ相試験(C4591044試験コホート2)。従来株ワクチン30 µgを 【SARS-CoV-2 血清中和抗体価(評価可能免疫原性解析対象集団)】
3回接種済みで、3回目接種から5~12カ月経過した12歳以上の健康人※1を対象に、
2価ワクチン30又は60 µgを接種したときの安全性及び免疫原性を評価。
・18~55歳及び55歳超における2価ワクチン(起源株/BA.4-5)の追加免疫により、
2価ワクチン(起源株/BA.1)接種群※2と比較して、参照株に対する免疫応答を損
なうことなく、BA.4/ BA.5系統に対する免疫応答は改善することが確認された。
PMDAの判断(概要・抜粋):
・C4591044試験コホート2には同時対照群が設定されておらず、厳密な比較によ
る考察は困難であるが、18歳以上の被験者において2価ワクチン(起源株/BA.45)の接種により、オミクロン株亜系統等に対する中和抗体価は、SARS-CoV-2感
染歴の有無を問わず、接種前よりも上昇することを確認した。
・本申請の対象年齢である5~11歳の小児に2価ワクチンを接種した際の免疫原性
のデータは現時点で得られていない。しかし、5~11歳の小児において親ワクチ
ンの追加免疫により免疫原性の回復が確認されていること、成人において2価ワク
チン(起源株/BA.4-5)の有効性が報告されていること等を踏まえ、5~11歳の
小児においても2価ワクチン(起源株/BA.4-5)の有効性は期待できると考える。
・5~11歳の小児に2価ワクチン(起源株/BA.4-5)を接種した際の成績が得ら
れ次第、速やかに評価・情報提供を含め必要な対応を行う必要がある。また、今
後各国で蓄積される情報や研究報告等から随時情報収集し、得られた情報に基づ
き必要な対応を検討する必要がある。
※1 本審査中には、12~17歳の年齢層の安全性データ及び18~55歳及び55歳超の年齢層の免疫原性(30 µg群のみ)及び安全性データが提出された。12~17歳の年齢層は、安全性解析対象集団:
107例/18~55歳の年齢層は、安全性解析対象集団:213例(30 μg群103例、60 μg群110例)、全免疫原性解析対象集団:30 μg群 97例、評価可能免疫原性解析対象集団:30 μg群 95例/
55歳超の年齢層は、安全性解析対象集団:208例(30 μg群106例、60 μg群102例)、全免疫原性解析対象集団:30 μg群 105例、可能免疫原性解析対象集団:30 μg群 102例。
※2 今回、 C4591044試験コホート2との記述的な比較検討のため、 既に承認されているオミクロン株対応2価ワクチン(BA.1対応型)の審査に用いられた、C4591031試験サブ試験Eにおける18歳
以上の年齢層の2価ワクチン(起源株/BA.1)を30 μg接種された被験者集団から100例の被験者データが参照群として抽出されている。
23