よむ、つかう、まなぶ。
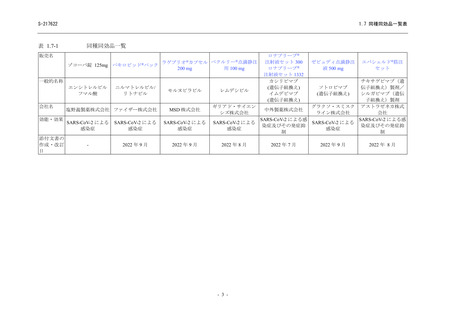
【資料No.1】1.7_同種同効品一覧表 (24 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29325.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会(令和4年度第5回 11/22)、医薬品第二部会(令和4年度第13回 11/22)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
*21. 承認条件
21.1 医薬品リスク管理計画を策定の上、適切に実施するこ
と。
21.2 新規変異株の流行が懸念される場合、当該変異株に対
する中和活性等を速やかに検討し、その結果を厚生労働
省に提出すること。
21.3 本剤の有効性が減弱するおそれがある変異株が流行し
ている場合は、新規変異株に対する中和活性、新規変異
株の地域ごとの流行状況等を踏まえ、適切な患者に対し
て投与するよう医師に対して要請するなど、本剤の適正
な使用が確保されるよう必要な措置を講じること。
22. 包装
〈ロナプリーブ注射液セット300〉
カシリビマブ製剤2.5mL×1バイアル及び
イムデビマブ製剤2.5mL×1バイアル
〈ロナプリーブ注射液セット1332〉
カシリビマブ製剤11.1mL×1バイアル及び
イムデビマブ製剤11.1mL×1バイアル
23. 主要文献
1)JV43180試験及びCOV-2067試験薬物動態結果(2021年
7月19日承認、CTD2.7.2.2)
2)JV43180試験薬物動態結果(2021年11月5日承認、
CTD2.7.2.2.2)
3)COV-2067試験有効性結果(2021年7月19日承認、
CTD2.5.4.2)
4)COV-2067試験安全性結果(2021年7月19日承認、
CTD2.5.5.2)
5)COV-2069試験有効性結果(2021年11月5日承認、
CTD2.5.4.3)
6)COV-2069試験安全性結果(2021年11月5日承認、
CTD2.5.5)
7)ウイルス中和試験(2021年7月19日承認、
CTD2.6.2.2.4)
8)低温電子顕微鏡を用いたSARS-CoV-2 RBDへの結合
特性(2021年7月19日承認、CTD2.6.2.2.2)
9)REGN10933及びREGN10987のSARS-CoV-2 RBD
に対する競合的結合特性(2021年7月19日承認、
CTD2.6.2.2.3)
10)Antiviral Resistance(Section 15)(2022年1月改訂
版、FDA FACT SHEET FOR HEALTH CARE
PROVIDERS EUA OF REGEN-COVⓇ(casirivimab
and imdevimab))
11)REGN10933及びREGN10987のスパイクタンパク質に対
する中和試験(2021年7月19日承認、CTD4.2.1.1-5)
24. 文献請求先及び問い合わせ先
中外製薬株式会社 メディカルインフォメーション部
〒103-8324 東京都中央区日本橋室町2-1-1
電話:0120-189706
Fax:0120-189705
https://www.chugai-pharm.co.jp/
26. 製造販売業者等
26.1 製造販売元
Ⓡ F.ホフマン・ラ・ロシュ社(スイス)登録商標
(5)
21.1 医薬品リスク管理計画を策定の上、適切に実施するこ
と。
21.2 新規変異株の流行が懸念される場合、当該変異株に対
する中和活性等を速やかに検討し、その結果を厚生労働
省に提出すること。
21.3 本剤の有効性が減弱するおそれがある変異株が流行し
ている場合は、新規変異株に対する中和活性、新規変異
株の地域ごとの流行状況等を踏まえ、適切な患者に対し
て投与するよう医師に対して要請するなど、本剤の適正
な使用が確保されるよう必要な措置を講じること。
22. 包装
〈ロナプリーブ注射液セット300〉
カシリビマブ製剤2.5mL×1バイアル及び
イムデビマブ製剤2.5mL×1バイアル
〈ロナプリーブ注射液セット1332〉
カシリビマブ製剤11.1mL×1バイアル及び
イムデビマブ製剤11.1mL×1バイアル
23. 主要文献
1)JV43180試験及びCOV-2067試験薬物動態結果(2021年
7月19日承認、CTD2.7.2.2)
2)JV43180試験薬物動態結果(2021年11月5日承認、
CTD2.7.2.2.2)
3)COV-2067試験有効性結果(2021年7月19日承認、
CTD2.5.4.2)
4)COV-2067試験安全性結果(2021年7月19日承認、
CTD2.5.5.2)
5)COV-2069試験有効性結果(2021年11月5日承認、
CTD2.5.4.3)
6)COV-2069試験安全性結果(2021年11月5日承認、
CTD2.5.5)
7)ウイルス中和試験(2021年7月19日承認、
CTD2.6.2.2.4)
8)低温電子顕微鏡を用いたSARS-CoV-2 RBDへの結合
特性(2021年7月19日承認、CTD2.6.2.2.2)
9)REGN10933及びREGN10987のSARS-CoV-2 RBD
に対する競合的結合特性(2021年7月19日承認、
CTD2.6.2.2.3)
10)Antiviral Resistance(Section 15)(2022年1月改訂
版、FDA FACT SHEET FOR HEALTH CARE
PROVIDERS EUA OF REGEN-COVⓇ(casirivimab
and imdevimab))
11)REGN10933及びREGN10987のスパイクタンパク質に対
する中和試験(2021年7月19日承認、CTD4.2.1.1-5)
24. 文献請求先及び問い合わせ先
中外製薬株式会社 メディカルインフォメーション部
〒103-8324 東京都中央区日本橋室町2-1-1
電話:0120-189706
Fax:0120-189705
https://www.chugai-pharm.co.jp/
26. 製造販売業者等
26.1 製造販売元
Ⓡ F.ホフマン・ラ・ロシュ社(スイス)登録商標
(5)