よむ、つかう、まなぶ。
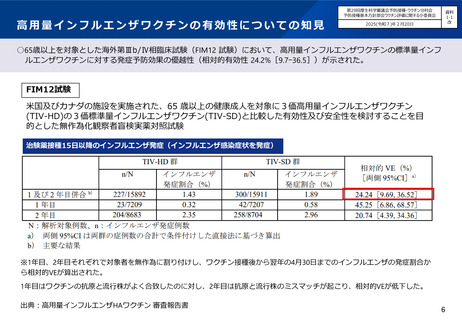
04資料1-2高用量インフルエンザワクチンについて (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_64997.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会 ワクチン評価に関する小委員会(第32回 10/22)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
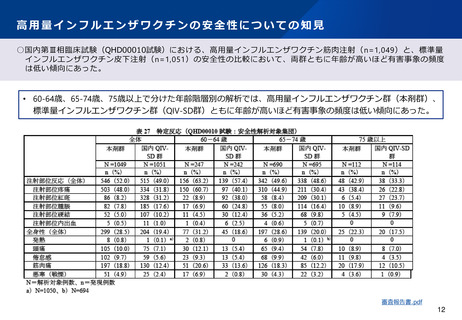
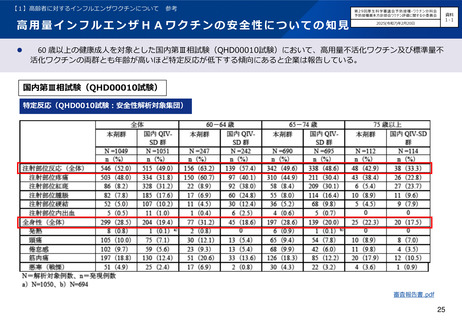
高用量インフルエンザワクチンの安全性についての知見
○国内第Ⅲ相臨床試験(QHD00010試験)における、高用量インフルエンザワクチン筋肉注射(n=1,049)と、標準量
インフルエンザワクチン皮下注射(n=1,051)の安全性の比較において、高用量インフルエンザワクチン群が発熱等
の有害事象の頻度が高い傾向にあったが、重篤な有害事象の頻度は同等であった。
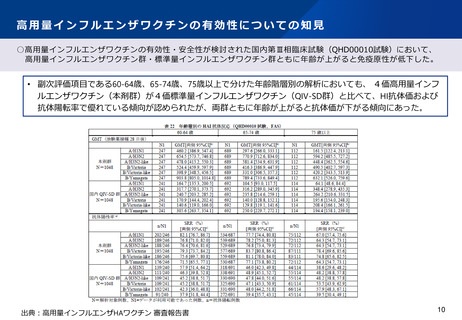
• 7日以内の特定反応のうち、注射部位反応の発現割合は、 4価高用量インフルエンザワクチン(HD-IIV4)群
(52.0%)が、 4価標準量インフルエンザワクチン(SD-IIV4)群(49.0%)よりわずかに高かったが、
Grade3の報告はHD-IIV4群(0.9%)と SD-IIV4群(1.3%)で同等であった。7日以内の特定反応のうち、全身
性の反応の発現割合は、 HD-IIV4群(28.5%)がSD-IIV4群(19.4%)より高い傾向にあったが、Grade3の報告
はHD-IIV4群(0.5%)とSD-IIV4群(0.2%)で同等であった。発熱は、 HD-IIV4群で8例(0.8%)、 SD-IIV4群
で1例(<0.1%)あり、39度以上はHD-IIV4群で3例認めた。
• 重篤な有害事象はHD-IIV4群で2例(0.2%)、 SD-IIV4群で5例(0.5%)認められたが、 HD-IIV4群について
はいずれも因果関係は否定された。
• 治験中止に至った有害事象についてはHD-IIV4群で1例(<0.1%)、 SD-IIV4群で3例(0.3%)認められたが、
いずれも因果関係は否定された。
• 死亡例の報告はなかった。
出典:高齢者に対するインフルエンザワクチンファクトシート(文献45)
11
○国内第Ⅲ相臨床試験(QHD00010試験)における、高用量インフルエンザワクチン筋肉注射(n=1,049)と、標準量
インフルエンザワクチン皮下注射(n=1,051)の安全性の比較において、高用量インフルエンザワクチン群が発熱等
の有害事象の頻度が高い傾向にあったが、重篤な有害事象の頻度は同等であった。
• 7日以内の特定反応のうち、注射部位反応の発現割合は、 4価高用量インフルエンザワクチン(HD-IIV4)群
(52.0%)が、 4価標準量インフルエンザワクチン(SD-IIV4)群(49.0%)よりわずかに高かったが、
Grade3の報告はHD-IIV4群(0.9%)と SD-IIV4群(1.3%)で同等であった。7日以内の特定反応のうち、全身
性の反応の発現割合は、 HD-IIV4群(28.5%)がSD-IIV4群(19.4%)より高い傾向にあったが、Grade3の報告
はHD-IIV4群(0.5%)とSD-IIV4群(0.2%)で同等であった。発熱は、 HD-IIV4群で8例(0.8%)、 SD-IIV4群
で1例(<0.1%)あり、39度以上はHD-IIV4群で3例認めた。
• 重篤な有害事象はHD-IIV4群で2例(0.2%)、 SD-IIV4群で5例(0.5%)認められたが、 HD-IIV4群について
はいずれも因果関係は否定された。
• 治験中止に至った有害事象についてはHD-IIV4群で1例(<0.1%)、 SD-IIV4群で3例(0.3%)認められたが、
いずれも因果関係は否定された。
• 死亡例の報告はなかった。
出典:高齢者に対するインフルエンザワクチンファクトシート(文献45)
11