よむ、つかう、まなぶ。
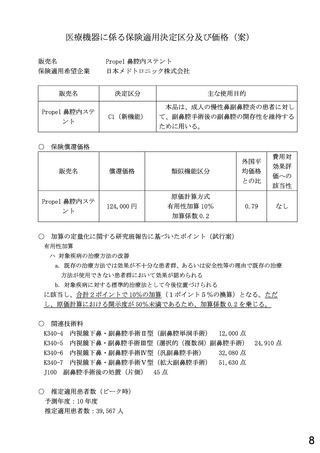
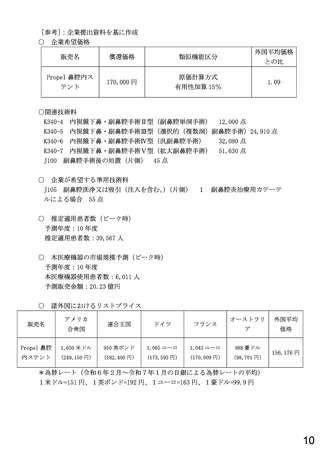
総-1医療機器の保険適用について (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_59560.html |
| 出典情報 | 中央社会保険医療協議会 総会(第612回 7/16)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
製品概要
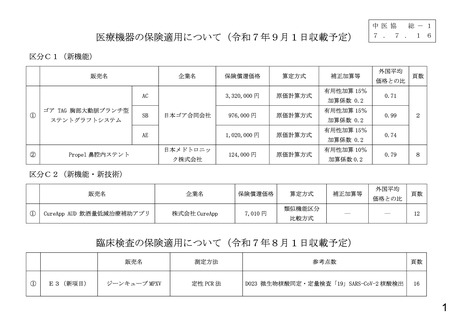
1 販売名
Propel鼻腔内ステント
2 希望企業 日本メドトロニック株式会社
3 使用目的
本品は、成人の慢性鼻副鼻腔炎の患者に対して、副鼻腔手術後の副鼻
腔の開存性を維持するために用いる。
製品特徴
出典:企業提出資料
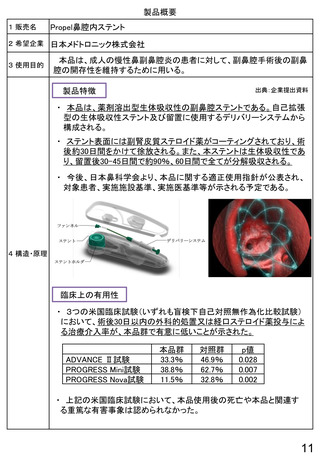
・ 本品は、薬剤溶出型生体吸収性の副鼻腔ステントである。自己拡張
型の生体吸収性ステント及び留置に使用するデリバリーシステムから
構成される。
・ ステント表面には副腎皮質ステロイド薬がコーティングされており、術
後約30日間をかけて徐放される。また、本ステントは生体吸収性であ
り、留置後30-45日間で約90%、60日間で全てが分解吸収される。
・ 今後、日本鼻科学会より、本品に関する適正使用指針が公表され、
対象患者、実施施設基準、実施医基準等が示される予定である。
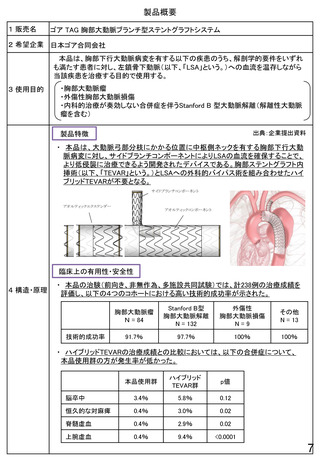
4 構造・原理
臨床上の有用性
・ 3つの米国臨床試験(いずれも盲検下自己対照無作為化比較試験)
において、術後30日以内の外科的処置又は経口ステロイド薬投与によ
る治療介入率が、本品群で有意に低いことが示された。
ADVANCE Ⅱ試験
PROGRESS Mini試験
PROGRESS Nova試験
本品群
33.3%
38.8%
11.5%
対照群
46.9%
62.7%
32.8%
p値
0.028
0.007
0.002
・ 上記の米国臨床試験において、本品使用後の死亡や本品と関連す
る重篤な有害事象は認められなかった。
11
1 販売名
Propel鼻腔内ステント
2 希望企業 日本メドトロニック株式会社
3 使用目的
本品は、成人の慢性鼻副鼻腔炎の患者に対して、副鼻腔手術後の副鼻
腔の開存性を維持するために用いる。
製品特徴
出典:企業提出資料
・ 本品は、薬剤溶出型生体吸収性の副鼻腔ステントである。自己拡張
型の生体吸収性ステント及び留置に使用するデリバリーシステムから
構成される。
・ ステント表面には副腎皮質ステロイド薬がコーティングされており、術
後約30日間をかけて徐放される。また、本ステントは生体吸収性であ
り、留置後30-45日間で約90%、60日間で全てが分解吸収される。
・ 今後、日本鼻科学会より、本品に関する適正使用指針が公表され、
対象患者、実施施設基準、実施医基準等が示される予定である。
4 構造・原理
臨床上の有用性
・ 3つの米国臨床試験(いずれも盲検下自己対照無作為化比較試験)
において、術後30日以内の外科的処置又は経口ステロイド薬投与によ
る治療介入率が、本品群で有意に低いことが示された。
ADVANCE Ⅱ試験
PROGRESS Mini試験
PROGRESS Nova試験
本品群
33.3%
38.8%
11.5%
対照群
46.9%
62.7%
32.8%
p値
0.028
0.007
0.002
・ 上記の米国臨床試験において、本品使用後の死亡や本品と関連す
る重篤な有害事象は認められなかった。
11