よむ、つかう、まなぶ。
【参考資料6】アルドシカ錠20mg並びにザルティア錠2.5mg及び同錠5mgの添付文書 (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_58149.html |
| 出典情報 | 医療用から要指導・一般用への転用に関する評価検討会議(第32回 5/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
められた。血藤中のメチルカテコール体はメチルカテコロールグルクロン酸抱
合体の10%未満であった%⑳ (外国人データ)。
16.5 排洪
健康成人6例に“C-タダラブイィル100mg\D を単回経口投与したときの、投与後
312時間までの放射能回収率は開便中60.5%、尿中36.1%であった。畑便中には
主にメチルカテコール体、カテコール体、尿中には主にメチルカテコールグルク
ロン酸抱合体及びカテコールグルクロン酸抱合体が認められた2 (外国人データ)。
16.6 特定の背景を有する患者
16.6.1 否障害上患者
(1) 軽度及び中等度腎障害患者
健康成人12例、軽度腎障害患者 (CLcr=51一80mL/min) 8例、中等度腎障害
患者 (CLcr=31一50mL/min) 8例にタダラフィル5mg及び10mgまり を単回経
口投与したとき、AUCo-=及びCraは健康成人のそれぞれ約100%及び20一30%
増加した⑳ (外国人データ)。[7.1、9.2.2参照]
(2) 血液透析を受けている末期腎不全患者
血液秀析を受けている末期覧不全愚者16例にタダラブフィル5mg、10mg及び
20mg*り を単回経口投与したとき、AUCo-s及びCagは健康成人のそれぞれ約
109%及び41%増加 した⑳ (外国人データ)。[9.2.1参照]
16.6.2 肝障害思者
健康成人8例及び肝障害患者25例中 にタダラフィル10mgD を単回経口投与し
たとき、軽度肝障害患者 (Child-Pugh class A) と中等度肝障害患者 (Child-
Pugh class B) のAUCo-sは健康成人とほぼ同様であった (外国人データ)。
注6) 軽微肝障害 (脂肪肝が認められた患者)、n=8:軽度肛障害 (Child-Pugh
class A)、n=8:中等度肝隊害 (Child-Pugh class B)、n=8:重度肝障害
(Child-Pugh class C)、n=1。
16.6.3 高齢者
健康高齢者12例 (65一78歳) 及び健康若年者12例 (19一45歳) にタダラフィ
ル10mgきり を単回経口投与したとき、Csxは高齢者と若年者とでほば同様で
あったが、高齢者のAUCo-sは若年者に比べ約25%高値であった2 (外国人デー
タ)。[9.8参照]
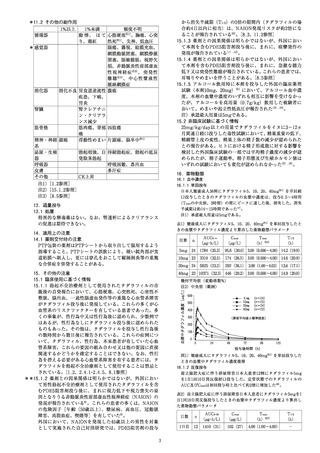
表3) 高齢填及び若年者にタダラフィル10mgきり を単回投与したときの血茜中タ
ダラブフィル測度より算出した薬物動態パラメータ
AUCo-s Canax Trmax Ta
(wg'h代) (ug人ル) (h) 9 (⑪)
高齢者 | 12 | 4881 (31.7) | 196 (269) | 200 (100一400) | 21.6 (390)
若年者 | 12 | 3896 (426) | 183 (255) | 250 00一600) | 169 (291)
幾何平均値 (変動係数%)
注7) 中央値 (範囲)
16.7 薬物相互作用
16.7.1 経ロケトコナゾール
健康成人12例にケトコナゾール400mg (1日1回経口投与、国内未革売) とタ
ダラフィル20mgり を併用投与したとき、タダラフィルのAUC。-s及びCa。。は、
それぞれ312%及び22%増加した9 (外国人データ)。
健康成人11例にケトコナゾール200mg (1日1回経口投与) とタダラフィル
10mgきり を併用投与したとき、タダラフィルのAUCo-s及びCrsxはそれぞれ
107%及び15%増加した (外国人データ)。[10.1参照]
16.7.2 リトナビル
健康成人16例にリトナビル500mg又は600mg (1日2回) とタダラフィル
20mg*り を併用投与したとき、タダラフィルのCaは30%低下したが、AUC。-
sは32%増加した29⑳ (外国人データ)。
健康成人8例にリトナビル200mg (1日2回) とタダラフィル20mgきり を併用投
与したとき、タダラフィルのCasは同程度であったが、AUCo-sは124%増加し
た? (外国人データ)。[10.1参照]
16.7.3 ボセンタン
健康成人15例にタダラフィル40mg (1日1回) 及びボセンタン125mg (1日2回)
を10日間併用投与した。投与1日目におけるタダラフィルのAUC及びCzszは本
剤を単独投与時の値と同程度であったが、投与10日有目におけるタダラフィル
のAUC及びCasは本剤を単独投与時の値と比べてそれぞれ41 .5%及び26 .6%低
下した。[16.1.2参照] 一方、本剤によるボセンタンのAUC及びCasに対する
影響は認められなかった9 (外国人データ)。[10.2参照]
16.7.4 ジゴキシン
健康成人20例にジゴキシン0.25mgを1日1回反復経口投与時の定常状態で、タダ
ラフィル40mgを1日1回10日間反復経口投与した結果、本剤によるジゴキシンの
AUC、 Cr及びCrに対する明らかな影響は認められなかった (外国人データ)。
16.7.5 q遮断剤
(1) ドキサゾシン
健康成人18例にドキサゾシン8mgを反復経口投与時の定常状態で、タダラフィ
ル20mg*り を単回経口投与したとき、立位の収縮期及び拡張期血圧の最大下
降時はそれぞれ9.81mmHg及び5.33mmHg、唄位の収縮期及び拡張期血圧の
最大下降量はそれぞれ3.64mmHg及び2.78mmHgであった7? (外国人データ)。
健康成人45例にドキサゾシン (4mgまで尊増) とタダラフィル5mgり を1日1
回反復経口授号したとき、ドキサゾシンの血圧降下作用に増強がみられた。
この試験において、和失神等の症状を伴う血圧変化に関する有害事象がみられ
た (外国人データ)。[10.2参照]
(2) タムスロシン
健康成人18例にタムスロシン0.4mgを反復経口投与時の定常状態で、タダラ
フィル10mg双は20mgきけり を単回投与したとき、立位の収縮期及び拡張期血圧
の最大下降量はそれぞれ2.3mmHg及び2.2mmHg、陰位の収縮期及び拡張期
10!
血圧の最大下隆量はそれぞれ3.2mmHg及び3.0mmHgであり、有明らかな血圧
への影響は認められなかった7? (外国人データ)。
健康成人39例にタムスロシン0.4mgとタダラフィル5mg*り を1日1回反復経口
投与したとき、明らかな血圧への影響は認められなかった (外国人データ)。
16.7.6 経口避妊薬
健康成人26例に経口避妊薬 (エチニルエストラジオール0.03mg及びレボノル
ゲダストレル0.15mg含有製剤) とタダラブフィル40mgを21日間併用投与した結
果、エチニルエストラジオールのAUC及びCaxは、経口避妊薬とプラセボを
併用投与したときの値と比べてそれぞれ26%及び70%増加 した。タダラフィル
併用投与時とプラセボ併用投与時でレボノルゲストレルの血中濃度に統計
学的に有意な差は認められなかった2 (外国人データ)。
16.7.7 その他の薬剤
他剤 (ニザチジン、制酸配合剤) 又はアルコールが本剤 (10又は20mgきり) に
及ぼす影響について検討した結果、ニザチジン、制酸配合剤奴はアルコールに
よる本剤の薬物動態に対する明らかな影響は認められなかった。 また、 本剤 (10
又は20mgきり) が他剤 (ミダゾラム、テオフィリン、ワルファリン及びアムロ
ジピン) 又はアルコールに及ぼすずす影響について検討した結果、本剤によるミダ
ゾラム、テオフィリン、ワルファリン、アムロジピン又はアルロールの薬物動
惑に対する明らかな影響は認められなかった9-9 9 7 :33) -3%) (外国人データ)。
7. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国際共同第息相試験
肺動脈性肺高血圧症患者 (405例、 日本人愚者26例を含む) を対象に本剤
2.5mg、10mg、20mgtり、40mg又はプラセボのいずれかを1日1回投与する18
週間 (16週間の投与期間) の多施設共同無作為化プアラセボ対照二重盲検比
試験を実施した。その結果、運動耐容能を評価する6分間歩行距離の投与開始
前から16週後の変化量において、本剤40mg群はプラセボ群に比べて統計学的
に有意に改善した (ゎ=0.0004)。隆床症状の悪化 (死亡、肺移植、心房中隔
裂開術、肺動脈性肺高血圧症悪化による入院、肺動脈性肺高血圧症に対する
新たな治療の開始叉はWHO機能分類の悪化を臨床症状の悪化と定義した) が
認められた被験者数はプラセボ群で13例 (15.9%) に対し、本剤40mg群で4例
(5.1%) であった。また、本剤40mg群は、一部の被験者で測定された肺血行
動態パラメータの平均肺動脈圧、肺血管抵抗係数、心係数及び心拍出量にお
いて、投与開始前と比べ改善が認められた。
なお、本試験ではQOLを評価するため、8項目の健康概念[身体機能、日常役
割機能 (身体)、身体の痛み、全体的健康感、活力、社会生活機能、日常役割
機能 (精神)、心の健康] からなるSF-36v2健康調査球、及び5つの質問 (移
動の程度、身の回りの管理、ふだんの活動、痛み/不快感、不安/ふさぎ込み)
と健康状態のQOLを判定するためのビジュアルアナログスケール (VAS) か
らなるEuroQol質問票を使用した。本剤40mg群は、SF-36v2健康調査票の6項
目 [身体機能、日常役割機能 (身体)、身体の痛み、全体的健康感、活力、社
会生活機能] において、またEuroQol質問票の効用値 [fndex Score (US) 及
びIndex Score (UK)] 及びVASにおいて、プラセボポ和群に比べ統計学的に有意
な改善が認められた (p<0.05) めの。
注1) 承認用量は40mgである。
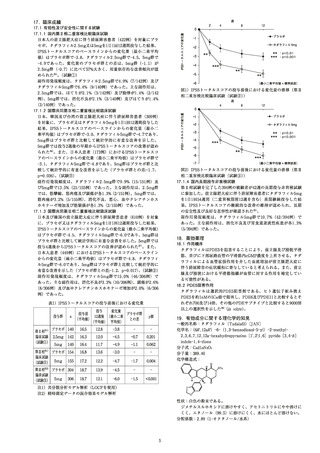
表1) 投与開始前から16週後の変化量
ュ ュ ニュ タダラフィル
評価項目 統計量 プラセボ和群 40me才
ー 平均値 9.21 41.14
MA (95%信問区間) | (-422一2265) | (29855242)
[症例数] [79] [76]
、 平均値 -221 -427
MM (95%信頼区間) (-7.24一2.82) (-7.53一-1.01)
8 [定例数] [14] [15]
肺血管抵抗係数 平均値 4.13 -117.05
(dyne・sec/cm?/ | (95%信頼区間) (-101.22一109.48) (-244.79一10.68)
m) [症例数] [121 [14]
心係数 平均値 -001 036
60 の の (95%信頼区間) (-044一0.41) (009-0.3)
[症例数] [2] [14]
、 平均値 -500 -200
MM (95%信頼区間) (-13.74一3.74) (-964~5.64)
8 [症例数] [141 [5]
本試験では、エンドセリン受容体牛抗剤でもるボセンタンとの併用による影響を
評価するため、ボセンタン治療の有無別に6分間歩行距離の変化量の部分集団解
析を実施した (ボセンタン併用被験者:53.3%)。その結果、本剤40mg群ではボセ
ンタン非併用被験者のみプラセボ群に比べ統計学的に有意な改善が認められた。
表2) 投与開始前から16週後の変化量
きき 計 ニ タダラフィル
評価項目 純計生 プラャボ本| タフフィ
ー 平均値 -2.89 42.18
ンーm] | (95%信痕区商) | (-2284一1706) | (2667-5769
[人数] [35] [37
ラニ 平均値 18.84 40.15
シンテン | (95%信区間) | (050-3719) | (2315719
[人数] [44 [39
合体の10%未満であった%⑳ (外国人データ)。
16.5 排洪
健康成人6例に“C-タダラブイィル100mg\D を単回経口投与したときの、投与後
312時間までの放射能回収率は開便中60.5%、尿中36.1%であった。畑便中には
主にメチルカテコール体、カテコール体、尿中には主にメチルカテコールグルク
ロン酸抱合体及びカテコールグルクロン酸抱合体が認められた2 (外国人データ)。
16.6 特定の背景を有する患者
16.6.1 否障害上患者
(1) 軽度及び中等度腎障害患者
健康成人12例、軽度腎障害患者 (CLcr=51一80mL/min) 8例、中等度腎障害
患者 (CLcr=31一50mL/min) 8例にタダラフィル5mg及び10mgまり を単回経
口投与したとき、AUCo-=及びCraは健康成人のそれぞれ約100%及び20一30%
増加した⑳ (外国人データ)。[7.1、9.2.2参照]
(2) 血液透析を受けている末期腎不全患者
血液秀析を受けている末期覧不全愚者16例にタダラブフィル5mg、10mg及び
20mg*り を単回経口投与したとき、AUCo-s及びCagは健康成人のそれぞれ約
109%及び41%増加 した⑳ (外国人データ)。[9.2.1参照]
16.6.2 肝障害思者
健康成人8例及び肝障害患者25例中 にタダラフィル10mgD を単回経口投与し
たとき、軽度肝障害患者 (Child-Pugh class A) と中等度肝障害患者 (Child-
Pugh class B) のAUCo-sは健康成人とほぼ同様であった (外国人データ)。
注6) 軽微肝障害 (脂肪肝が認められた患者)、n=8:軽度肛障害 (Child-Pugh
class A)、n=8:中等度肝隊害 (Child-Pugh class B)、n=8:重度肝障害
(Child-Pugh class C)、n=1。
16.6.3 高齢者
健康高齢者12例 (65一78歳) 及び健康若年者12例 (19一45歳) にタダラフィ
ル10mgきり を単回経口投与したとき、Csxは高齢者と若年者とでほば同様で
あったが、高齢者のAUCo-sは若年者に比べ約25%高値であった2 (外国人デー
タ)。[9.8参照]
表3) 高齢填及び若年者にタダラフィル10mgきり を単回投与したときの血茜中タ
ダラブフィル測度より算出した薬物動態パラメータ
AUCo-s Canax Trmax Ta
(wg'h代) (ug人ル) (h) 9 (⑪)
高齢者 | 12 | 4881 (31.7) | 196 (269) | 200 (100一400) | 21.6 (390)
若年者 | 12 | 3896 (426) | 183 (255) | 250 00一600) | 169 (291)
幾何平均値 (変動係数%)
注7) 中央値 (範囲)
16.7 薬物相互作用
16.7.1 経ロケトコナゾール
健康成人12例にケトコナゾール400mg (1日1回経口投与、国内未革売) とタ
ダラフィル20mgり を併用投与したとき、タダラフィルのAUC。-s及びCa。。は、
それぞれ312%及び22%増加した9 (外国人データ)。
健康成人11例にケトコナゾール200mg (1日1回経口投与) とタダラフィル
10mgきり を併用投与したとき、タダラフィルのAUCo-s及びCrsxはそれぞれ
107%及び15%増加した (外国人データ)。[10.1参照]
16.7.2 リトナビル
健康成人16例にリトナビル500mg又は600mg (1日2回) とタダラフィル
20mg*り を併用投与したとき、タダラフィルのCaは30%低下したが、AUC。-
sは32%増加した29⑳ (外国人データ)。
健康成人8例にリトナビル200mg (1日2回) とタダラフィル20mgきり を併用投
与したとき、タダラフィルのCasは同程度であったが、AUCo-sは124%増加し
た? (外国人データ)。[10.1参照]
16.7.3 ボセンタン
健康成人15例にタダラフィル40mg (1日1回) 及びボセンタン125mg (1日2回)
を10日間併用投与した。投与1日目におけるタダラフィルのAUC及びCzszは本
剤を単独投与時の値と同程度であったが、投与10日有目におけるタダラフィル
のAUC及びCasは本剤を単独投与時の値と比べてそれぞれ41 .5%及び26 .6%低
下した。[16.1.2参照] 一方、本剤によるボセンタンのAUC及びCasに対する
影響は認められなかった9 (外国人データ)。[10.2参照]
16.7.4 ジゴキシン
健康成人20例にジゴキシン0.25mgを1日1回反復経口投与時の定常状態で、タダ
ラフィル40mgを1日1回10日間反復経口投与した結果、本剤によるジゴキシンの
AUC、 Cr及びCrに対する明らかな影響は認められなかった (外国人データ)。
16.7.5 q遮断剤
(1) ドキサゾシン
健康成人18例にドキサゾシン8mgを反復経口投与時の定常状態で、タダラフィ
ル20mg*り を単回経口投与したとき、立位の収縮期及び拡張期血圧の最大下
降時はそれぞれ9.81mmHg及び5.33mmHg、唄位の収縮期及び拡張期血圧の
最大下降量はそれぞれ3.64mmHg及び2.78mmHgであった7? (外国人データ)。
健康成人45例にドキサゾシン (4mgまで尊増) とタダラフィル5mgり を1日1
回反復経口授号したとき、ドキサゾシンの血圧降下作用に増強がみられた。
この試験において、和失神等の症状を伴う血圧変化に関する有害事象がみられ
た (外国人データ)。[10.2参照]
(2) タムスロシン
健康成人18例にタムスロシン0.4mgを反復経口投与時の定常状態で、タダラ
フィル10mg双は20mgきけり を単回投与したとき、立位の収縮期及び拡張期血圧
の最大下降量はそれぞれ2.3mmHg及び2.2mmHg、陰位の収縮期及び拡張期
10!
血圧の最大下隆量はそれぞれ3.2mmHg及び3.0mmHgであり、有明らかな血圧
への影響は認められなかった7? (外国人データ)。
健康成人39例にタムスロシン0.4mgとタダラフィル5mg*り を1日1回反復経口
投与したとき、明らかな血圧への影響は認められなかった (外国人データ)。
16.7.6 経口避妊薬
健康成人26例に経口避妊薬 (エチニルエストラジオール0.03mg及びレボノル
ゲダストレル0.15mg含有製剤) とタダラブフィル40mgを21日間併用投与した結
果、エチニルエストラジオールのAUC及びCaxは、経口避妊薬とプラセボを
併用投与したときの値と比べてそれぞれ26%及び70%増加 した。タダラフィル
併用投与時とプラセボ併用投与時でレボノルゲストレルの血中濃度に統計
学的に有意な差は認められなかった2 (外国人データ)。
16.7.7 その他の薬剤
他剤 (ニザチジン、制酸配合剤) 又はアルコールが本剤 (10又は20mgきり) に
及ぼす影響について検討した結果、ニザチジン、制酸配合剤奴はアルコールに
よる本剤の薬物動態に対する明らかな影響は認められなかった。 また、 本剤 (10
又は20mgきり) が他剤 (ミダゾラム、テオフィリン、ワルファリン及びアムロ
ジピン) 又はアルコールに及ぼすずす影響について検討した結果、本剤によるミダ
ゾラム、テオフィリン、ワルファリン、アムロジピン又はアルロールの薬物動
惑に対する明らかな影響は認められなかった9-9 9 7 :33) -3%) (外国人データ)。
7. 臨床成績
17.1 有効性及び安全性に関する試験
17.1.1 国際共同第息相試験
肺動脈性肺高血圧症患者 (405例、 日本人愚者26例を含む) を対象に本剤
2.5mg、10mg、20mgtり、40mg又はプラセボのいずれかを1日1回投与する18
週間 (16週間の投与期間) の多施設共同無作為化プアラセボ対照二重盲検比
試験を実施した。その結果、運動耐容能を評価する6分間歩行距離の投与開始
前から16週後の変化量において、本剤40mg群はプラセボ群に比べて統計学的
に有意に改善した (ゎ=0.0004)。隆床症状の悪化 (死亡、肺移植、心房中隔
裂開術、肺動脈性肺高血圧症悪化による入院、肺動脈性肺高血圧症に対する
新たな治療の開始叉はWHO機能分類の悪化を臨床症状の悪化と定義した) が
認められた被験者数はプラセボ群で13例 (15.9%) に対し、本剤40mg群で4例
(5.1%) であった。また、本剤40mg群は、一部の被験者で測定された肺血行
動態パラメータの平均肺動脈圧、肺血管抵抗係数、心係数及び心拍出量にお
いて、投与開始前と比べ改善が認められた。
なお、本試験ではQOLを評価するため、8項目の健康概念[身体機能、日常役
割機能 (身体)、身体の痛み、全体的健康感、活力、社会生活機能、日常役割
機能 (精神)、心の健康] からなるSF-36v2健康調査球、及び5つの質問 (移
動の程度、身の回りの管理、ふだんの活動、痛み/不快感、不安/ふさぎ込み)
と健康状態のQOLを判定するためのビジュアルアナログスケール (VAS) か
らなるEuroQol質問票を使用した。本剤40mg群は、SF-36v2健康調査票の6項
目 [身体機能、日常役割機能 (身体)、身体の痛み、全体的健康感、活力、社
会生活機能] において、またEuroQol質問票の効用値 [fndex Score (US) 及
びIndex Score (UK)] 及びVASにおいて、プラセボポ和群に比べ統計学的に有意
な改善が認められた (p<0.05) めの。
注1) 承認用量は40mgである。
表1) 投与開始前から16週後の変化量
ュ ュ ニュ タダラフィル
評価項目 統計量 プラセボ和群 40me才
ー 平均値 9.21 41.14
MA (95%信問区間) | (-422一2265) | (29855242)
[症例数] [79] [76]
、 平均値 -221 -427
MM (95%信頼区間) (-7.24一2.82) (-7.53一-1.01)
8 [定例数] [14] [15]
肺血管抵抗係数 平均値 4.13 -117.05
(dyne・sec/cm?/ | (95%信頼区間) (-101.22一109.48) (-244.79一10.68)
m) [症例数] [121 [14]
心係数 平均値 -001 036
60 の の (95%信頼区間) (-044一0.41) (009-0.3)
[症例数] [2] [14]
、 平均値 -500 -200
MM (95%信頼区間) (-13.74一3.74) (-964~5.64)
8 [症例数] [141 [5]
本試験では、エンドセリン受容体牛抗剤でもるボセンタンとの併用による影響を
評価するため、ボセンタン治療の有無別に6分間歩行距離の変化量の部分集団解
析を実施した (ボセンタン併用被験者:53.3%)。その結果、本剤40mg群ではボセ
ンタン非併用被験者のみプラセボ群に比べ統計学的に有意な改善が認められた。
表2) 投与開始前から16週後の変化量
きき 計 ニ タダラフィル
評価項目 純計生 プラャボ本| タフフィ
ー 平均値 -2.89 42.18
ンーm] | (95%信痕区商) | (-2284一1706) | (2667-5769
[人数] [35] [37
ラニ 平均値 18.84 40.15
シンテン | (95%信区間) | (050-3719) | (2315719
[人数] [44 [39