よむ、つかう、まなぶ。
03資料1予防接種事務デジタル化及び接種記録の保存期間について[6.2MB] (46 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_36952.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会(第59回 3/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
副反応疑い報告制度における報告事項
令和2年1月27日予防接種基本方針部会資料改編
第95回厚生科学審議会予防接種・
ワクチン分科会副反応検討部会
2023(令和5)年9月1日
資料
1
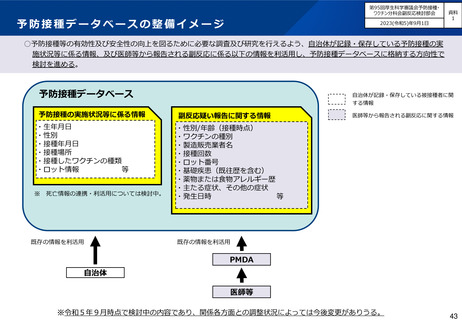
〇 予防接種後の有害事象に関する情報を適切に収集し、評価を行うため、ワクチンに関する情報、接種時
の状況、発生した症状の概要及び転帰等について、報告するよう定めている。
報告事項
○予防接種法上の定期接種・任意接種の別:
○患者情報:氏名又はイニシャル、性別、接種時年齢、住所、生年月日
○報告者情報:氏名、医療機関名、電話番号、住所
○接種場所:医療機関名、住所
○ワクチン情報:ワクチンの種類、ロット番号、製造販売業者、接種回数
○接種の状況:接種日、出生体重、接種前の体温、家族歴、予診票での留意点
○症状の概要:症状、発生日時、本剤との因果関係、他要因の可能性の有無
概要
○症状の程度:重い(1.死亡、2.障害、3.死亡につながるおそれ、
4.障害につながるおそれ、5.入院、6.上記1~5に準じて重い、
7.後世代における先天性の疾病又は異常)、重くない
○症状の転帰:回復、軽快、未回復、後遺症、死亡、不明
○報告者意見
○報告回数
45
令和2年1月27日予防接種基本方針部会資料改編
第95回厚生科学審議会予防接種・
ワクチン分科会副反応検討部会
2023(令和5)年9月1日
資料
1
〇 予防接種後の有害事象に関する情報を適切に収集し、評価を行うため、ワクチンに関する情報、接種時
の状況、発生した症状の概要及び転帰等について、報告するよう定めている。
報告事項
○予防接種法上の定期接種・任意接種の別:
○患者情報:氏名又はイニシャル、性別、接種時年齢、住所、生年月日
○報告者情報:氏名、医療機関名、電話番号、住所
○接種場所:医療機関名、住所
○ワクチン情報:ワクチンの種類、ロット番号、製造販売業者、接種回数
○接種の状況:接種日、出生体重、接種前の体温、家族歴、予診票での留意点
○症状の概要:症状、発生日時、本剤との因果関係、他要因の可能性の有無
概要
○症状の程度:重い(1.死亡、2.障害、3.死亡につながるおそれ、
4.障害につながるおそれ、5.入院、6.上記1~5に準じて重い、
7.後世代における先天性の疾病又は異常)、重くない
○症状の転帰:回復、軽快、未回復、後遺症、死亡、不明
○報告者意見
○報告回数
45