よむ、つかう、まなぶ。
参考資料4 新型コロナワクチン「コミナティ筋注6ヵ月~4歳用」(ファイザー株式会社)審査報告書 (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00053.html |
| 出典情報 | 第87回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第16回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
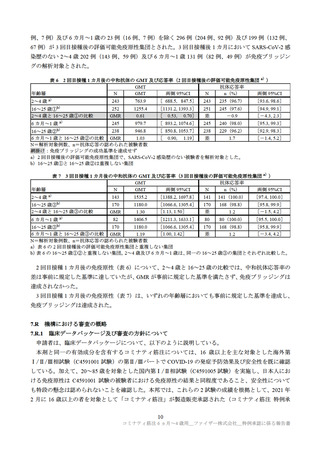
での評価が計画されているが、本申請では表 1 に示す 6 カ月~1 歳及び 2~4 歳の年齢層に係る成績が提
出された。
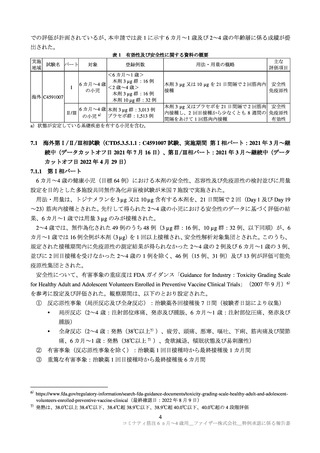
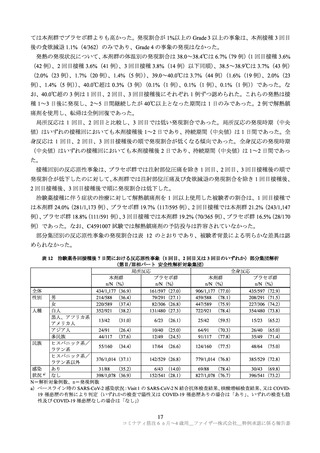
表 1 有効性及び安全性に関する資料の概要
実施
試験名 パート
地域
対象
登録例数
用法・用量の概略
主な
評価項目
Ⅰ
<6 カ月~1 歳>
本剤 3 µg 群:16 例
6 カ月~4 歳
<2 歳~4 歳>
の小児
本剤 3 µg 群:16 例
本剤 10 µg 群:32 例
本剤 3 µg 又は 10 µg を 21 日間隔で 2 回筋肉内 安全性
接種
免疫原性
Ⅱ/Ⅲ
6 カ月~4 歳 本剤 3 µg 群:3,013 例
の小児 a) プラセボ群:1,513 例
本剤 3 µg 又はプラセボを 21 日間隔で 2 回筋肉 安全性
内接種し、2 回目接種から少なくとも 8 週間の 免疫原性
間隔をあけて 1 回筋肉内接種
有効性
海外 C4591007
a)状態が安定している基礎疾患を有する小児を含む。
7.1 海外第Ⅰ/Ⅱ/Ⅲ相試験(CTD5.3.5.1.1:C4591007 試験、実施期間 第Ⅰ相パート:2021 年 3 月~継
続中(データカットオフ日 2021 年 7 月 16 日)、第Ⅱ/Ⅲ相パート:2021 年 3 月~継続中(データ
カットオフ日 2022 年 4 月 29 日)
7.1.1 第Ⅰ相パート
6 カ月~4 歳の健康小児(目標 64 例)における本剤の安全性、忍容性及び免疫原性の検討並びに用量
設定を目的とした多施設共同無作為化非盲検試験が米国 7 施設で実施された。
用法・用量は、トジナメランを 3 µg 又は 10 µg 含有する本剤を、21 日間隔で 2 回(Day 1 及び Day 19
~23)筋肉内接種とされた。先行して得られた 2~4 歳の小児における安全性のデータに基づく評価の結
果、6 カ月~1 歳では用量 3 µg のみが接種された。
2~4 歳では、無作為化された 49 例のうち 48 例(3 µg 群:16 例、10 µg 群:32 例、以下同順)が、6
カ月~1 歳では 16 例全例が本剤(3 µg)を 1 回以上接種され、安全性解析対象集団とされた。このうち、
規定された接種期間内に免疫原性の測定結果が得られなかった 2~4 歳の 2 例及び 6 カ月~1 歳の 3 例、
並びに 2 回目接種を受けなかった 2~4 歳の 1 例を除く、46 例(15 例、31 例)及び 13 例が評価可能免
疫原性集団とされた。
安全性について、有害事象の重症度は FDA ガイダンス「Guidance for Industry:Toxicity Grading Scale
for Healthy Adult and Adolescent Volunteers Enrolled in Preventive Vaccine Clinical Trials」(2007 年 9 月)6)
を参考に設定及び評価された。観察期間は、以下のとおり設定された。
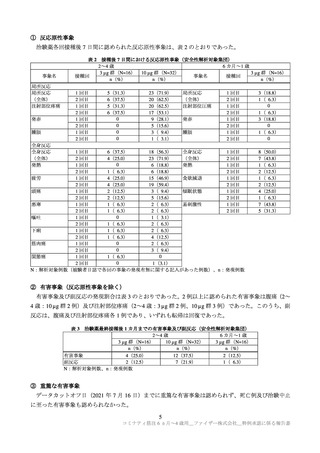
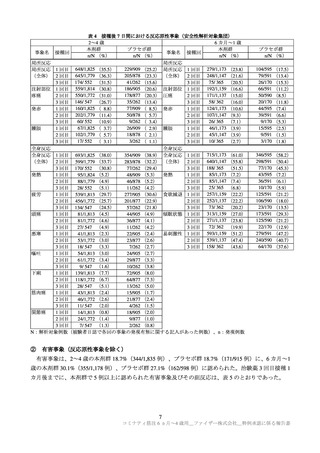
① 反応原性事象(局所反応及び全身反応):治験薬各回接種後 7 日間(被験者日誌により収集)
局所反応(2~4 歳:注射部位疼痛、発赤及び腫脹、6 カ月~1 歳:注射部位圧痛、発赤及び
腫脹)
全身反応(2~4 歳:発熱(38℃以上7))、疲労、頭痛、悪寒、嘔吐、下痢、筋肉痛及び関節
痛、6 カ月~1 歳:発熱(38℃以上 7))、食欲減退、傾眠状態及び易刺激性)
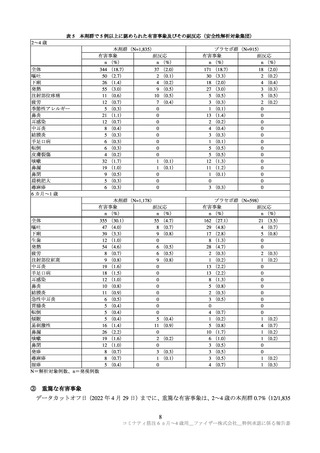
② 有害事象(反応原性事象を除く):治験薬 1 回目接種時から最終接種後 1 カ月間
③ 重篤な有害事象:治験薬 1 回目接種時から最終接種後 6 カ月間
6)https://www.fda.gov/regulatory-information/search-fda-guidance-documents/toxicity-grading-scale-healthy-adult-and-adolescent-
volunteers-enrolled-preventive-vaccine-clinical(最終確認日:2022 年 8 月 9 日)
38.4℃以下、38.4℃超 38.9℃以下、38.9℃超 40.0℃以下、40.0℃超の 4 段階評価
7)発熱は、38.0℃以上
4
コミナティ筋注 6 ヵ月~4 歳用_ファイザー株式会社_特例承認に係る報告書
出された。
表 1 有効性及び安全性に関する資料の概要
実施
試験名 パート
地域
対象
登録例数
用法・用量の概略
主な
評価項目
Ⅰ
<6 カ月~1 歳>
本剤 3 µg 群:16 例
6 カ月~4 歳
<2 歳~4 歳>
の小児
本剤 3 µg 群:16 例
本剤 10 µg 群:32 例
本剤 3 µg 又は 10 µg を 21 日間隔で 2 回筋肉内 安全性
接種
免疫原性
Ⅱ/Ⅲ
6 カ月~4 歳 本剤 3 µg 群:3,013 例
の小児 a) プラセボ群:1,513 例
本剤 3 µg 又はプラセボを 21 日間隔で 2 回筋肉 安全性
内接種し、2 回目接種から少なくとも 8 週間の 免疫原性
間隔をあけて 1 回筋肉内接種
有効性
海外 C4591007
a)状態が安定している基礎疾患を有する小児を含む。
7.1 海外第Ⅰ/Ⅱ/Ⅲ相試験(CTD5.3.5.1.1:C4591007 試験、実施期間 第Ⅰ相パート:2021 年 3 月~継
続中(データカットオフ日 2021 年 7 月 16 日)、第Ⅱ/Ⅲ相パート:2021 年 3 月~継続中(データ
カットオフ日 2022 年 4 月 29 日)
7.1.1 第Ⅰ相パート
6 カ月~4 歳の健康小児(目標 64 例)における本剤の安全性、忍容性及び免疫原性の検討並びに用量
設定を目的とした多施設共同無作為化非盲検試験が米国 7 施設で実施された。
用法・用量は、トジナメランを 3 µg 又は 10 µg 含有する本剤を、21 日間隔で 2 回(Day 1 及び Day 19
~23)筋肉内接種とされた。先行して得られた 2~4 歳の小児における安全性のデータに基づく評価の結
果、6 カ月~1 歳では用量 3 µg のみが接種された。
2~4 歳では、無作為化された 49 例のうち 48 例(3 µg 群:16 例、10 µg 群:32 例、以下同順)が、6
カ月~1 歳では 16 例全例が本剤(3 µg)を 1 回以上接種され、安全性解析対象集団とされた。このうち、
規定された接種期間内に免疫原性の測定結果が得られなかった 2~4 歳の 2 例及び 6 カ月~1 歳の 3 例、
並びに 2 回目接種を受けなかった 2~4 歳の 1 例を除く、46 例(15 例、31 例)及び 13 例が評価可能免
疫原性集団とされた。
安全性について、有害事象の重症度は FDA ガイダンス「Guidance for Industry:Toxicity Grading Scale
for Healthy Adult and Adolescent Volunteers Enrolled in Preventive Vaccine Clinical Trials」(2007 年 9 月)6)
を参考に設定及び評価された。観察期間は、以下のとおり設定された。
① 反応原性事象(局所反応及び全身反応):治験薬各回接種後 7 日間(被験者日誌により収集)
局所反応(2~4 歳:注射部位疼痛、発赤及び腫脹、6 カ月~1 歳:注射部位圧痛、発赤及び
腫脹)
全身反応(2~4 歳:発熱(38℃以上7))、疲労、頭痛、悪寒、嘔吐、下痢、筋肉痛及び関節
痛、6 カ月~1 歳:発熱(38℃以上 7))、食欲減退、傾眠状態及び易刺激性)
② 有害事象(反応原性事象を除く):治験薬 1 回目接種時から最終接種後 1 カ月間
③ 重篤な有害事象:治験薬 1 回目接種時から最終接種後 6 カ月間
6)https://www.fda.gov/regulatory-information/search-fda-guidance-documents/toxicity-grading-scale-healthy-adult-and-adolescent-
volunteers-enrolled-preventive-vaccine-clinical(最終確認日:2022 年 8 月 9 日)
38.4℃以下、38.4℃超 38.9℃以下、38.9℃超 40.0℃以下、40.0℃超の 4 段階評価
7)発熱は、38.0℃以上
4
コミナティ筋注 6 ヵ月~4 歳用_ファイザー株式会社_特例承認に係る報告書