よむ、つかう、まなぶ。
参考資料4 新型コロナワクチン「コミナティ筋注6ヵ月~4歳用」(ファイザー株式会社)審査報告書 (24 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00053.html |
| 出典情報 | 第87回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第16回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
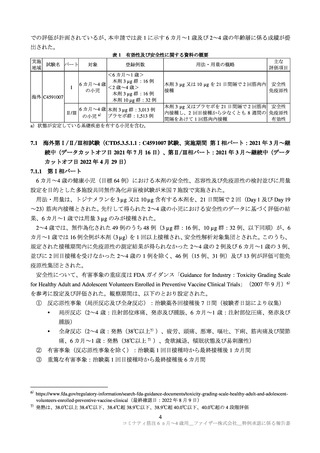
7.R.3.2 製造販売後の安全性情報について
申請者は、海外の使用許可等以降に得られた 6 カ月~4 歳の小児における安全性情報について、以下
のように説明している。
6 カ月~4 歳の小児に対する本剤の使用は 2022 年 6 月 17 日(米国の緊急使用許可)後に開始され、
現時点で使用実績が限られており、海外製造販売後の安全性情報については収集・評価中である。2022
年 7 月 15 日までの自発報告において、既承認の SARS-CoV-2 ワクチンでもリスクとして特定されてい
るショック、アナフィラキシー、心筋炎等は認められておらず、6 カ月~4 歳の小児に特有の有害事象は
認められていない。6 カ月~4 歳の小児における安全性については、C4591007 試験のフォローアップも
含む製造販売後等に得られる情報に基づき、症例評価、文献検索及びシグナル検出を引き続き行い、新
たな安全性上の懸念がないか監視を行う。なお、6 カ月~4 歳の小児への接種に際し、自覚症状(心筋
炎、心膜炎の症状含め)を訴えることが難しい年齢層であることも踏まえ、5 歳以上の小児に関する対
応と同様に、被接種者の保護者が児の体調変化等により早期に気づき、必要に応じて受診する等の対応
がとれるように、資材等にて情報提供する予定である。
機構は、以下のように考える。
海外において、SARS-CoV-2 に対する mRNA ワクチン接種後の心筋炎又は心膜炎の報告は、2 回目接
種後に多く、特に若年層の男性の 2 回目接種後に多いことが報告されている(N Engl J Med 2021; 385:
2140-9、Myopericarditis following COVID-19 vaccination: Updates from the Vaccine Adverse Event Reporting
System(VAERS)15))
。本邦では、製造販売業者からの心筋炎関連事象疑いの報告が集積されたことから、
2021 年 12 月 6 日に心筋炎及び心膜炎を副反応疑い報告基準として定め、当該リスクについて定期的な
評価が行われている。第 81 回厚生科学審議会予防接種・ワクチン分副反応検討部会、令和 4 年度第 6 回
薬事・食品衛生審議会分科会医薬品等安全対策部会安全調査会(合同開催)において製造販売業者より
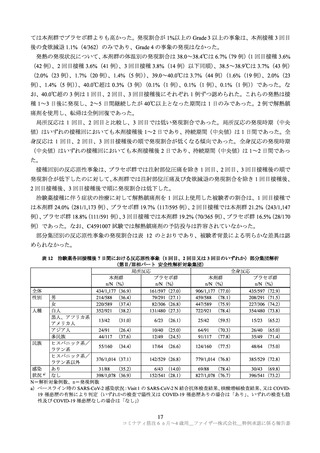
報告された心筋炎及び心膜炎疑い例の 100 万回接種当たりの報告件数(ブライトン分類レベル 4 及びレ
ベル 5 も含む全報告件数)は、コミナティ筋注を接種後(報告期間:2021 年 2 月 17 日~2022 年 6 月 12
日)では全年齢で心筋炎 0.6~3.2 件、心膜炎 0.4~1.3 件、コミナティ筋注 5~11 歳用を接種後(報告期
間:2022 年 2 月 21 日~2022 年 6 月 12 日)では心筋炎 2.3~2.6 件、心膜炎 0~1.7 件であり、現時点で
は、5 歳以上の小児を含め、ワクチンの接種体制に影響を与える程の重大な懸念は認められないと判断
された。
若年層におけるワクチン接種後の心筋炎・心膜炎の発生頻度は COVID-19 に合併する心筋炎関連事象
の発生頻度よりも低く、発現したとしてもほとんどが無症状又は軽症である(Circulation 2021; 144: 47184 等)
。加えて、コミナティ筋注 5~11 歳用接種後の発生状況を踏まえると、現時点で 6 カ月~4 歳の小
児において許容できないリスクを示唆する情報は得られていないと考える。
また、心筋炎・心膜炎以外の副反応について、現時点で 6 カ月~4 歳の小児において、ショック、ア
ナフィラキシーの報告や、当該年齢層に特有のリスクを示唆する報告は認められていない。ただし、6 カ
月~4 歳の小児における安全性情報は、海外情報も含め、引き続き収集することが重要であり、得られ
た情報に基づき適切な対応を検討する必要がある。なお、6 カ月~4 歳の小児は副反応の症状の自覚と訴
えが難しいことから、被接種者の保護者に対し、具体的な症状や受診の必要性等を資材で情報提供する
15)ACIP Presentation Slides: October 20-21, 2021 Meeting、https://www.cdc.gov/vaccines/acip/meetings/downloads/slides-2021-10-
20-21/07-COVID-Su-508.pdf(最終確認日:2022 年 8 月 9 日)
20
コミナティ筋注 6 ヵ月~4 歳用_ファイザー株式会社_特例承認に係る報告書
申請者は、海外の使用許可等以降に得られた 6 カ月~4 歳の小児における安全性情報について、以下
のように説明している。
6 カ月~4 歳の小児に対する本剤の使用は 2022 年 6 月 17 日(米国の緊急使用許可)後に開始され、
現時点で使用実績が限られており、海外製造販売後の安全性情報については収集・評価中である。2022
年 7 月 15 日までの自発報告において、既承認の SARS-CoV-2 ワクチンでもリスクとして特定されてい
るショック、アナフィラキシー、心筋炎等は認められておらず、6 カ月~4 歳の小児に特有の有害事象は
認められていない。6 カ月~4 歳の小児における安全性については、C4591007 試験のフォローアップも
含む製造販売後等に得られる情報に基づき、症例評価、文献検索及びシグナル検出を引き続き行い、新
たな安全性上の懸念がないか監視を行う。なお、6 カ月~4 歳の小児への接種に際し、自覚症状(心筋
炎、心膜炎の症状含め)を訴えることが難しい年齢層であることも踏まえ、5 歳以上の小児に関する対
応と同様に、被接種者の保護者が児の体調変化等により早期に気づき、必要に応じて受診する等の対応
がとれるように、資材等にて情報提供する予定である。
機構は、以下のように考える。
海外において、SARS-CoV-2 に対する mRNA ワクチン接種後の心筋炎又は心膜炎の報告は、2 回目接
種後に多く、特に若年層の男性の 2 回目接種後に多いことが報告されている(N Engl J Med 2021; 385:
2140-9、Myopericarditis following COVID-19 vaccination: Updates from the Vaccine Adverse Event Reporting
System(VAERS)15))
。本邦では、製造販売業者からの心筋炎関連事象疑いの報告が集積されたことから、
2021 年 12 月 6 日に心筋炎及び心膜炎を副反応疑い報告基準として定め、当該リスクについて定期的な
評価が行われている。第 81 回厚生科学審議会予防接種・ワクチン分副反応検討部会、令和 4 年度第 6 回
薬事・食品衛生審議会分科会医薬品等安全対策部会安全調査会(合同開催)において製造販売業者より
報告された心筋炎及び心膜炎疑い例の 100 万回接種当たりの報告件数(ブライトン分類レベル 4 及びレ
ベル 5 も含む全報告件数)は、コミナティ筋注を接種後(報告期間:2021 年 2 月 17 日~2022 年 6 月 12
日)では全年齢で心筋炎 0.6~3.2 件、心膜炎 0.4~1.3 件、コミナティ筋注 5~11 歳用を接種後(報告期
間:2022 年 2 月 21 日~2022 年 6 月 12 日)では心筋炎 2.3~2.6 件、心膜炎 0~1.7 件であり、現時点で
は、5 歳以上の小児を含め、ワクチンの接種体制に影響を与える程の重大な懸念は認められないと判断
された。
若年層におけるワクチン接種後の心筋炎・心膜炎の発生頻度は COVID-19 に合併する心筋炎関連事象
の発生頻度よりも低く、発現したとしてもほとんどが無症状又は軽症である(Circulation 2021; 144: 47184 等)
。加えて、コミナティ筋注 5~11 歳用接種後の発生状況を踏まえると、現時点で 6 カ月~4 歳の小
児において許容できないリスクを示唆する情報は得られていないと考える。
また、心筋炎・心膜炎以外の副反応について、現時点で 6 カ月~4 歳の小児において、ショック、ア
ナフィラキシーの報告や、当該年齢層に特有のリスクを示唆する報告は認められていない。ただし、6 カ
月~4 歳の小児における安全性情報は、海外情報も含め、引き続き収集することが重要であり、得られ
た情報に基づき適切な対応を検討する必要がある。なお、6 カ月~4 歳の小児は副反応の症状の自覚と訴
えが難しいことから、被接種者の保護者に対し、具体的な症状や受診の必要性等を資材で情報提供する
15)ACIP Presentation Slides: October 20-21, 2021 Meeting、https://www.cdc.gov/vaccines/acip/meetings/downloads/slides-2021-10-
20-21/07-COVID-Su-508.pdf(最終確認日:2022 年 8 月 9 日)
20
コミナティ筋注 6 ヵ月~4 歳用_ファイザー株式会社_特例承認に係る報告書