よむ、つかう、まなぶ。
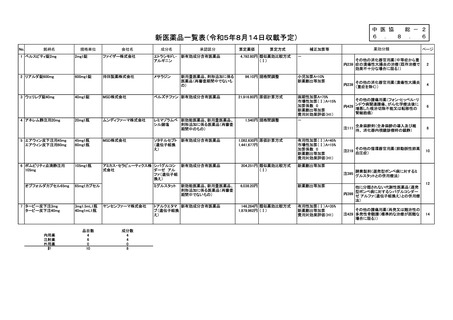
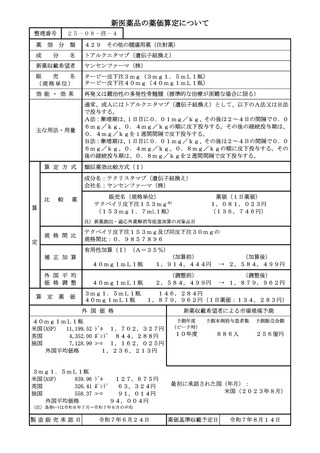
総-2医薬品の新規薬価収載について (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_60772.html |
| 出典情報 | 中央社会保険医療協議会 総会(第614回 8/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
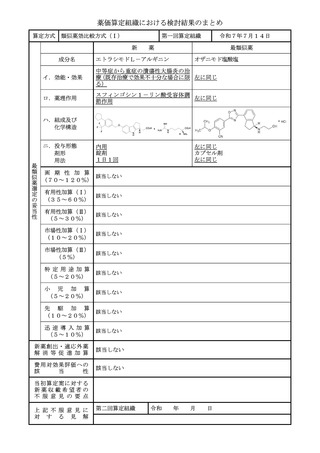
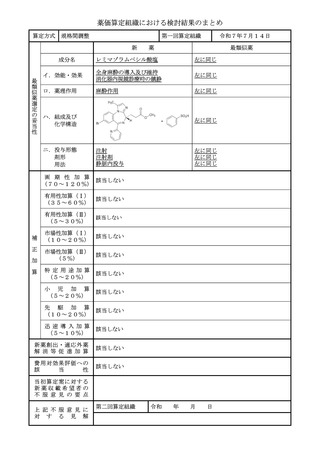
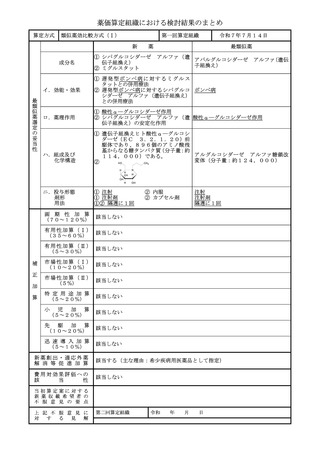
薬価算定組織における検討結果のまとめ
算定方式
原価計算方式
第一回算定組織
新
原
価
計
算
方
式
を
採
用
す
る
妥
当
性
成分名
イ.効能・効果
ロ.薬理作用
令和7年7月14日
薬
類似薬がない根拠
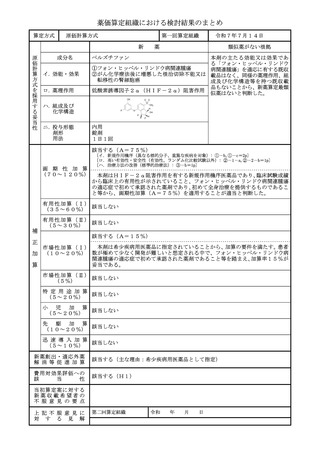
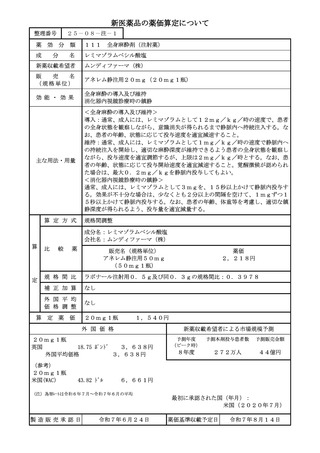
ベルズチファン
本剤の主たる効能又は効果であ
る「フォン・ヒッペル・リンドウ
①フォン・ヒッペル・リンドウ病関連腫瘍
病関連腫瘍」を適応に有する既収
②がん化学療法後に増悪した根治切除不能又は 載品はなく、同様の薬理作用、組
転移性の腎細胞癌
成及び化学構造等を持つ既収載
品もないことから、新薬算定最類
低酸素誘導因子2α(HIF-2α)阻害作用
似薬はないと判断した。
ハ.組成及び
化学構造
ニ.投与形態
剤形
用法
内用
錠剤
1日1回
該当する(A=75%)
画 期 性 加 算
(70~120%)
〔イ.新規作用機序(異なる標的分子、重篤な疾病を対象): ①-b,①-c=2p〕
〔ロ.高い有効性・安全性(有効性、ランダム化比較試験以外): ②-1-a,②-2-b=1p〕
〔ハ.治療方法の改善(標準的治療法): ③-b=1p〕
本剤はHIF-2α阻害作用を有する新規作用機序医薬品であり、臨床試験成績
から臨床上の有用性が示されていること、フォン・ヒッペル・リンドウ病関連腫瘍
の適応症で初めて承認された薬剤であり、初めて全身治療を提供するものであるこ
と等から、画期性加算(A=75%)を適用することが適当と判断した。
有用性加算(Ⅰ)
該当しない
(35~60%)
補
有用性加算(Ⅱ)
該当しない
(5~30%)
該当する(A=15%)
正
市 場 性 加 算 ( Ⅰ ) 本剤は希少疾病用医薬品に指定されていることから、加算の要件を満たす。患者
(10~20%) 数が極めて少なく開発が難しいと想定される中で、フォン・ヒッペル・リンドウ病
関連腫瘍の適応症で初めて承認された薬剤であること等を踏まえ、加算率15%が
妥当である。
算
加
市場性加算(Ⅱ)
該当しない
(5%)
特 定 用 途 加 算
該当しない
(5~20%)
小
児 加 算
該当しない
(5~20%)
先 駆 加 算
該当しない
(10~20%)
迅 速 導 入 加 算
該当しない
(5~10%)
新薬創出・適応外薬
解 消 等 促 進 加 算
該当する(主な理由:希少疾病用医薬品として指定)
費用対効果評価への
該
当
性
該当する(H1)
当初算定案に対する
新薬収載希望者の
不 服 意 見 の 要 点
上 記 不 服 意 見 に
対 す る 見 解
第二回算定組織
令和
7
年
月
日
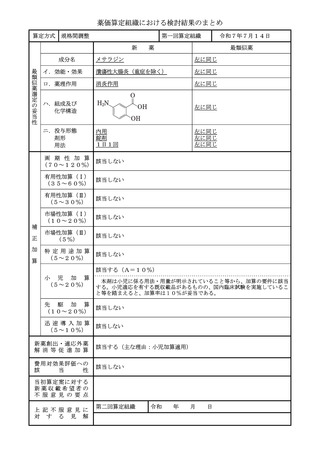
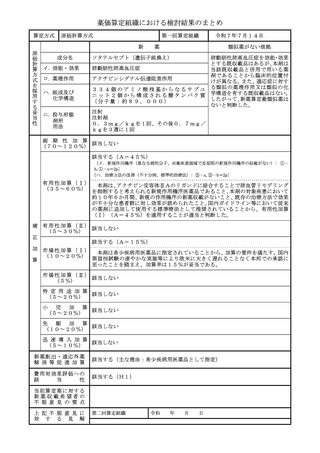
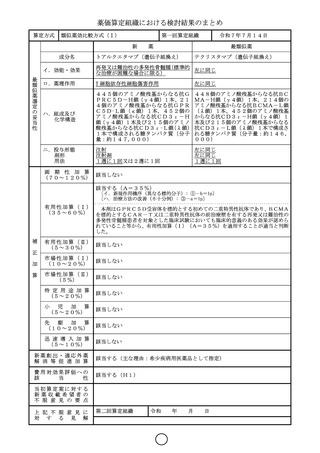
算定方式
原価計算方式
第一回算定組織
新
原
価
計
算
方
式
を
採
用
す
る
妥
当
性
成分名
イ.効能・効果
ロ.薬理作用
令和7年7月14日
薬
類似薬がない根拠
ベルズチファン
本剤の主たる効能又は効果であ
る「フォン・ヒッペル・リンドウ
①フォン・ヒッペル・リンドウ病関連腫瘍
病関連腫瘍」を適応に有する既収
②がん化学療法後に増悪した根治切除不能又は 載品はなく、同様の薬理作用、組
転移性の腎細胞癌
成及び化学構造等を持つ既収載
品もないことから、新薬算定最類
低酸素誘導因子2α(HIF-2α)阻害作用
似薬はないと判断した。
ハ.組成及び
化学構造
ニ.投与形態
剤形
用法
内用
錠剤
1日1回
該当する(A=75%)
画 期 性 加 算
(70~120%)
〔イ.新規作用機序(異なる標的分子、重篤な疾病を対象): ①-b,①-c=2p〕
〔ロ.高い有効性・安全性(有効性、ランダム化比較試験以外): ②-1-a,②-2-b=1p〕
〔ハ.治療方法の改善(標準的治療法): ③-b=1p〕
本剤はHIF-2α阻害作用を有する新規作用機序医薬品であり、臨床試験成績
から臨床上の有用性が示されていること、フォン・ヒッペル・リンドウ病関連腫瘍
の適応症で初めて承認された薬剤であり、初めて全身治療を提供するものであるこ
と等から、画期性加算(A=75%)を適用することが適当と判断した。
有用性加算(Ⅰ)
該当しない
(35~60%)
補
有用性加算(Ⅱ)
該当しない
(5~30%)
該当する(A=15%)
正
市 場 性 加 算 ( Ⅰ ) 本剤は希少疾病用医薬品に指定されていることから、加算の要件を満たす。患者
(10~20%) 数が極めて少なく開発が難しいと想定される中で、フォン・ヒッペル・リンドウ病
関連腫瘍の適応症で初めて承認された薬剤であること等を踏まえ、加算率15%が
妥当である。
算
加
市場性加算(Ⅱ)
該当しない
(5%)
特 定 用 途 加 算
該当しない
(5~20%)
小
児 加 算
該当しない
(5~20%)
先 駆 加 算
該当しない
(10~20%)
迅 速 導 入 加 算
該当しない
(5~10%)
新薬創出・適応外薬
解 消 等 促 進 加 算
該当する(主な理由:希少疾病用医薬品として指定)
費用対効果評価への
該
当
性
該当する(H1)
当初算定案に対する
新薬収載希望者の
不 服 意 見 の 要 点
上 記 不 服 意 見 に
対 す る 見 解
第二回算定組織
令和
7
年
月
日