よむ、つかう、まなぶ。
【資料4】モルヌピラビル(ラゲブリオカプセル200mg )の安全性について(医薬・生活衛生局の説明資料) (9 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_24538.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第7回 3/18)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
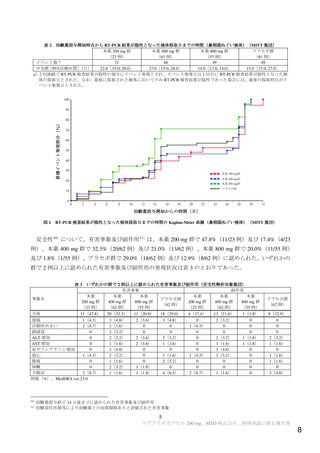
死亡に至った有害事象は、認められなかった。
重篤な有害事象は、本薬 400 mg 群 2 例(酸素飽和度低下及び脳血管発作各 1 例)、本薬 800 mg 群 1
例(急性呼吸不全)、プラセボ群 1 例(低酸素症)に認められ、いずれも治験薬との因果関係は否定さ
れた。
投与中止に至った有害事象は、本薬 400 mg 群 1 例(酸素飽和度低下)、本薬 800 mg 群 1 例(急性呼
吸不全)、プラセボ群 1 例(低酸素症)に認められ、いずれも治験薬との因果関係が否定された。
2.2
2.2.1
国際共同第Ⅱ/Ⅲ相試験(MK-4482-002 試験<2020 年 10 月~継続中>)
第Ⅱ相パート(2021 年 3 月データカットオフ)
18 歳以上の SARS-CoV-2 による感染症患者[目標例数 300 例(各群 75 例)12)]を対象に、本薬の有
効性及び安全性を検討することを目的として、プラセボ対照無作為化二重盲検並行群間比較試験が、米
国、ロシア、コロンビア等の 12 カ国 82 施設で実施された。本試験の主な選択・除外基準は表 4 のとお
りであった。
12)
各群の被験者数が 60 例のとき、ウイルス量のベースラインからの変化量(log10 copies/mL)について、各本薬群とプラセボ群の群間
の差を-0.75~-1.25、各投与群の標準偏差を 1.25~1.75 と設定した場合、有意水準片側 2.5%の下、検出力は 64%~99%超となる。
6
ラゲブリオカプセル 200 mg_MSD 株式会社_特例承認に係る報告書
9
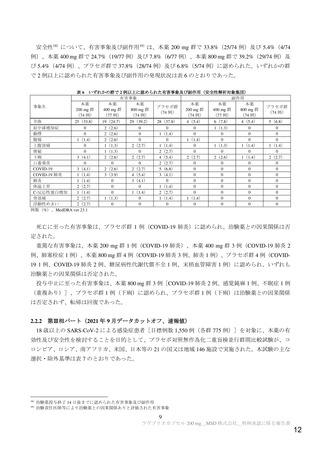
重篤な有害事象は、本薬 400 mg 群 2 例(酸素飽和度低下及び脳血管発作各 1 例)、本薬 800 mg 群 1
例(急性呼吸不全)、プラセボ群 1 例(低酸素症)に認められ、いずれも治験薬との因果関係は否定さ
れた。
投与中止に至った有害事象は、本薬 400 mg 群 1 例(酸素飽和度低下)、本薬 800 mg 群 1 例(急性呼
吸不全)、プラセボ群 1 例(低酸素症)に認められ、いずれも治験薬との因果関係が否定された。
2.2
2.2.1
国際共同第Ⅱ/Ⅲ相試験(MK-4482-002 試験<2020 年 10 月~継続中>)
第Ⅱ相パート(2021 年 3 月データカットオフ)
18 歳以上の SARS-CoV-2 による感染症患者[目標例数 300 例(各群 75 例)12)]を対象に、本薬の有
効性及び安全性を検討することを目的として、プラセボ対照無作為化二重盲検並行群間比較試験が、米
国、ロシア、コロンビア等の 12 カ国 82 施設で実施された。本試験の主な選択・除外基準は表 4 のとお
りであった。
12)
各群の被験者数が 60 例のとき、ウイルス量のベースラインからの変化量(log10 copies/mL)について、各本薬群とプラセボ群の群間
の差を-0.75~-1.25、各投与群の標準偏差を 1.25~1.75 と設定した場合、有意水準片側 2.5%の下、検出力は 64%~99%超となる。
6
ラゲブリオカプセル 200 mg_MSD 株式会社_特例承認に係る報告書
9