よむ、つかう、まなぶ。
03資料1-1 小児におけるRSウイルス感染症の予防について (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_70339.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会(第64回 2/12)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
母子免疫ワクチンの定期接種化に伴う
副反応に係る取扱いについて
第110回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、
令和7年度第11回薬事審議会医薬品等安全対策部会安全対策調査会(合同開催)
2026(令和8)年2月4日
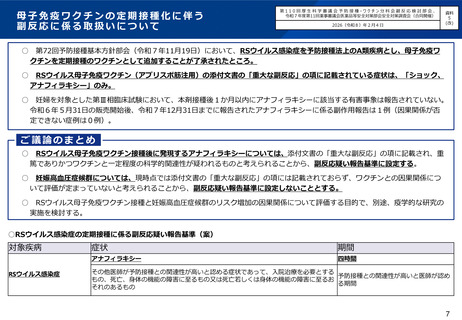
○
第72回予防接種基本方針部会(令和7年11月19日)において、RSウイルス感染症を予防接種法上のA類疾病とし、母子免疫ワ
クチンを定期接種のワクチンとして追加することが了承されたところ。
○
RSウイルス母子免疫ワクチン(アブリスボ筋注用)の添付文書の「重大な副反応」の項に記載されている症状は、「ショック、
アナフィラキシー」のみ。
資料
5
(改)
○ 妊婦を対象とした第Ⅲ相臨床試験において、本剤接種後1か月以内にアナフィラキシーに該当する有害事象は報告されていない。
令和6年5月31日の販売開始後、令和7年12月31日までに報告されたアナフィラキシーに係る副作用報告は1例(因果関係が否
定できない症例は0例)。
ご議論のまとめ
○
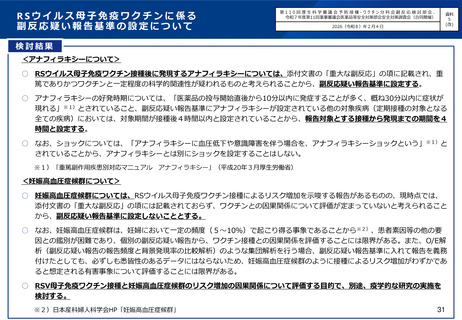
RSウイルス母子免疫ワクチン接種後に発現するアナフィラキシーについては、添付文書の「重大な副反応」の項に記載され、重
篤でありかつワクチンと一定程度の科学的関連性が疑われるものと考えられることから、副反応疑い報告基準に設定する。
○
妊娠高血圧症候群については、現時点では添付文書の「重大な副反応」の項には記載されておらず、ワクチンとの因果関係につ
いて評価が定まっていないと考えられることから、副反応疑い報告基準に設定しないこととする。
○ RSウイルス母子免疫ワクチン接種と妊娠高血圧症候群のリスク増加の因果関係について評価する目的で、別途、疫学的な研究の
実施を検討する。
○RSウイルス感染症の定期接種に係る副反応疑い報告基準(案)
対象疾病
RSウイルス感染症
症状
期間
アナフィラキシー
四時間
その他医師が予防接種との関連性が高いと認める症状であって、入院治療を必要とする
予防接種との関連性が高いと医師が認め
もの、死亡、身体の機能の障害に至るもの又は死亡若しくは身体の機能の障害に至るお
る期間
それのあるもの
7
副反応に係る取扱いについて
第110回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、
令和7年度第11回薬事審議会医薬品等安全対策部会安全対策調査会(合同開催)
2026(令和8)年2月4日
○
第72回予防接種基本方針部会(令和7年11月19日)において、RSウイルス感染症を予防接種法上のA類疾病とし、母子免疫ワ
クチンを定期接種のワクチンとして追加することが了承されたところ。
○
RSウイルス母子免疫ワクチン(アブリスボ筋注用)の添付文書の「重大な副反応」の項に記載されている症状は、「ショック、
アナフィラキシー」のみ。
資料
5
(改)
○ 妊婦を対象とした第Ⅲ相臨床試験において、本剤接種後1か月以内にアナフィラキシーに該当する有害事象は報告されていない。
令和6年5月31日の販売開始後、令和7年12月31日までに報告されたアナフィラキシーに係る副作用報告は1例(因果関係が否
定できない症例は0例)。
ご議論のまとめ
○
RSウイルス母子免疫ワクチン接種後に発現するアナフィラキシーについては、添付文書の「重大な副反応」の項に記載され、重
篤でありかつワクチンと一定程度の科学的関連性が疑われるものと考えられることから、副反応疑い報告基準に設定する。
○
妊娠高血圧症候群については、現時点では添付文書の「重大な副反応」の項には記載されておらず、ワクチンとの因果関係につ
いて評価が定まっていないと考えられることから、副反応疑い報告基準に設定しないこととする。
○ RSウイルス母子免疫ワクチン接種と妊娠高血圧症候群のリスク増加の因果関係について評価する目的で、別途、疫学的な研究の
実施を検討する。
○RSウイルス感染症の定期接種に係る副反応疑い報告基準(案)
対象疾病
RSウイルス感染症
症状
期間
アナフィラキシー
四時間
その他医師が予防接種との関連性が高いと認める症状であって、入院治療を必要とする
予防接種との関連性が高いと医師が認め
もの、死亡、身体の機能の障害に至るもの又は死亡若しくは身体の機能の障害に至るお
る期間
それのあるもの
7