よむ、つかう、まなぶ。
03資料1-1 小児におけるRSウイルス感染症の予防について (31 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_70339.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会(第64回 2/12)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
RSウイルス母子免疫ワクチンに係る
副反応疑い報告基準の設定について
第110回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、
令和7年度第11回薬事審議会医薬品等安全対策部会安全対策調査会(合同開催)
資料
5
(改)
2026(令和8)年2月4日
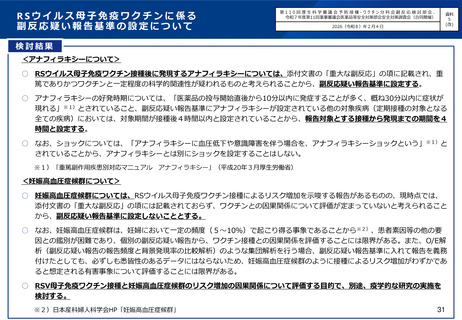
検討結果
<アナフィラキシーについて>
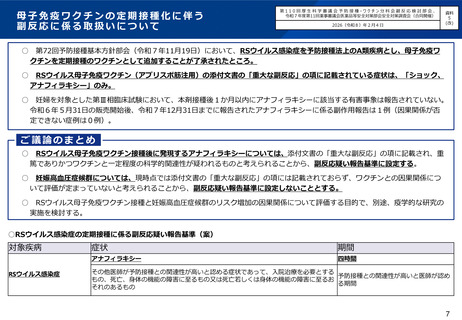
○ RSウイルス母子免疫ワクチン接種後に発現するアナフィラキシーについては、添付文書の「重大な副反応」の項に記載され、重
篤でありかつワクチンと一定程度の科学的関連性が疑われるものと考えられることから、副反応疑い報告基準に設定する。
○ アナフィラキシーの好発時期については、「医薬品の投与開始直後から10分以内に発症することが多く、概ね30分以内に症状が
現れる」※1)とされていること、副反応疑い報告基準にアナフィラキシーが設定されている他の対象疾病(定期接種の対象となる
全ての疾病)においては、対象期間が接種後4時間以内と設定されていることから、報告対象とする接種から発現までの期間を4
時間と設定する。
○ なお、ショックについては、「アナフィラキシーに血圧低下や意識障害を伴う場合を、アナフィラキシーショックという」※1)と
されていることから、アナフィラキシーとは別にショックを設定することはしない。
※1)「重篤副作用疾患別対応マニュアル アナフィラキシー」(平成20年3月厚生労働省)
<妊娠高血圧症候群について>
○ 妊娠高血圧症候群については、RSウイルス母子免疫ワクチン接種によるリスク増加を示唆する報告があるものの、現時点では、
添付文書の「重大な副反応」の項には記載されておらず、ワクチンとの因果関係について評価が定まっていないと考えられること
から、副反応疑い報告基準に設定しないこととする。
○ なお、妊娠高血圧症候群は、妊婦において一定の頻度(5~10%)で起こり得る事象であることから※2)、患者素因等の他の要
因との鑑別が困難であり、個別の副反応疑い報告から、ワクチン接種との因果関係を評価することには限界がある。また、O/E解
析(副反応疑い報告の報告頻度と背景発現率の比較解析)のような集団解析を行う場合、副反応疑い報告基準に入れて報告を義務
付けたとしても、必ずしも悉皆性のあるデータにはならないため、妊娠高血圧症候群のように接種によるリスク増加がわずかであ
ると想定される有害事象について評価することには限界がある。
○ RSV母子免疫ワクチン接種と妊娠高血圧症候群のリスク増加の因果関係について評価する目的で、別途、疫学的な研究の実施を
検討する。
※2)日本産科婦人科学会HP「妊娠高血圧症候群」
31
副反応疑い報告基準の設定について
第110回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、
令和7年度第11回薬事審議会医薬品等安全対策部会安全対策調査会(合同開催)
資料
5
(改)
2026(令和8)年2月4日
検討結果
<アナフィラキシーについて>
○ RSウイルス母子免疫ワクチン接種後に発現するアナフィラキシーについては、添付文書の「重大な副反応」の項に記載され、重
篤でありかつワクチンと一定程度の科学的関連性が疑われるものと考えられることから、副反応疑い報告基準に設定する。
○ アナフィラキシーの好発時期については、「医薬品の投与開始直後から10分以内に発症することが多く、概ね30分以内に症状が
現れる」※1)とされていること、副反応疑い報告基準にアナフィラキシーが設定されている他の対象疾病(定期接種の対象となる
全ての疾病)においては、対象期間が接種後4時間以内と設定されていることから、報告対象とする接種から発現までの期間を4
時間と設定する。
○ なお、ショックについては、「アナフィラキシーに血圧低下や意識障害を伴う場合を、アナフィラキシーショックという」※1)と
されていることから、アナフィラキシーとは別にショックを設定することはしない。
※1)「重篤副作用疾患別対応マニュアル アナフィラキシー」(平成20年3月厚生労働省)
<妊娠高血圧症候群について>
○ 妊娠高血圧症候群については、RSウイルス母子免疫ワクチン接種によるリスク増加を示唆する報告があるものの、現時点では、
添付文書の「重大な副反応」の項には記載されておらず、ワクチンとの因果関係について評価が定まっていないと考えられること
から、副反応疑い報告基準に設定しないこととする。
○ なお、妊娠高血圧症候群は、妊婦において一定の頻度(5~10%)で起こり得る事象であることから※2)、患者素因等の他の要
因との鑑別が困難であり、個別の副反応疑い報告から、ワクチン接種との因果関係を評価することには限界がある。また、O/E解
析(副反応疑い報告の報告頻度と背景発現率の比較解析)のような集団解析を行う場合、副反応疑い報告基準に入れて報告を義務
付けたとしても、必ずしも悉皆性のあるデータにはならないため、妊娠高血圧症候群のように接種によるリスク増加がわずかであ
ると想定される有害事象について評価することには限界がある。
○ RSV母子免疫ワクチン接種と妊娠高血圧症候群のリスク増加の因果関係について評価する目的で、別途、疫学的な研究の実施を
検討する。
※2)日本産科婦人科学会HP「妊娠高血圧症候群」
31