よむ、つかう、まなぶ。
参考資料4-4 特例承認医薬品の市販直後調査報告書 (62 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29975.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和4年度第22回 12/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
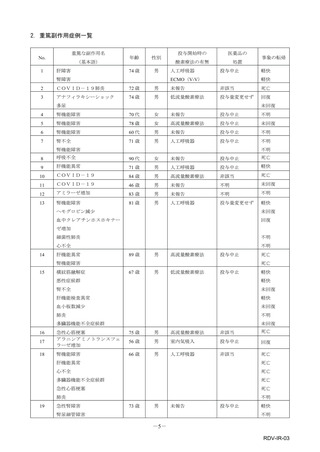
1. 推定患者数
本報告書の集計対象期間中(2022 年 9 ⽉ 1 ⽇〜2022 年 11 ⽉ 23 ⽇)にエバシェルド筋注セットの投与
患者は、7136 ⼈でした(投与予定を含む)。
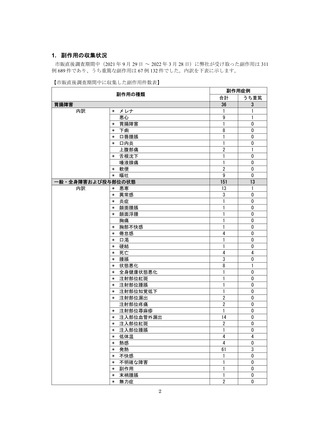
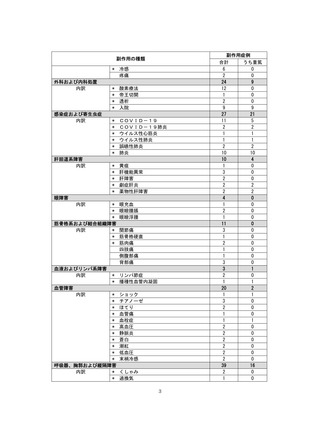
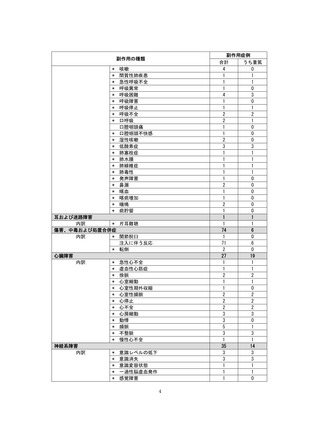
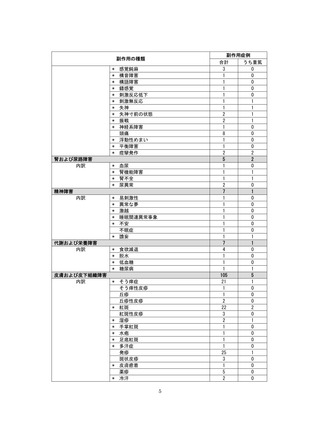
2. 収集された副作⽤
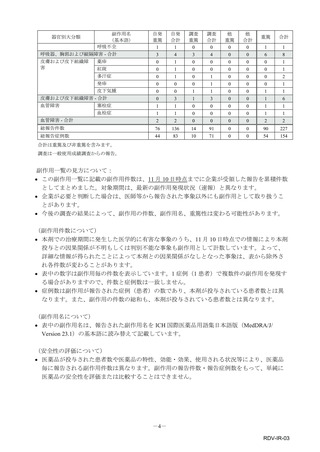
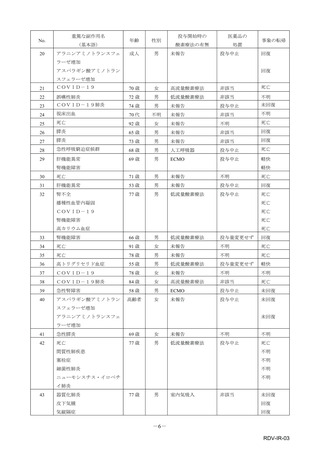
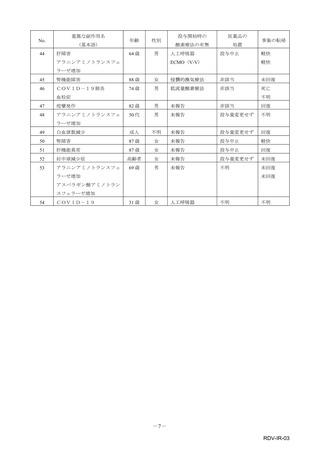
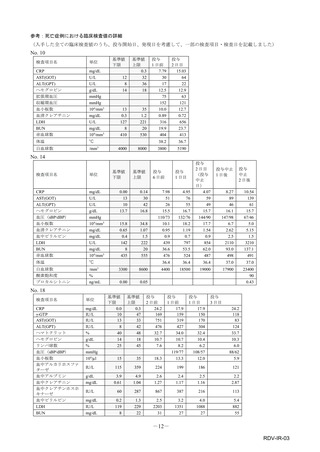
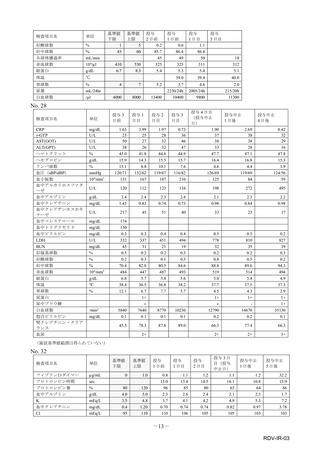
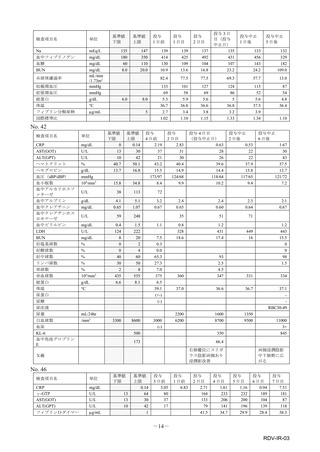
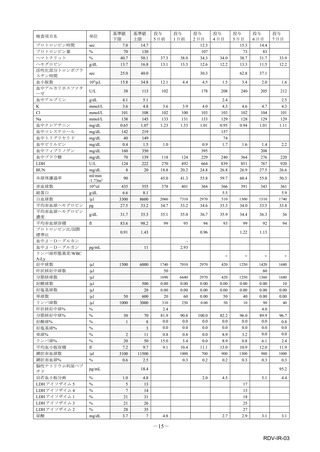
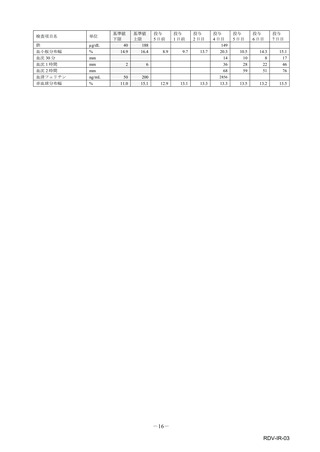
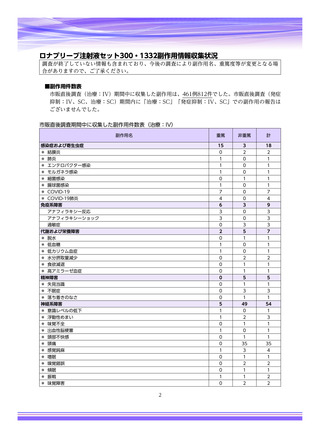
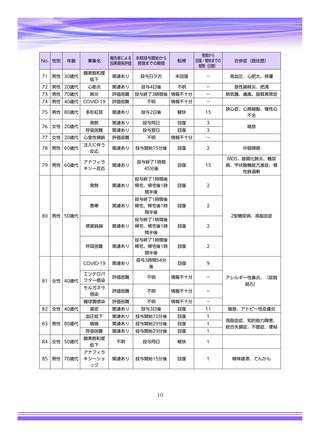
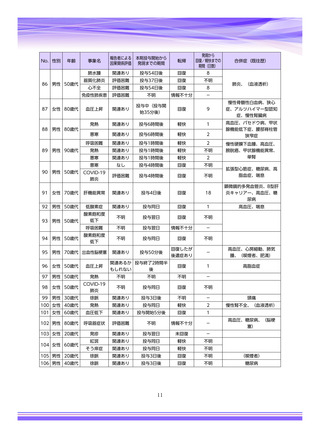
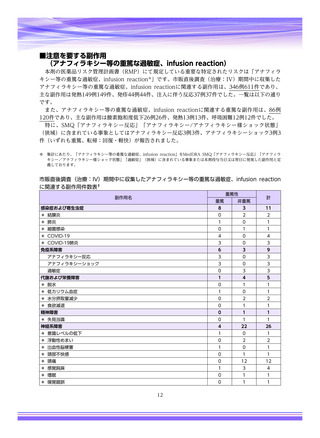
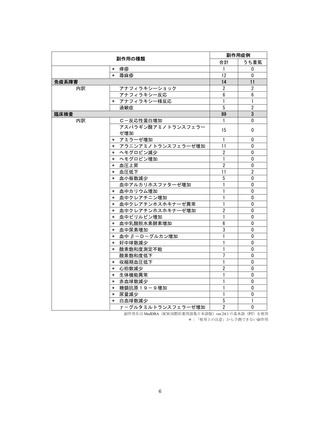
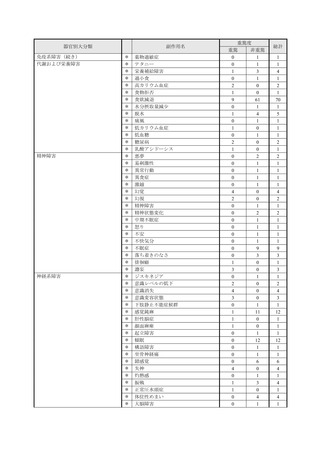
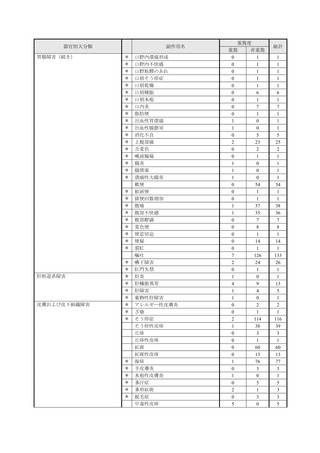
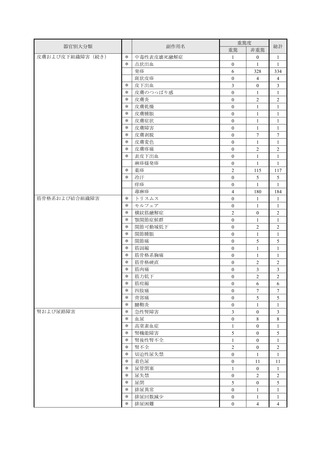
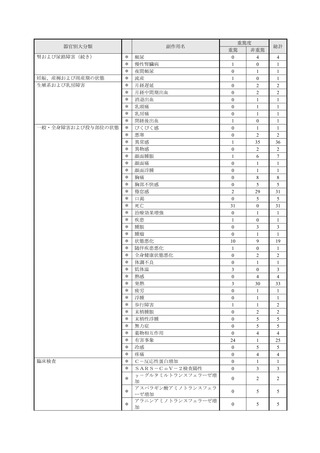
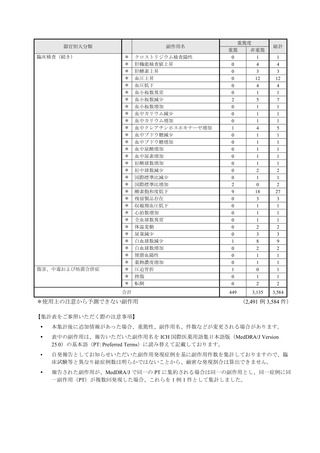
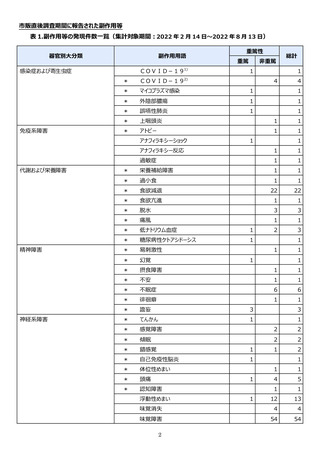
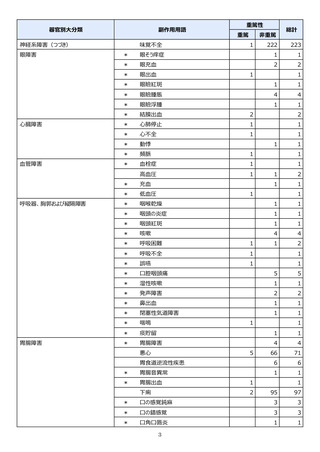
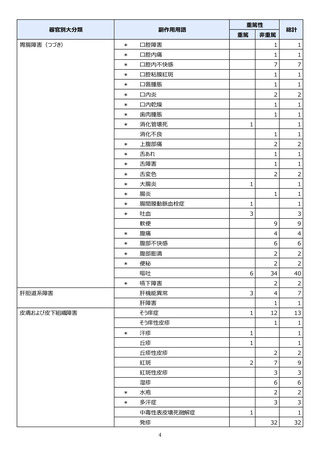
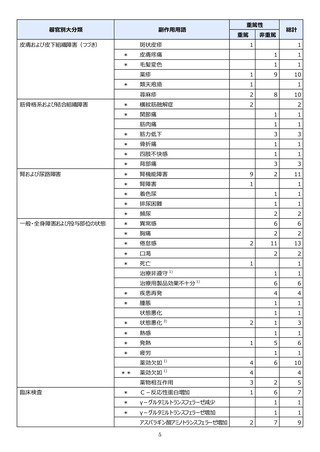
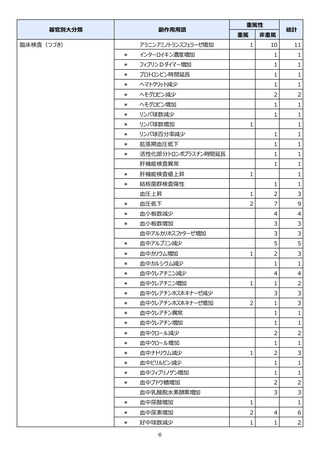
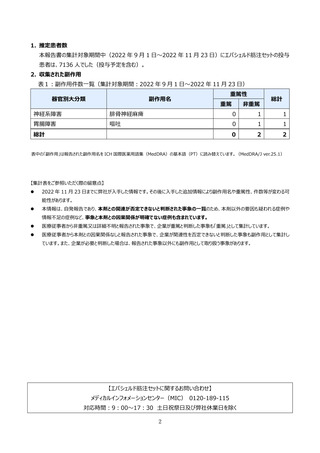
表1︓副作⽤件数⼀覧(集計対象期間︓2022 年 9 ⽉ 1 ⽇〜2022 年 11 ⽉ 23 ⽇)
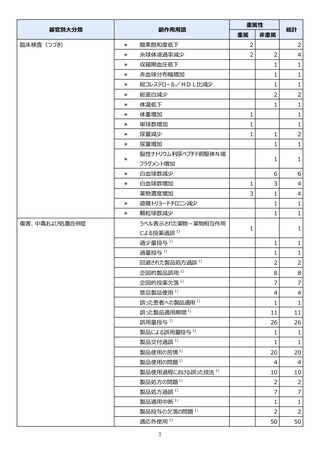
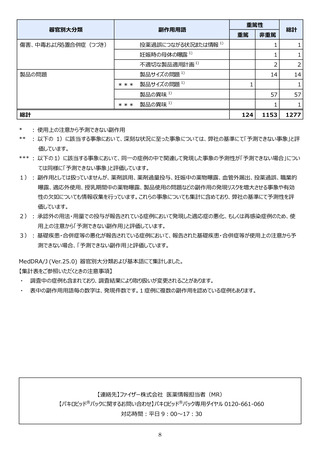
器官別⼤分類
副作⽤名
重篤性
重篤
⾮重篤
総計
神経系障害
腓⾻神経⿇痺
0
1
1
胃腸障害
嘔吐
0
1
1
0
2
2
総計
表中の「副作⽤」は報告された副作⽤名を ICH 国際医薬⽤語集(MedDRA)の基本語(PT)に読み替えています。(MedDRA/J ver.25.1)
【集計表をご参照いただく際の留意点】
2022 年 11 ⽉ 23 ⽇までに弊社が⼊⼿した情報です。その後に⼊⼿した追加情報により副作⽤名や重篤性、件数等が変わる可
能性があります。
本情報は、⾃発報告であり、本剤との関連が否定できないと判断された事象の⼀覧のため、本剤以外の要因も疑われる症例や
情報不⾜の症例など、事象と本剤との因果関係が明確でない症例も含まれています。
医療従事者から⾮重篤⼜は詳細不明と報告された事象で、企業が重篤と判断した事象も「重篤」として集計しています。
医療従事者から本剤との因果関係なしと報告された事象で、企業が関連性を否定できないと判断した事象も副作⽤として集計し
ています。また、企業が必要と判断した場合は、報告された事象以外にも副作⽤として取り扱う事象があります。
【エバシェルド筋注セットに関するお問い合わせ】
メディカルインフォメーションセンター(MIC) 0120-189-115
対応時間︓9︓00〜17︓30 ⼟⽇祝祭⽇及び弊社休業⽇を除く
2
本報告書の集計対象期間中(2022 年 9 ⽉ 1 ⽇〜2022 年 11 ⽉ 23 ⽇)にエバシェルド筋注セットの投与
患者は、7136 ⼈でした(投与予定を含む)。
2. 収集された副作⽤
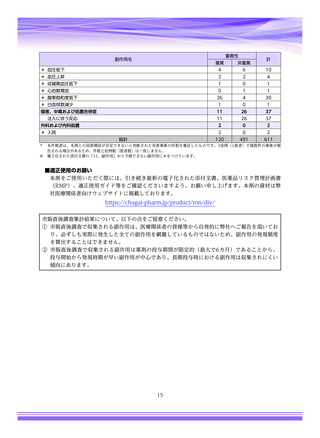
表1︓副作⽤件数⼀覧(集計対象期間︓2022 年 9 ⽉ 1 ⽇〜2022 年 11 ⽉ 23 ⽇)
器官別⼤分類
副作⽤名
重篤性
重篤
⾮重篤
総計
神経系障害
腓⾻神経⿇痺
0
1
1
胃腸障害
嘔吐
0
1
1
0
2
2
総計
表中の「副作⽤」は報告された副作⽤名を ICH 国際医薬⽤語集(MedDRA)の基本語(PT)に読み替えています。(MedDRA/J ver.25.1)
【集計表をご参照いただく際の留意点】
2022 年 11 ⽉ 23 ⽇までに弊社が⼊⼿した情報です。その後に⼊⼿した追加情報により副作⽤名や重篤性、件数等が変わる可
能性があります。
本情報は、⾃発報告であり、本剤との関連が否定できないと判断された事象の⼀覧のため、本剤以外の要因も疑われる症例や
情報不⾜の症例など、事象と本剤との因果関係が明確でない症例も含まれています。
医療従事者から⾮重篤⼜は詳細不明と報告された事象で、企業が重篤と判断した事象も「重篤」として集計しています。
医療従事者から本剤との因果関係なしと報告された事象で、企業が関連性を否定できないと判断した事象も副作⽤として集計し
ています。また、企業が必要と判断した場合は、報告された事象以外にも副作⽤として取り扱う事象があります。
【エバシェルド筋注セットに関するお問い合わせ】
メディカルインフォメーションセンター(MIC) 0120-189-115
対応時間︓9︓00〜17︓30 ⼟⽇祝祭⽇及び弊社休業⽇を除く
2