よむ、つかう、まなぶ。
参考資料4-4 特例承認医薬品の市販直後調査報告書 (30 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29975.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会安全対策調査会(令和4年度第22回 12/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
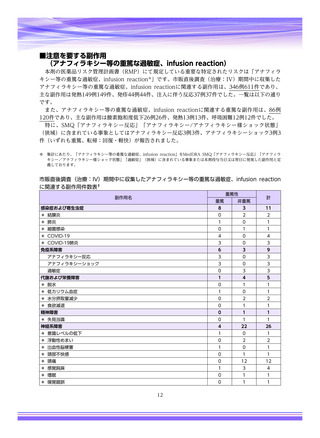
■注意を要する副作用
(アナフィラキシー等の重篤な過敏症、infusion reaction)
本剤の医薬品リスク管理計画書(RMP)にて規定している重要な特定されたリスクは「アナフィラ
キシー等の重篤な過敏症、infusion reaction※」です。市販直後調査(治療:IV)期間中に収集した
アナフィラキシー等の重篤な過敏症、infusion reactionに関連する副作用は、346例611件であり、
主な副作用は発熱149例149件、発疹44例44件、注入に伴う反応37例37件でした。一覧は以下の通り
です。
また、アナフィラキシー等の重篤な過敏症、infusion reactionに関連する重篤な副作用は、86例
120件であり、主な副作用は酸素飽和度低下26例26件、発熱13例13件、呼吸困難12例12件でした。
特に、SMQ「アナフィラキシー反応」「アナフィラキシー/アナフィラキシー様ショック状態」
(狭域)に含まれている事象としてはアナフィラキシー反応3例3件、アナフィラキシーショック3例3
件(いずれも重篤、転帰:回復・軽快)が報告されました。
※ 集計にあたり、「アナフィラキシー等の重篤な過敏症、infusion reaction」をMedDRA SMQ「アナフィラキシー反応」「アナフィラ
キシー/アナフィラキシー様ショック状態」「過敏症」(狭域)に含まれている事象または本剤投与当日又は翌日に発現した副作用と定
義しております。
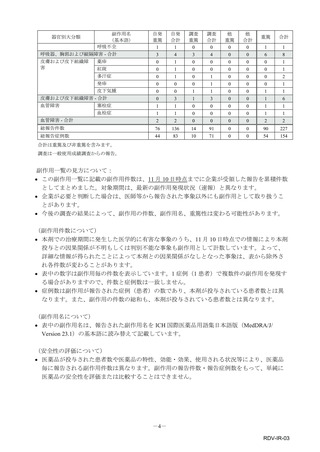
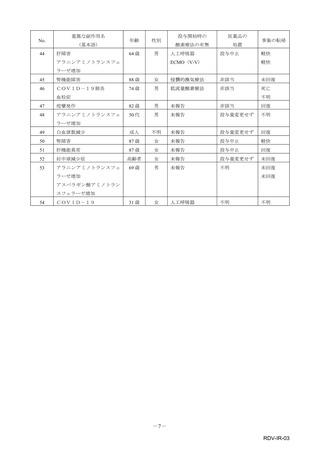
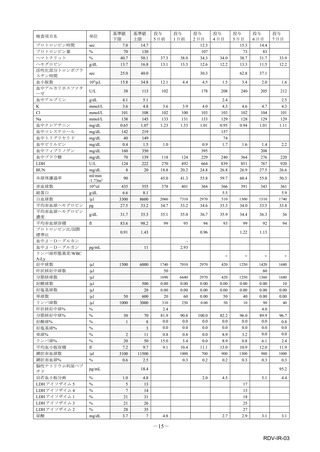
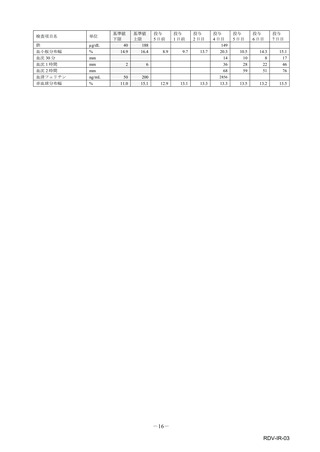
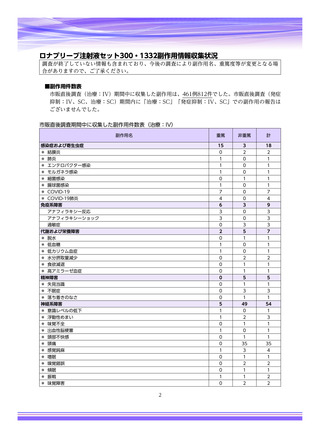
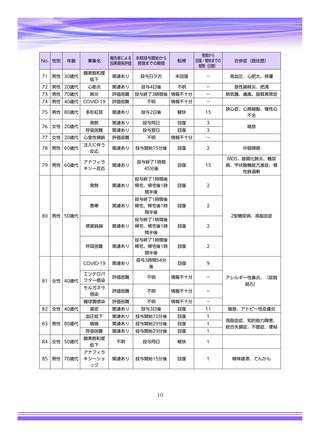
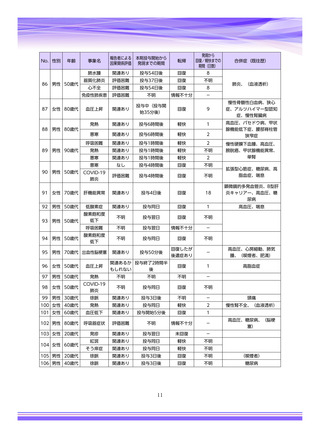
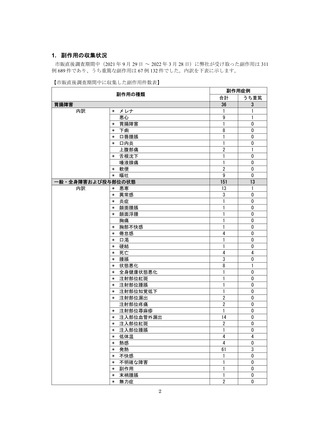
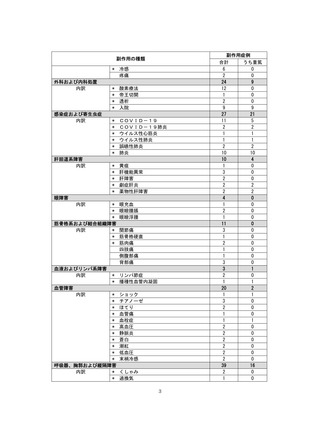
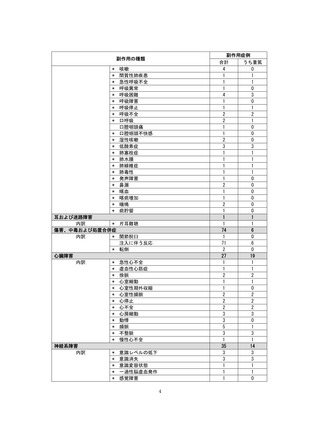
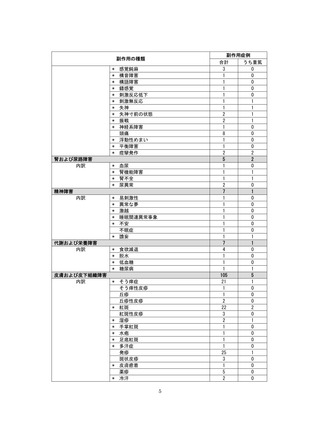
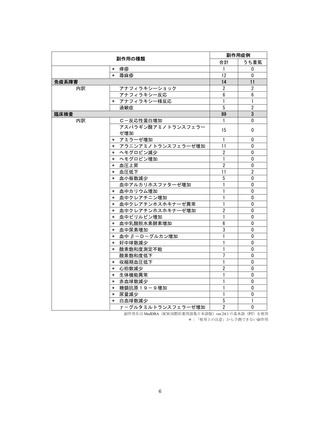
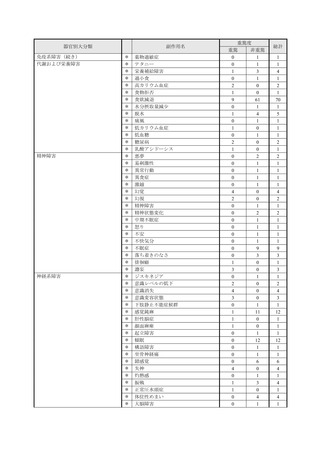
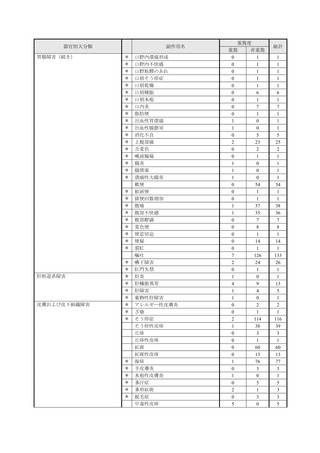
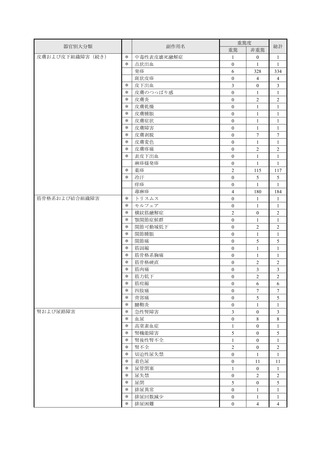
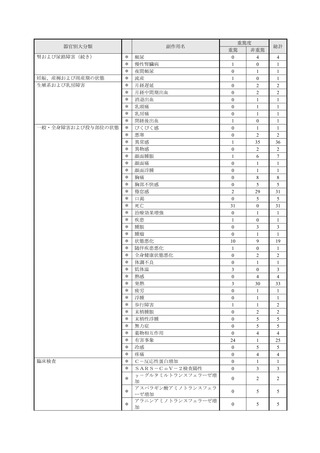
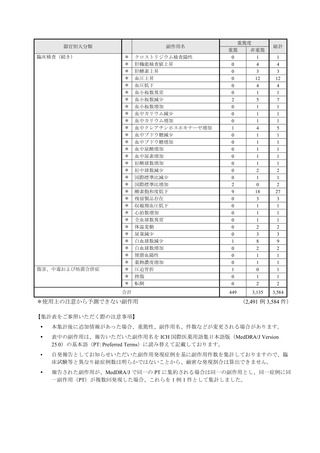
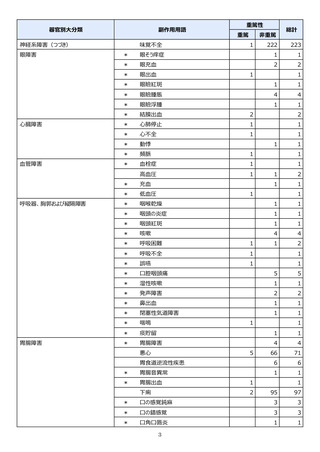
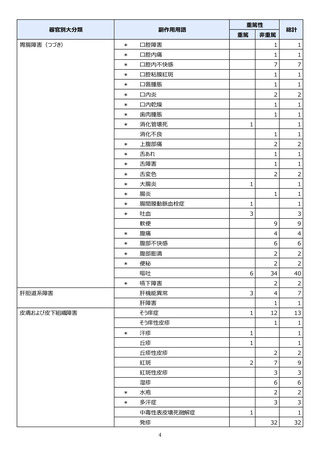
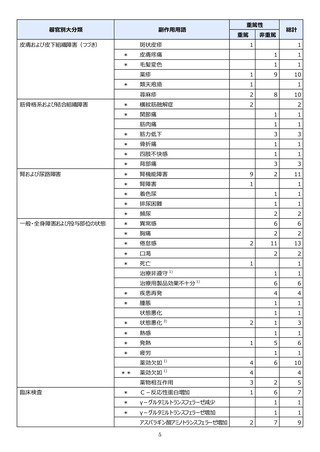
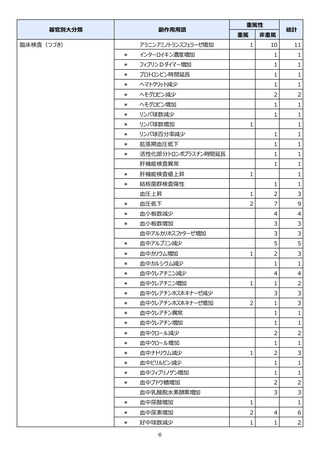
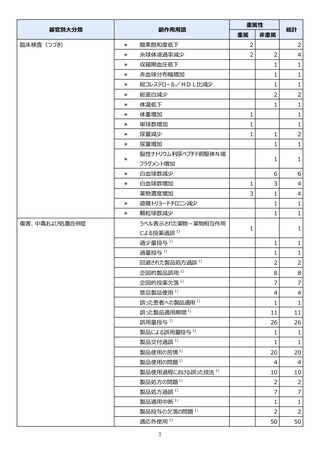
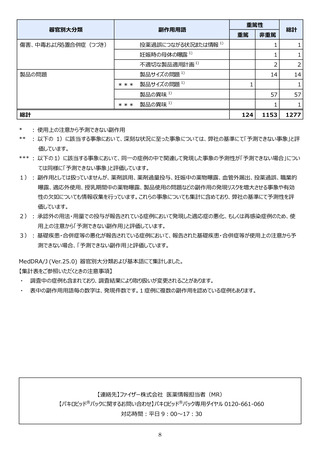
市販直後調査(治療:IV)期間中に収集したアナフィラキシー等の重篤な過敏症、infusion reaction
に関連する副作用件数表†
重篤性
副作用名
計
重篤
非重篤
感染症および寄生虫症
8
3
11
* 結膜炎
0
2
2
* 肺炎
1
0
1
* 細菌感染
0
1
1
* COVID-19
4
0
4
* COVID-19肺炎
3
0
3
免疫系障害
6
3
9
アナフィラキシー反応
3
0
3
アナフィラキシーショック
3
0
3
過敏症
0
3
3
代謝および栄養障害
1
4
5
* 脱水
0
1
1
* 低カリウム血症
1
0
1
* 水分摂取量減少
0
2
2
* 食欲減退
0
1
1
精神障害
0
1
1
* 失見当識
0
1
1
神経系障害
4
22
26
* 意識レベルの低下
1
0
1
* 浮動性めまい
0
2
2
* 出血性脳梗塞
1
0
1
* 頭部不快感
0
1
1
* 頭痛
0
12
12
* 感覚鈍麻
1
3
4
* 嗜眠
0
1
1
* 嗅覚錯誤
0
1
1
12
(アナフィラキシー等の重篤な過敏症、infusion reaction)
本剤の医薬品リスク管理計画書(RMP)にて規定している重要な特定されたリスクは「アナフィラ
キシー等の重篤な過敏症、infusion reaction※」です。市販直後調査(治療:IV)期間中に収集した
アナフィラキシー等の重篤な過敏症、infusion reactionに関連する副作用は、346例611件であり、
主な副作用は発熱149例149件、発疹44例44件、注入に伴う反応37例37件でした。一覧は以下の通り
です。
また、アナフィラキシー等の重篤な過敏症、infusion reactionに関連する重篤な副作用は、86例
120件であり、主な副作用は酸素飽和度低下26例26件、発熱13例13件、呼吸困難12例12件でした。
特に、SMQ「アナフィラキシー反応」「アナフィラキシー/アナフィラキシー様ショック状態」
(狭域)に含まれている事象としてはアナフィラキシー反応3例3件、アナフィラキシーショック3例3
件(いずれも重篤、転帰:回復・軽快)が報告されました。
※ 集計にあたり、「アナフィラキシー等の重篤な過敏症、infusion reaction」をMedDRA SMQ「アナフィラキシー反応」「アナフィラ
キシー/アナフィラキシー様ショック状態」「過敏症」(狭域)に含まれている事象または本剤投与当日又は翌日に発現した副作用と定
義しております。
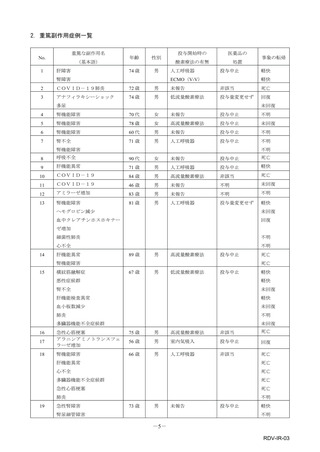
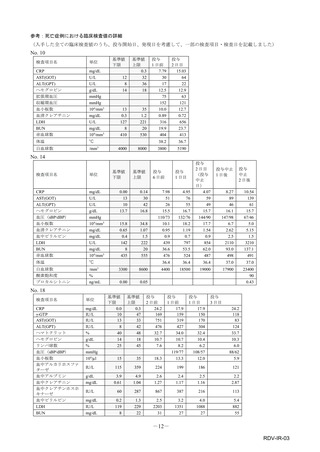
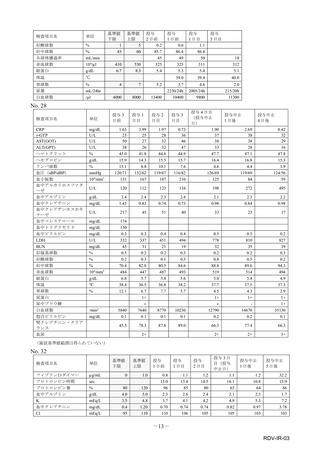
市販直後調査(治療:IV)期間中に収集したアナフィラキシー等の重篤な過敏症、infusion reaction
に関連する副作用件数表†
重篤性
副作用名
計
重篤
非重篤
感染症および寄生虫症
8
3
11
* 結膜炎
0
2
2
* 肺炎
1
0
1
* 細菌感染
0
1
1
* COVID-19
4
0
4
* COVID-19肺炎
3
0
3
免疫系障害
6
3
9
アナフィラキシー反応
3
0
3
アナフィラキシーショック
3
0
3
過敏症
0
3
3
代謝および栄養障害
1
4
5
* 脱水
0
1
1
* 低カリウム血症
1
0
1
* 水分摂取量減少
0
2
2
* 食欲減退
0
1
1
精神障害
0
1
1
* 失見当識
0
1
1
神経系障害
4
22
26
* 意識レベルの低下
1
0
1
* 浮動性めまい
0
2
2
* 出血性脳梗塞
1
0
1
* 頭部不快感
0
1
1
* 頭痛
0
12
12
* 感覚鈍麻
1
3
4
* 嗜眠
0
1
1
* 嗅覚錯誤
0
1
1
12