よむ、つかう、まなぶ。
【資料No.1】★審査報告書(3) (14 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_29325.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会(令和4年度第5回 11/22)、医薬品第二部会(令和4年度第13回 11/22)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
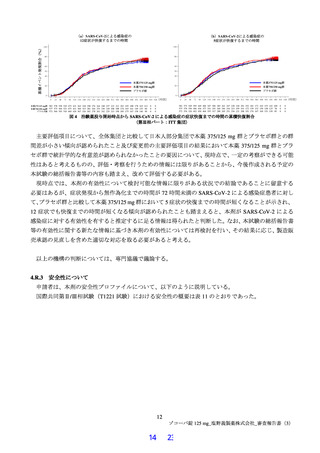
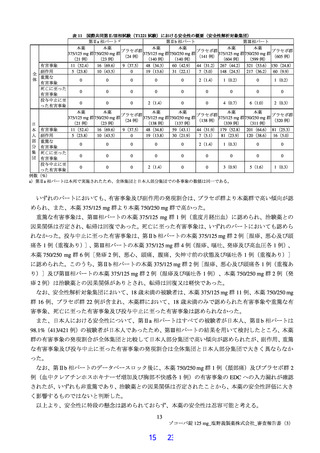
図 4 治験薬投与開始時点から SARS-CoV-2 による感染症の症状快復までの時間の累積快復割合
(第Ⅲ相パート:ITT 集団)
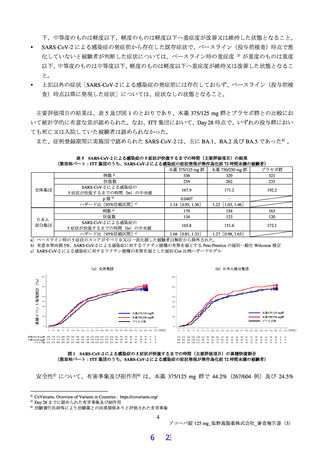
主要評価項目について、全体集団と比較して日本人部分集団で本薬 375/125 mg 群とプラセボ群との群
間差が小さい傾向が認められたこと及び変更前の主要評価項目の結果において本薬 375/125 mg 群とプラ
セボ群で統計学的な有意差が認められなかったことの要因について、現時点で、一定の考察ができる可能
性はあると考えるものの、評価・考察を行うための情報には限りがあることから、今後作成される予定の
本試験の総括報告書等の内容も踏まえ、改めて評価する必要がある。
現時点では、本剤の有効性について検討可能な情報に限りがある状況での結論であることに留意する
必要はあるが、症状発現から無作為化までの時間が 72 時間未満の SARS-CoV-2 による感染症患者に対し
て、プラセボ群と比較して本薬 375/125 mg 群において 5 症状の快復までの時間が短くなることが示され、
12 症状でも快復までの時間が短くなる傾向が認められたことも踏まえると、本剤が SARS-CoV-2 による
感染症に対する有効性を有すると推定するに足る情報は得られたと判断した。なお、本試験の総括報告書
等の有効性に関する新たな情報に基づき本剤の有効性については再検討を行い、その結果に応じ、製造販
売承認の見直しを含めた適切な対応を取る必要があると考える。
以上の機構の判断については、専門協議で議論する。
4.R.3 安全性について
申請者は、本剤の安全性プロファイルについて、以下のように説明している。
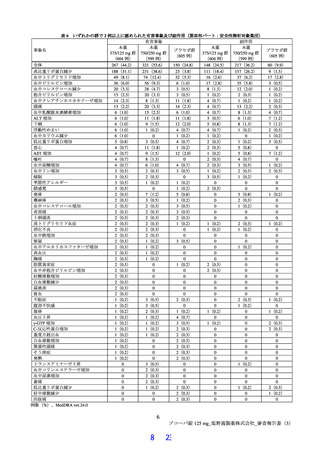
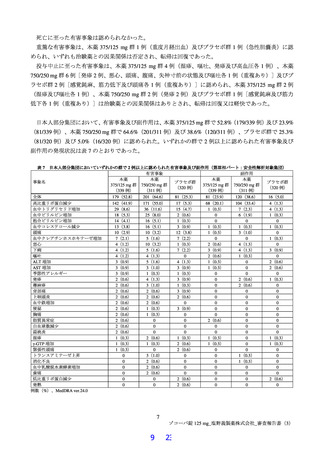
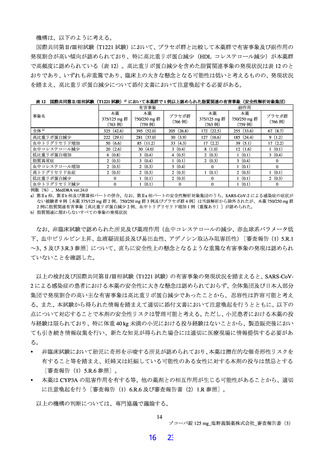
国際共同第Ⅱ/Ⅲ相試験(T1221 試験)における安全性の概要は表 11 のとおりであった。
12
ゾコーバ錠 125 mg_塩野義製薬株式会社_審査報告書(3)
14 / 23
(第Ⅲ相パート:ITT 集団)
主要評価項目について、全体集団と比較して日本人部分集団で本薬 375/125 mg 群とプラセボ群との群
間差が小さい傾向が認められたこと及び変更前の主要評価項目の結果において本薬 375/125 mg 群とプラ
セボ群で統計学的な有意差が認められなかったことの要因について、現時点で、一定の考察ができる可能
性はあると考えるものの、評価・考察を行うための情報には限りがあることから、今後作成される予定の
本試験の総括報告書等の内容も踏まえ、改めて評価する必要がある。
現時点では、本剤の有効性について検討可能な情報に限りがある状況での結論であることに留意する
必要はあるが、症状発現から無作為化までの時間が 72 時間未満の SARS-CoV-2 による感染症患者に対し
て、プラセボ群と比較して本薬 375/125 mg 群において 5 症状の快復までの時間が短くなることが示され、
12 症状でも快復までの時間が短くなる傾向が認められたことも踏まえると、本剤が SARS-CoV-2 による
感染症に対する有効性を有すると推定するに足る情報は得られたと判断した。なお、本試験の総括報告書
等の有効性に関する新たな情報に基づき本剤の有効性については再検討を行い、その結果に応じ、製造販
売承認の見直しを含めた適切な対応を取る必要があると考える。
以上の機構の判断については、専門協議で議論する。
4.R.3 安全性について
申請者は、本剤の安全性プロファイルについて、以下のように説明している。
国際共同第Ⅱ/Ⅲ相試験(T1221 試験)における安全性の概要は表 11 のとおりであった。
12
ゾコーバ錠 125 mg_塩野義製薬株式会社_審査報告書(3)
14 / 23