よむ、つかう、まなぶ。
【資料No.5-1】四柳参考人提出資料 (20 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_26901.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会(令和4年度第3回 7/20)、医薬品第二部会(令和4年度第6回 7/20)(合同開催)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
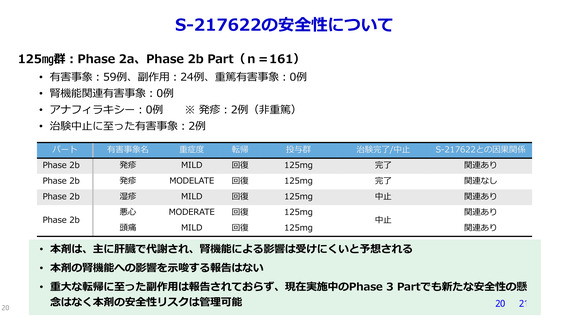
S-217622の安全性について
125㎎群:Phase 2a、Phase 2b Part(n=161)
• 有害事象:59例、副作用:24例、重篤有害事象:0例
• 腎機能関連有害事象:0例
• アナフィラキシー:0例
※ 発疹:2例(非重篤)
• 治験中止に至った有害事象:2例
パート
有害事象名
重症度
転帰
投与群
治験完了/中止
S-217622との因果関係
Phase 2b
発疹
MILD
回復
125mg
完了
関連あり
Phase 2b
発疹
MODELATE
回復
125mg
完了
関連なし
Phase 2b
湿疹
MILD
回復
125mg
中止
関連あり
悪心
MODERATE
回復
125mg
頭痛
MILD
回復
125mg
Phase 2b
中止
関連あり
関連あり
• 本剤は、主に肝臓で代謝され、腎機能による影響は受けにくいと予想される
• 本剤の腎機能への影響を示唆する報告はない
20
• 重大な転帰に至った副作用は報告されておらず、現在実施中のPhase 3 Partでも新たな安全性の懸
念はなく本剤の安全性リスクは管理可能
20 / 21
125㎎群:Phase 2a、Phase 2b Part(n=161)
• 有害事象:59例、副作用:24例、重篤有害事象:0例
• 腎機能関連有害事象:0例
• アナフィラキシー:0例
※ 発疹:2例(非重篤)
• 治験中止に至った有害事象:2例
パート
有害事象名
重症度
転帰
投与群
治験完了/中止
S-217622との因果関係
Phase 2b
発疹
MILD
回復
125mg
完了
関連あり
Phase 2b
発疹
MODELATE
回復
125mg
完了
関連なし
Phase 2b
湿疹
MILD
回復
125mg
中止
関連あり
悪心
MODERATE
回復
125mg
頭痛
MILD
回復
125mg
Phase 2b
中止
関連あり
関連あり
• 本剤は、主に肝臓で代謝され、腎機能による影響は受けにくいと予想される
• 本剤の腎機能への影響を示唆する報告はない
20
• 重大な転帰に至った副作用は報告されておらず、現在実施中のPhase 3 Partでも新たな安全性の懸
念はなく本剤の安全性リスクは管理可能
20 / 21