よむ、つかう、まなぶ。
資料4 今後のがんゲノム医療中核拠点病院等の指定の考え方について (9 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71567.html |
| 出典情報 | がんゲノム医療中核拠点病院等の指定要件に関するワーキンググループ(第7回 3/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
第63回医療上の必要性の高い未承認薬・適応外薬
検討会議(令和7年5月9日)資料2-1抜粋、一部改変
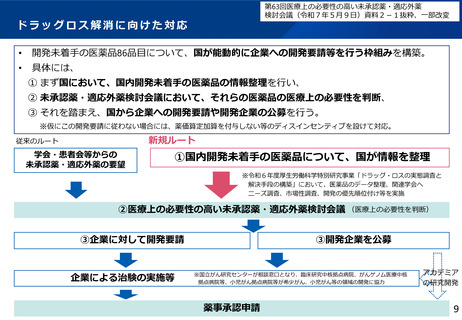
ドラッグロス解消に向けた対応
•
開発未着手の医薬品86品目について、国が能動的に企業への開発要請等を行う枠組みを構築。
•
具体には、
① まず国において、国内開発未着手の医薬品の情報整理を行い、
② 未承認薬・適応外薬検討会議において、それらの医薬品の医療上の必要性を判断、
③ それを踏まえ、国から企業への開発要請や開発企業の公募を行う。
※仮にこの開発要請に従わない場合には、薬価算定加算を付与しない等のディスインセンティブを設けて対応。
新規ルート
従来のルート
学会・患者会等からの
未承認薬・適応外薬の要望
①国内開発未着手の医薬品について、国が情報を整理
※令和6年度厚生労働科学特別研究事業「ドラッグ・ロスの実態調査と
解決手段の構築」において、医薬品のデータ整理、関連学会へ
ニーズ調査、市場性調査、開発の優先順位付け等を実施
②医療上の必要性の高い未承認薬・適応外薬検討会議 (医療上の必要性を判断)
③企業に対して開発要請
企業による治験の実施等
③開発企業を公募
※国立がん研究センターが相談窓口となり、臨床研究中核拠点病院、がんゲノム医療中核
拠点病院等、小児がん拠点病院等が希少がん、小児がん等の領域の開発に協力
薬事承認申請
アカデミア
の研究開発
9
検討会議(令和7年5月9日)資料2-1抜粋、一部改変
ドラッグロス解消に向けた対応
•
開発未着手の医薬品86品目について、国が能動的に企業への開発要請等を行う枠組みを構築。
•
具体には、
① まず国において、国内開発未着手の医薬品の情報整理を行い、
② 未承認薬・適応外薬検討会議において、それらの医薬品の医療上の必要性を判断、
③ それを踏まえ、国から企業への開発要請や開発企業の公募を行う。
※仮にこの開発要請に従わない場合には、薬価算定加算を付与しない等のディスインセンティブを設けて対応。
新規ルート
従来のルート
学会・患者会等からの
未承認薬・適応外薬の要望
①国内開発未着手の医薬品について、国が情報を整理
※令和6年度厚生労働科学特別研究事業「ドラッグ・ロスの実態調査と
解決手段の構築」において、医薬品のデータ整理、関連学会へ
ニーズ調査、市場性調査、開発の優先順位付け等を実施
②医療上の必要性の高い未承認薬・適応外薬検討会議 (医療上の必要性を判断)
③企業に対して開発要請
企業による治験の実施等
③開発企業を公募
※国立がん研究センターが相談窓口となり、臨床研究中核拠点病院、がんゲノム医療中核
拠点病院等、小児がん拠点病院等が希少がん、小児がん等の領域の開発に協力
薬事承認申請
アカデミア
の研究開発
9