よむ、つかう、まなぶ。
資料4 今後のがんゲノム医療中核拠点病院等の指定の考え方について (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71567.html |
| 出典情報 | がんゲノム医療中核拠点病院等の指定要件に関するワーキンググループ(第7回 3/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
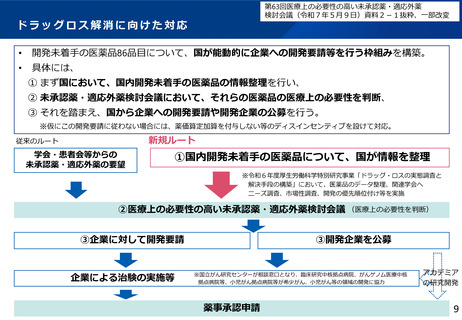
ドラッグ・ラグ/ドラッグ・ロスの実態
第63回医療上の必要性の高い未承認薬・適応外薬
検討会議(令和7年5月9日)資料2-1抜粋、一部改変
•
2016~2020年に欧米で承認された医薬品のうち、2023年3月時点で日本では承認されていない医
薬品(未承認薬)は143品目。
•
そのうち、そもそも開発未着手で、承認申請すらなされない医薬品が86品目(60.1%)。
⇒ ドラッグラグ・ロスの発生
•
開発未着手の86品目は、ベンチャー※1発の医薬品やオーファン、小児※2の割合が大きい。
※1:日本に開発拠点を有さない企業が多く、日本の薬事制度等を把握していない可能性が高い。
※2:市場規模が小さい等の理由から、開発が進みづらい。
日欧米のドラッグラグ・ロスの状況
米国
欧州
承認済
未承認合計
136
7
86
57
日本国内未着手の品目内訳
未承認の内数 (品目数)
開発中
未着手
3
4
26
31
内訳
ベンチャー発
希少疾病用医薬品
(オーファン)
小児用医薬品
56
47
37
%
(48品目)
%
(40品目)
%
(32品目)
※ロス86品目のうち、ベンチャー、オーファン、小児のいずれでもない品目は14品目(16%)
日本
0
143
57
86
(品目)
8
第63回医療上の必要性の高い未承認薬・適応外薬
検討会議(令和7年5月9日)資料2-1抜粋、一部改変
•
2016~2020年に欧米で承認された医薬品のうち、2023年3月時点で日本では承認されていない医
薬品(未承認薬)は143品目。
•
そのうち、そもそも開発未着手で、承認申請すらなされない医薬品が86品目(60.1%)。
⇒ ドラッグラグ・ロスの発生
•
開発未着手の86品目は、ベンチャー※1発の医薬品やオーファン、小児※2の割合が大きい。
※1:日本に開発拠点を有さない企業が多く、日本の薬事制度等を把握していない可能性が高い。
※2:市場規模が小さい等の理由から、開発が進みづらい。
日欧米のドラッグラグ・ロスの状況
米国
欧州
承認済
未承認合計
136
7
86
57
日本国内未着手の品目内訳
未承認の内数 (品目数)
開発中
未着手
3
4
26
31
内訳
ベンチャー発
希少疾病用医薬品
(オーファン)
小児用医薬品
56
47
37
%
(48品目)
%
(40品目)
%
(32品目)
※ロス86品目のうち、ベンチャー、オーファン、小児のいずれでもない品目は14品目(16%)
日本
0
143
57
86
(品目)
8