よむ、つかう、まなぶ。
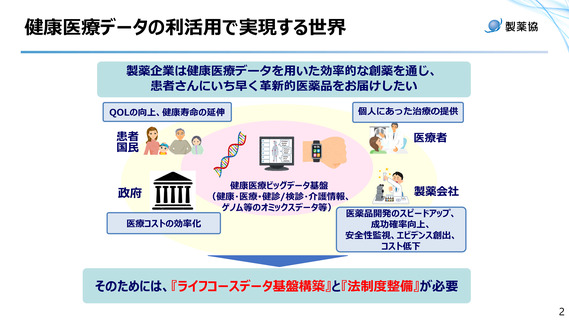
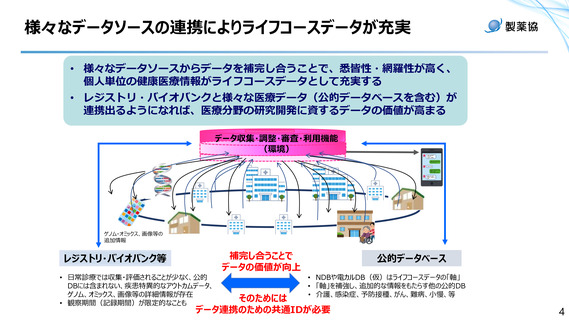
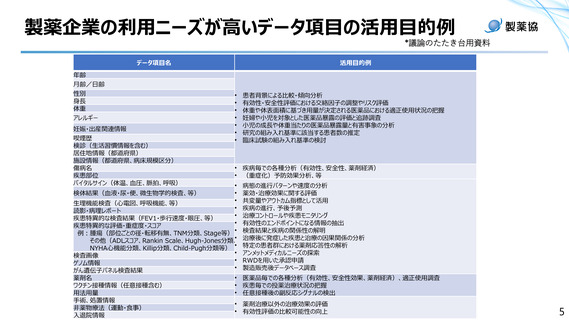
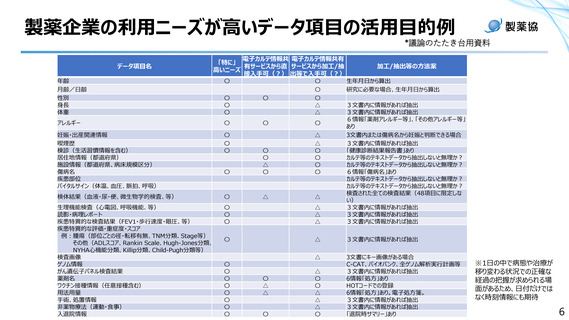
資料1ー6 日本製薬工業協会提出資料 (7 ページ)
出典
| 公開元URL | https://www8.cao.go.jp/kisei-kaikaku/kisei/meeting/wg/2501_02medical/260311/medical10_agenda.html |
| 出典情報 | 規制改革推進会議 健康・医療・介護ワーキング・グループ(第10回 3/11)《内閣府》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
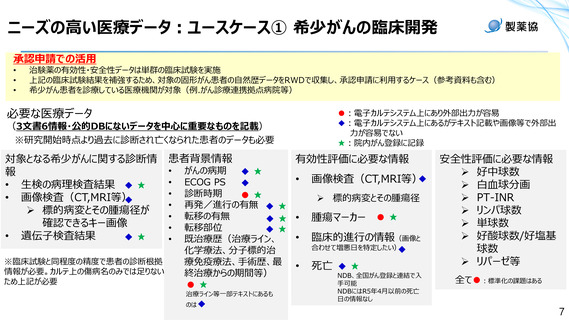
ニーズの高い医療データ:ユースケース① 希少がんの臨床開発
承認申請での活用
•
•
•
治験薬の有効性・安全性データは単群の臨床試験を実施
上記の臨床試験結果を補強するため、対象の固形がん患者の自然歴データをRWDで収集し、承認申請に利用するケース(参考資料も含む)
希少がん患者を診療している医療機関が対象(例.がん診療連携拠点病院等)
必要な医療データ
●:電子カルテシステム上にあり外部出力が容易
◆:電子カルテシステム上にあるがテキスト記載や画像等で外部出
力が容易でない
★:院内がん登録に記録
(3文書6情報・公的DBにないデータを中心に重要なものを記載)
※研究開始時点より過去に診断され亡くなられた患者のデータも必要
対象となる希少がんに関する診断情
報
• 生検の病理検査結果 ◆ ★
• 画像検査(CT,MRI等)
◆
標的病変とその腫瘍径が
確認できるキー画像
• 遺伝子検査結果
◆★
※臨床試験と同程度の精度で患者の診断根拠
情報が必要。カルテ上の傷病名のみでは足りない
ため上記が必要
患者背景情報
•
•
•
•
•
•
•
がんの病期 ◆ ★
ECOG PS
◆
診断時期
●★
再発/進行の有無 ◆ ★
転移の有無
◆★
転移部位
◆★
既治療歴(治療ライン、
化学療法、分子標的治
療免疫療法、手術歴、最
終治療からの期間等)
●★
治療ライン等一部テキストにあるも
のは◆
有効性評価に必要な情報
•
画像検査(CT,MRI等)◆
標的病変とその腫瘍径
•
腫瘍マーカー ● ★
•
臨床的進行の情報(画像と
•
合わせて増悪日を特定したい)
◆
死亡 ◆ ★
NDB、全国がん登録と連結で入
手可能
NDBにはR5年4月以前の死亡
日の情報なし
安全性評価に必要な情報
好中球数
白血球分画
PT-INR
リンパ球数
単球数
好酸球数/好塩基
球数
リパーゼ等
全て●:標準化の課題はある
7
承認申請での活用
•
•
•
治験薬の有効性・安全性データは単群の臨床試験を実施
上記の臨床試験結果を補強するため、対象の固形がん患者の自然歴データをRWDで収集し、承認申請に利用するケース(参考資料も含む)
希少がん患者を診療している医療機関が対象(例.がん診療連携拠点病院等)
必要な医療データ
●:電子カルテシステム上にあり外部出力が容易
◆:電子カルテシステム上にあるがテキスト記載や画像等で外部出
力が容易でない
★:院内がん登録に記録
(3文書6情報・公的DBにないデータを中心に重要なものを記載)
※研究開始時点より過去に診断され亡くなられた患者のデータも必要
対象となる希少がんに関する診断情
報
• 生検の病理検査結果 ◆ ★
• 画像検査(CT,MRI等)
◆
標的病変とその腫瘍径が
確認できるキー画像
• 遺伝子検査結果
◆★
※臨床試験と同程度の精度で患者の診断根拠
情報が必要。カルテ上の傷病名のみでは足りない
ため上記が必要
患者背景情報
•
•
•
•
•
•
•
がんの病期 ◆ ★
ECOG PS
◆
診断時期
●★
再発/進行の有無 ◆ ★
転移の有無
◆★
転移部位
◆★
既治療歴(治療ライン、
化学療法、分子標的治
療免疫療法、手術歴、最
終治療からの期間等)
●★
治療ライン等一部テキストにあるも
のは◆
有効性評価に必要な情報
•
画像検査(CT,MRI等)◆
標的病変とその腫瘍径
•
腫瘍マーカー ● ★
•
臨床的進行の情報(画像と
•
合わせて増悪日を特定したい)
◆
死亡 ◆ ★
NDB、全国がん登録と連結で入
手可能
NDBにはR5年4月以前の死亡
日の情報なし
安全性評価に必要な情報
好中球数
白血球分画
PT-INR
リンパ球数
単球数
好酸球数/好塩基
球数
リパーゼ等
全て●:標準化の課題はある
7