よむ、つかう、まなぶ。
参考資料2-2 患者向医薬品ガイド検討会 とりまとめ 概要資料[1.8MB] (9 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_70725.html |
| 出典情報 | 薬事審議会 医薬品等安全対策部会(令和7年度第4回 3/6)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
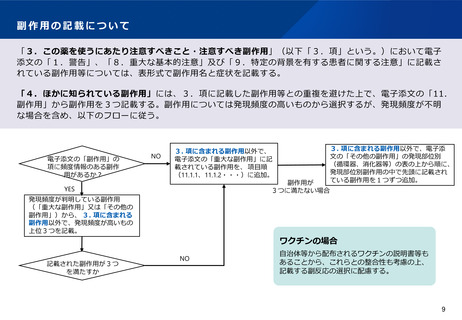
副作用の記載について
「3.この薬を使うにあたり注意すべきこと・注意すべき副作用」(以下「3.項」という。)において電子
添文の「1.警告」、「8.重大な基本的注意」及び「9.特定の背景を有する患者に関する注意」に記載さ
れている副作用等については、表形式で副作用名と症状を記載する。
「4.ほかに知られている副作用」には、3.項に記載した副作用等との重複を避けた上で、電子添文の「11.
副作用」から副作用を3つ記載する。副作用については発現頻度の高いものから選択するが、発現頻度が不明
な場合を含め、以下のフローに従う。
電子添文の「副作用」の
項に頻度情報のある副作
用があるか?
NO
3. 項に含まれる副作用以外で、
電子添文の「重大な副作用」に記
載されている副作用を、 項目順
(11.1.1、11.1.2・・・)に追加。
副作用が
3つに満たない場合
YES
3. 項に含まれる副作用以外で、電子添
文の「その他の副作用」の発現部位別
(循環器、消化器等)の表の上から順に、
発現部位別副作用の中で先頭に記載され
ている副作用を1つずつ追加。
発現頻度が判明している副作用
(「重大な副作用」又は「その他の
副作用」)から、 3. 項に含まれる
副作用以外で、発現頻度が高いもの
上位3つを記載。
ワクチンの場合
記載された副作用が3つ
を満たすか
NO
自治体等から配布されるワクチンの説明書等も
あることから、これらとの整合性も考慮の上、
記載する副反応の選択に配慮する。
9
「3.この薬を使うにあたり注意すべきこと・注意すべき副作用」(以下「3.項」という。)において電子
添文の「1.警告」、「8.重大な基本的注意」及び「9.特定の背景を有する患者に関する注意」に記載さ
れている副作用等については、表形式で副作用名と症状を記載する。
「4.ほかに知られている副作用」には、3.項に記載した副作用等との重複を避けた上で、電子添文の「11.
副作用」から副作用を3つ記載する。副作用については発現頻度の高いものから選択するが、発現頻度が不明
な場合を含め、以下のフローに従う。
電子添文の「副作用」の
項に頻度情報のある副作
用があるか?
NO
3. 項に含まれる副作用以外で、
電子添文の「重大な副作用」に記
載されている副作用を、 項目順
(11.1.1、11.1.2・・・)に追加。
副作用が
3つに満たない場合
YES
3. 項に含まれる副作用以外で、電子添
文の「その他の副作用」の発現部位別
(循環器、消化器等)の表の上から順に、
発現部位別副作用の中で先頭に記載され
ている副作用を1つずつ追加。
発現頻度が判明している副作用
(「重大な副作用」又は「その他の
副作用」)から、 3. 項に含まれる
副作用以外で、発現頻度が高いもの
上位3つを記載。
ワクチンの場合
記載された副作用が3つ
を満たすか
NO
自治体等から配布されるワクチンの説明書等も
あることから、これらとの整合性も考慮の上、
記載する副反応の選択に配慮する。
9