よむ、つかう、まなぶ。
費薬材-1条件期限付き再⽣医療等製品の診療報酬上の算定方法の⾒直しについて (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_65755.html |
| 出典情報 | 中央社会保険医療協議会 費用対効果評価専門部会・薬価専門部会・保険医療材料専門部会 合同部会(第22回 11/12)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
1.薬価及び材料価格算定
とりまとめの方向(案)
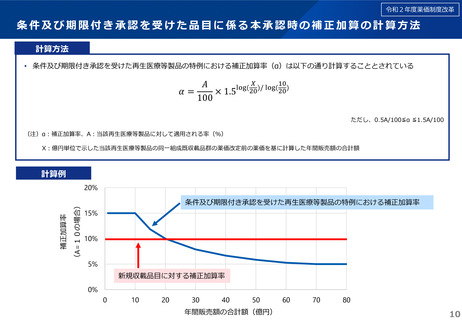
条件及び期限付き承認を受けた再生医療等製品の薬価・材料価格算定については、有効性が確認ではなく推定されたことをもって
同承認が付与されたことを踏まえ、以下の点を対応として取りまとめることとしてはどうか。
• 原価計算方式により算定される場合に用いる営業利益率の係数は、有効性が不確実な段階で利益をどこまで保障すべきかという
意見があることから、平均的な営業利益率に0.5を乗じた値を用いることとする。
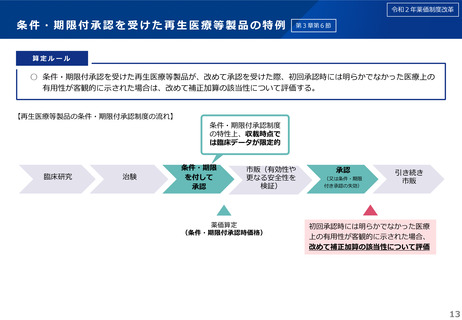
• 有用性系加算については、本承認時に改めて該当性を判断することとし、算定時には該当性を判断しない。
• 有用性系加算以外の補正加算については、市場規模が小さいが医療上の必要性が高い医薬品の評価・革新的な新薬の日本へ早期
導入の評価によりイノベーションを推進するという当該補正加算の趣旨を鑑み、有効性が確認ではなく推定されたことをもって
条件及び期限付き承認承認が付与されたことを踏まえた上で、算定時に該当性等を判断する。
• 革新的な新薬の創出を加速させるための新薬創出等加算の適用については、通常の承認を受けた再生医療等製品と同様に取り扱
うこととする。
• 外国平均価格調整について、価格の引き上げ、引き下げともに、通常の承認を受けた再生医療等製品と同様の取り扱いとする。
• その他の算定ルールの適用については、通常の承認を受けた再生医療等製品と同様の取り扱いとする。
6
とりまとめの方向(案)
条件及び期限付き承認を受けた再生医療等製品の薬価・材料価格算定については、有効性が確認ではなく推定されたことをもって
同承認が付与されたことを踏まえ、以下の点を対応として取りまとめることとしてはどうか。
• 原価計算方式により算定される場合に用いる営業利益率の係数は、有効性が不確実な段階で利益をどこまで保障すべきかという
意見があることから、平均的な営業利益率に0.5を乗じた値を用いることとする。
• 有用性系加算については、本承認時に改めて該当性を判断することとし、算定時には該当性を判断しない。
• 有用性系加算以外の補正加算については、市場規模が小さいが医療上の必要性が高い医薬品の評価・革新的な新薬の日本へ早期
導入の評価によりイノベーションを推進するという当該補正加算の趣旨を鑑み、有効性が確認ではなく推定されたことをもって
条件及び期限付き承認承認が付与されたことを踏まえた上で、算定時に該当性等を判断する。
• 革新的な新薬の創出を加速させるための新薬創出等加算の適用については、通常の承認を受けた再生医療等製品と同様に取り扱
うこととする。
• 外国平均価格調整について、価格の引き上げ、引き下げともに、通常の承認を受けた再生医療等製品と同様の取り扱いとする。
• その他の算定ルールの適用については、通常の承認を受けた再生医療等製品と同様の取り扱いとする。
6