よむ、つかう、まなぶ。
費薬材-1条件及び期限付承認に関する意見 (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_65349.html |
| 出典情報 | 中央社会保険医療協議会 費用対効果評価専門部会・薬価専門部会・保険医療材料専門部会 合同部会(第21回 10/29)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
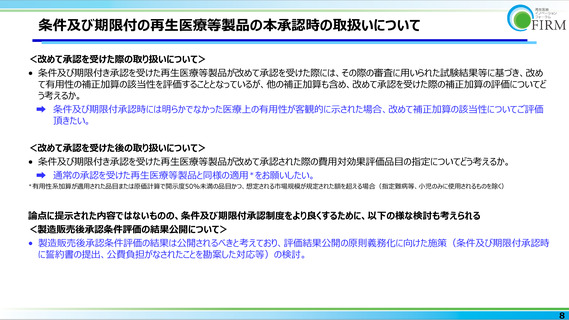
条件及び期限付の再生医療等製品の本承認時の取扱いについて
<改めて承認を受けた際の取り扱いについて>
• 条件及び期限付き承認を受けた再生医療等製品が改めて承認を受けた際には、その際の審査に用いられた試験結果等に基づき、改め
て有用性の補正加算の該当性を評価することとなっているが、他の補正加算も含め、改めて承認を受けた際の補正加算の評価についてど
う考えるか。
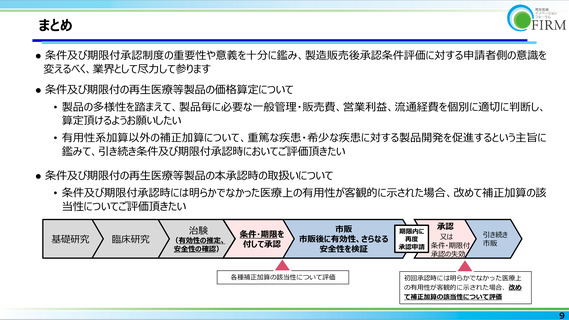
➡ 条件及び期限付承認時には明らかでなかった医療上の有用性が客観的に示された場合、改めて補正加算の該当性についてご評価
頂きたい。
<改めて承認を受けた後の取り扱いについて>
• 条件及び期限付き承認を受けた再生医療等製品が改めて承認された際の費用対効果評価品目の指定についてどう考えるか。
➡ 通常の承認を受けた再生医療等製品と同様の適用*をお願いしたい。
*有用性系加算が適用された品目または原価計算で開示度50%未満の品目かつ、想定される市場規模が規定された額を超える場合(指定難病等、小児のみに使用されるものを除く)
論点に提示された内容ではないものの、条件及び期限付承認制度をより良くするために、以下の様な検討も考えられる
<製造販売後承認条件評価の結果公開について>
• 製造販売後承認条件評価の結果は公開されるべきと考えており、評価結果公開の原則義務化に向けた施策(条件及び期限付承認時
に誓約書の提出、公費負担がなされたことを勘案した対応等)の検討。
8
<改めて承認を受けた際の取り扱いについて>
• 条件及び期限付き承認を受けた再生医療等製品が改めて承認を受けた際には、その際の審査に用いられた試験結果等に基づき、改め
て有用性の補正加算の該当性を評価することとなっているが、他の補正加算も含め、改めて承認を受けた際の補正加算の評価についてど
う考えるか。
➡ 条件及び期限付承認時には明らかでなかった医療上の有用性が客観的に示された場合、改めて補正加算の該当性についてご評価
頂きたい。
<改めて承認を受けた後の取り扱いについて>
• 条件及び期限付き承認を受けた再生医療等製品が改めて承認された際の費用対効果評価品目の指定についてどう考えるか。
➡ 通常の承認を受けた再生医療等製品と同様の適用*をお願いしたい。
*有用性系加算が適用された品目または原価計算で開示度50%未満の品目かつ、想定される市場規模が規定された額を超える場合(指定難病等、小児のみに使用されるものを除く)
論点に提示された内容ではないものの、条件及び期限付承認制度をより良くするために、以下の様な検討も考えられる
<製造販売後承認条件評価の結果公開について>
• 製造販売後承認条件評価の結果は公開されるべきと考えており、評価結果公開の原則義務化に向けた施策(条件及び期限付承認時
に誓約書の提出、公費負担がなされたことを勘案した対応等)の検討。
8