よむ、つかう、まなぶ。
費薬材-1条件及び期限付承認に関する意見 (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_65349.html |
| 出典情報 | 中央社会保険医療協議会 費用対効果評価専門部会・薬価専門部会・保険医療材料専門部会 合同部会(第21回 10/29)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
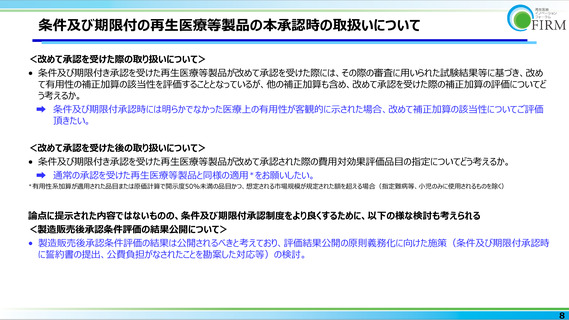
製造販売後承認条件評価について
● 再生医療等製品に係る条件及び期限付承認並びにその後の有効性評価計画策定に関するガイダンス
再生医療等製品に係る条件及び期限付承認並びにその後の有効性評価計画策定に関するガイダンスについて(医薬機審発0329第3号 令和6年3月29日)
• 条件及び期限付承認後の再申請に向けて、本製品の有効性検証を行うことを念頭に入れ、試験の成功確
率を高めるために十分な検討を行う
• PMDAの相談制度も活用しながら、個別の製品に固有の特性も十分理解した上で、「合理性のある判断又
は評価が達成できない可能性」を最小化する
● 条件及び期限付承認時の情報収集とその活用
• 条件及び期限付承認期間の情報収集は、単に医療情報の集約のみでなく、関連する製造関連情報の集
約が重要である。加えて、これら情報の収集方法ならびにその評価方法の適切性を確保する活動も必要で
ある
• 承認取り消し製品の検証こそ重要で、製品の課題、使用方法の課題、検証方法の課題などを明らかにし、
経験値として次の製品へ活用する
• パブリックヘルスの観点からも、製造販売後承認条件評価の結果は公開する
4
● 再生医療等製品に係る条件及び期限付承認並びにその後の有効性評価計画策定に関するガイダンス
再生医療等製品に係る条件及び期限付承認並びにその後の有効性評価計画策定に関するガイダンスについて(医薬機審発0329第3号 令和6年3月29日)
• 条件及び期限付承認後の再申請に向けて、本製品の有効性検証を行うことを念頭に入れ、試験の成功確
率を高めるために十分な検討を行う
• PMDAの相談制度も活用しながら、個別の製品に固有の特性も十分理解した上で、「合理性のある判断又
は評価が達成できない可能性」を最小化する
● 条件及び期限付承認時の情報収集とその活用
• 条件及び期限付承認期間の情報収集は、単に医療情報の集約のみでなく、関連する製造関連情報の集
約が重要である。加えて、これら情報の収集方法ならびにその評価方法の適切性を確保する活動も必要で
ある
• 承認取り消し製品の検証こそ重要で、製品の課題、使用方法の課題、検証方法の課題などを明らかにし、
経験値として次の製品へ活用する
• パブリックヘルスの観点からも、製造販売後承認条件評価の結果は公開する
4