よむ、つかう、まなぶ。
(資料1)危機対応医薬品等(MCM)の利用可能性確保に関する検討 (8 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_62702.html |
| 出典情報 | 厚生科学審議会 危機対応医薬品等に関する小委員会(第9回 9/1)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
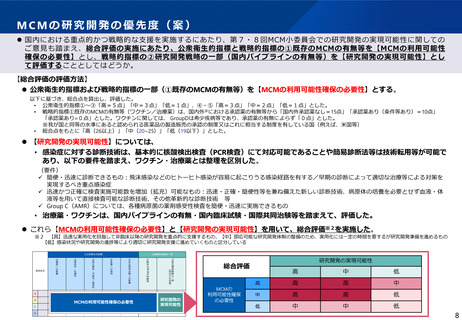
研究開発の基本的考え方(案)に基づく優先度(イメージ)
研究開発の
優先度
疾
病
負
荷
が
高
い
/
高
く
な
る
蓋
然
性
が
あ
る
重
点
感
染
症
国
内
外
に
承
認
薬
が
な
い
臨床研究段階の国内パイプライン
(基礎~応用)
臨床研究段階の国内パイプライン
(前臨床以降)
国内臨床試験:困難
(国際共同治験が必要※)
低
国内臨床試験:可
中
国内臨床試験:困難
(国際共同治験が必要)
中
国内臨床試験:可
高
既存薬と同一モダリティ/作用機序等
国
内
外
い
ず
れ
か
に
承
認
薬
あ
り
臨床研究段階の国内パイプライン
(基礎~応用)
低
国内臨床試験:困難
(国際共同治験が必要)
低
国内臨床試験:可
中
既存薬と異なるモダリティ/作用機序等
既存薬と同一モダリティ/作用機序等
臨床研究段階の国内パイプライン
(前臨床以降)
低
国内臨床試験:困難
(国際共同治験が必要)
中
国内臨床試験:可
高
既存薬と異なるモダリティ/作用機序等
(参考)国立研究開発法人日本医療研究開発機構(AMED)各開発フェーズの定義
https://www.amed.go.jp/content/000022342.pdf
7
研究開発の
優先度
疾
病
負
荷
が
高
い
/
高
く
な
る
蓋
然
性
が
あ
る
重
点
感
染
症
国
内
外
に
承
認
薬
が
な
い
臨床研究段階の国内パイプライン
(基礎~応用)
臨床研究段階の国内パイプライン
(前臨床以降)
国内臨床試験:困難
(国際共同治験が必要※)
低
国内臨床試験:可
中
国内臨床試験:困難
(国際共同治験が必要)
中
国内臨床試験:可
高
既存薬と同一モダリティ/作用機序等
国
内
外
い
ず
れ
か
に
承
認
薬
あ
り
臨床研究段階の国内パイプライン
(基礎~応用)
低
国内臨床試験:困難
(国際共同治験が必要)
低
国内臨床試験:可
中
既存薬と異なるモダリティ/作用機序等
既存薬と同一モダリティ/作用機序等
臨床研究段階の国内パイプライン
(前臨床以降)
低
国内臨床試験:困難
(国際共同治験が必要)
中
国内臨床試験:可
高
既存薬と異なるモダリティ/作用機序等
(参考)国立研究開発法人日本医療研究開発機構(AMED)各開発フェーズの定義
https://www.amed.go.jp/content/000022342.pdf
7