よむ、つかう、まなぶ。
08 参考資料1-2 沈降ヘモフィルスb型ワクチンファクトシート[2.4MB] (20 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_34803.html |
| 出典情報 | 厚生科学審議会 予防接種・ワクチン分科会 予防接種基本方針部会 ワクチン評価に関する小委員会(第20回 8/29)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
⑤ 安全性
⑤-1. 国内臨床試験における安全性評価
VaxemHib の国内における臨床試験の概要を表 7 に示す。
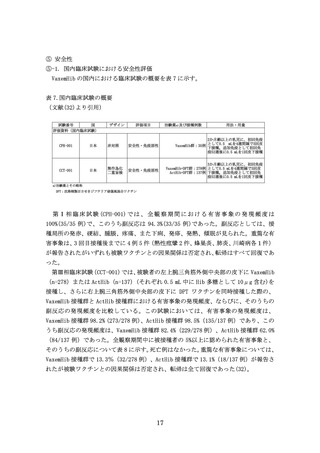
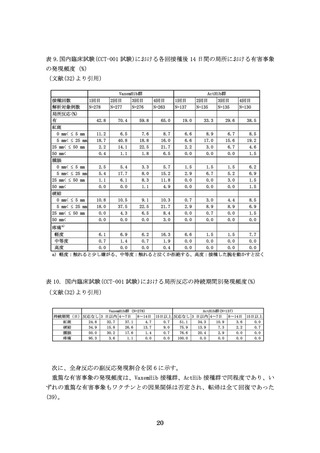
表 7.国内臨床試験の概要
(文献(32)より引用)
第 Ⅰ 相 臨 床 試 験 (CPH-001) で は 、 全 観 察 期 間 に お け る 有 害 事 象 の 発 現 頻 度 は
100%(35/35 例)で、このうち副反応は 94.3%(33/35 例)であった。副反応としては、接
種局所の発赤、硬結、腫脹、疼痛、また下痢、発疹、発熱、傾眠が見られた。重篤な有
害事象は、3 回目接種後までに 4 例 5 件(熱性痙攣 2 件、蜂巣炎、肺炎、川崎病各1件)
が報告されたがいずれも被験ワクチンとの因果関係は否定され、転帰はすべて回復であ
った。
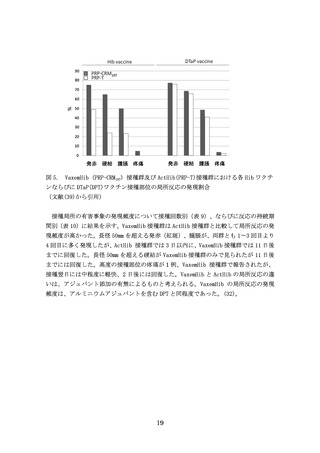
第Ⅲ相臨床試験(CCT-001)では、被験者の左上腕三角筋外側中央部の皮下に VaxemHib
(n=278)または ActHib(n=137)(それぞれ 0.5 mL 中に Hib 多糖として 10μg 含む)を
接種し、さらに右上腕三角筋外側中央部の皮下に DPT ワクチンを同時接種した際の、
VaxemHib 接種群と ActHib 接種群における有害事象の発現頻度、ならびに、そのうちの
副反応の発現頻度を比較している。この試験においては、有害事象の発現頻度は、
VaxemHib 接種群 98.2% (273/278 例)、ActHib 接種群 98.5%(135/137 例)であり、この
うち副反応の発現頻度は、VaxemHib 接種群 82.4%(229/278 例)、ActHib 接種群 62.0%
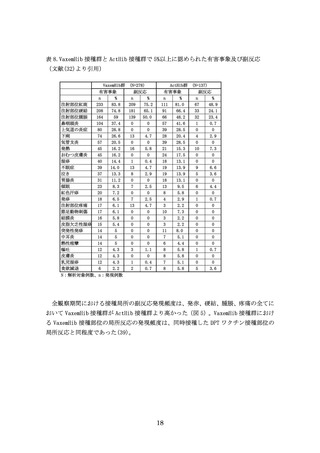
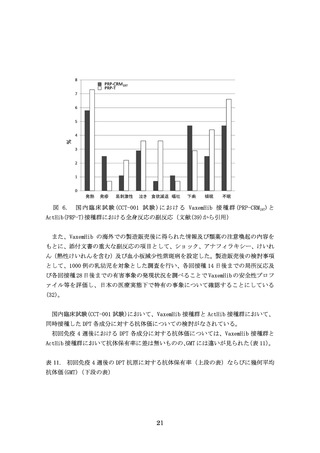
(84/137 例)であった。全観察期間中に被接種者の 5%以上に認められた有害事象と、
そのうちの副反応について表 8 に示す。死亡例はなかった。重篤な有害事象については、
VaxemHib 接種群で 13.3%(32/278 例)、ActHib 接種群で 13.1%(18/137 例)が報告さ
れたが被験ワクチンとの因果関係は否定され、転帰は全て回復であった(32)。
17
⑤-1. 国内臨床試験における安全性評価
VaxemHib の国内における臨床試験の概要を表 7 に示す。
表 7.国内臨床試験の概要
(文献(32)より引用)
第 Ⅰ 相 臨 床 試 験 (CPH-001) で は 、 全 観 察 期 間 に お け る 有 害 事 象 の 発 現 頻 度 は
100%(35/35 例)で、このうち副反応は 94.3%(33/35 例)であった。副反応としては、接
種局所の発赤、硬結、腫脹、疼痛、また下痢、発疹、発熱、傾眠が見られた。重篤な有
害事象は、3 回目接種後までに 4 例 5 件(熱性痙攣 2 件、蜂巣炎、肺炎、川崎病各1件)
が報告されたがいずれも被験ワクチンとの因果関係は否定され、転帰はすべて回復であ
った。
第Ⅲ相臨床試験(CCT-001)では、被験者の左上腕三角筋外側中央部の皮下に VaxemHib
(n=278)または ActHib(n=137)(それぞれ 0.5 mL 中に Hib 多糖として 10μg 含む)を
接種し、さらに右上腕三角筋外側中央部の皮下に DPT ワクチンを同時接種した際の、
VaxemHib 接種群と ActHib 接種群における有害事象の発現頻度、ならびに、そのうちの
副反応の発現頻度を比較している。この試験においては、有害事象の発現頻度は、
VaxemHib 接種群 98.2% (273/278 例)、ActHib 接種群 98.5%(135/137 例)であり、この
うち副反応の発現頻度は、VaxemHib 接種群 82.4%(229/278 例)、ActHib 接種群 62.0%
(84/137 例)であった。全観察期間中に被接種者の 5%以上に認められた有害事象と、
そのうちの副反応について表 8 に示す。死亡例はなかった。重篤な有害事象については、
VaxemHib 接種群で 13.3%(32/278 例)、ActHib 接種群で 13.1%(18/137 例)が報告さ
れたが被験ワクチンとの因果関係は否定され、転帰は全て回復であった(32)。
17
関連画像
ページ内で利用されている画像ファイルです。
有料会員登録をして頂くことで、このページ内で利用されている画像を個別に閲覧・ダウンロードすることができるようになります。