よむ、つかう、まなぶ。
【資料3】医薬品等行政評価・監視委員会における海外調査(令和4年度・欧米の薬事制度に関する調査) (40 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_32109.html |
| 出典情報 | 医薬品等行政評価・監視委員会(第11回 3/23)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
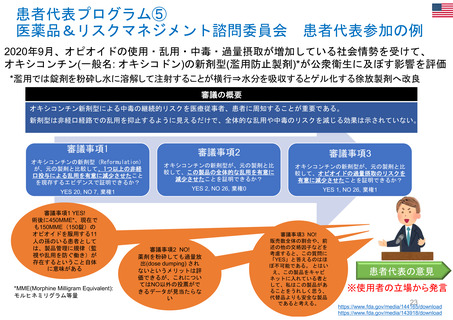
条件付き承認制度の対象品目
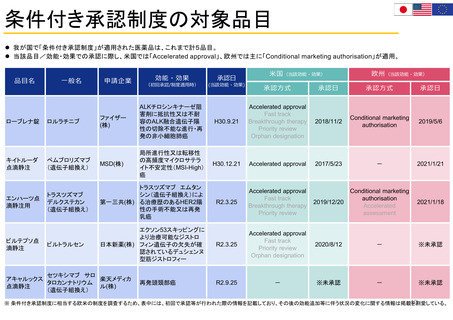
我が国で「条件付き承認制度」が適用された医薬品は、これまで計5品目。
当該品目/効能・効果での承認に際し、米国では「Accelerated approval」、欧州では主に「Conditional marketing authorisation」が適用。
品目名
一般名
申請企業
効能・効果
(初回承認/制度適用時)
(当該効能・効果)
米国 (当該効能・効果)
欧州 (当該効能・効果)
承認方式
承認日
承認方式
承認日
2018/11/2
Conditional marketing
authorisation
2019/5/6
2017/5/23
-
2021/1/21
2021/1/18
ファイザー
(株)
ALKチロシンキナーゼ阻
害剤に抵抗性又は不耐
容のALK融合遺伝子陽
性の切除不能な進行・再
発の非小細胞肺癌
H30.9.21
Accelerated approval
Fast track
Breakthrough therapy
Priority review
Orphan designation
局所進行性又は転移性
の高頻度マイクロサテラ
イト不安定性(MSI-High)
癌
H30.12.21
Accelerated approval
R2.3.25
Accelerated approval
Fast track
Breakthrough therapy
Priority review
2019/12/20
Conditional marketing
authorisation
Accelerated
assessment
R2.3.25
Accelerated approval
Fast track
Priority review
Orphan designation
2020/8/12
-
※未承認
R2.9.25
-
※未承認
-
※未承認
ローブレナ錠
ロルラチニブ
キイトルーダ
点滴静注
ペムブロリズマブ
(遺伝子組換え)
MSD(株)
エンハーツ点
滴静注用
トラスツズマブ
デルクステカン
(遺伝子組換え)
トラスツズマブ エムタン
シン(遺伝子組換え)によ
第一三共(株) る治療歴のあるHER2陽
性の手術不能又は再発
乳癌
ビルトラルセン
エクソン53スキッピングに
より治療可能なジストロ
日本新薬(株) フィン遺伝子の欠失が確
認されているデュシェンヌ
型筋ジストロフィー
ビルテプソ点
滴静注
承認日
セツキシマブ サロ
アキャルックス
楽天メディカ
タロカンナトリウム
点滴静注
ル(株)
(遺伝子組換え)
再発頭頸部癌
40
※ 条件付き承認制度に相当する欧米の制度を調査するため、表中には、初回で承認等が行われた際の情報を記載しており、その後の効能追加等に伴う状況の変化に関する情報は掲載を割愛している。
我が国で「条件付き承認制度」が適用された医薬品は、これまで計5品目。
当該品目/効能・効果での承認に際し、米国では「Accelerated approval」、欧州では主に「Conditional marketing authorisation」が適用。
品目名
一般名
申請企業
効能・効果
(初回承認/制度適用時)
(当該効能・効果)
米国 (当該効能・効果)
欧州 (当該効能・効果)
承認方式
承認日
承認方式
承認日
2018/11/2
Conditional marketing
authorisation
2019/5/6
2017/5/23
-
2021/1/21
2021/1/18
ファイザー
(株)
ALKチロシンキナーゼ阻
害剤に抵抗性又は不耐
容のALK融合遺伝子陽
性の切除不能な進行・再
発の非小細胞肺癌
H30.9.21
Accelerated approval
Fast track
Breakthrough therapy
Priority review
Orphan designation
局所進行性又は転移性
の高頻度マイクロサテラ
イト不安定性(MSI-High)
癌
H30.12.21
Accelerated approval
R2.3.25
Accelerated approval
Fast track
Breakthrough therapy
Priority review
2019/12/20
Conditional marketing
authorisation
Accelerated
assessment
R2.3.25
Accelerated approval
Fast track
Priority review
Orphan designation
2020/8/12
-
※未承認
R2.9.25
-
※未承認
-
※未承認
ローブレナ錠
ロルラチニブ
キイトルーダ
点滴静注
ペムブロリズマブ
(遺伝子組換え)
MSD(株)
エンハーツ点
滴静注用
トラスツズマブ
デルクステカン
(遺伝子組換え)
トラスツズマブ エムタン
シン(遺伝子組換え)によ
第一三共(株) る治療歴のあるHER2陽
性の手術不能又は再発
乳癌
ビルトラルセン
エクソン53スキッピングに
より治療可能なジストロ
日本新薬(株) フィン遺伝子の欠失が確
認されているデュシェンヌ
型筋ジストロフィー
ビルテプソ点
滴静注
承認日
セツキシマブ サロ
アキャルックス
楽天メディカ
タロカンナトリウム
点滴静注
ル(株)
(遺伝子組換え)
再発頭頸部癌
40
※ 条件付き承認制度に相当する欧米の制度を調査するため、表中には、初回で承認等が行われた際の情報を記載しており、その後の効能追加等に伴う状況の変化に関する情報は掲載を割愛している。