よむ、つかう、まなぶ。
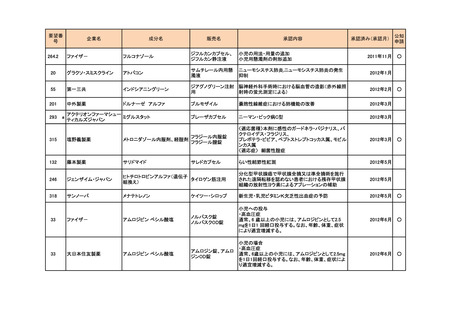
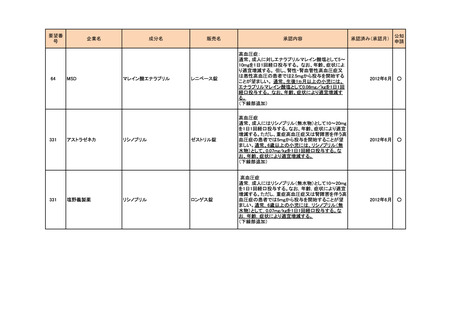
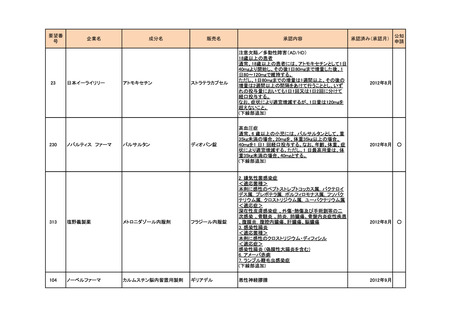
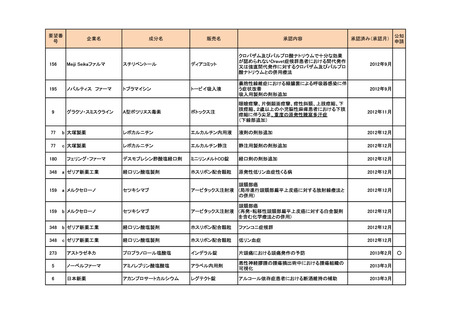
資料5-3 企業から提出された開発工程表の概要等(第I回要望) (16 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00022.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第50回 1/26)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
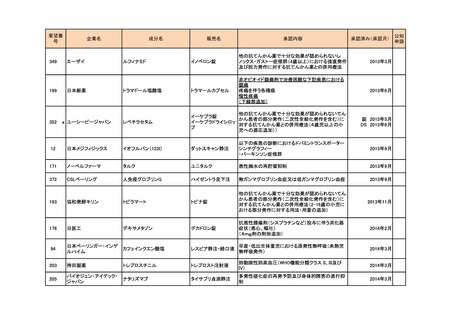
要望番
号
成分名
マリンクロットジャパン(富
インジウム(111In)ペンテトレオ
士フィルムRIファーマが承
チド
認取得)
51
352
企業名
b ユーシービージャパン
販売名
承認内容
承認済み(承認月)
オクトレオスキャン
シンチグラフィによるソマトスタチン受容体を有する原
発性及び転移性の神経内分泌腫瘍の診断
2015年9月
レベチラセタム
イーケプラ錠
6歳以上の特発性全般てんかん患者における強直間
代発作に対する併用療法
2016年2月
2016年7月
81
ノバルティス ファーマ
(ノーベルファーマが承認
取得)
オクスカルバゼピン
オクノベル錠
オクノベル懸濁液
他の抗てんかん薬で十分な効果が認められない小児
の部分発作の併用療法
70
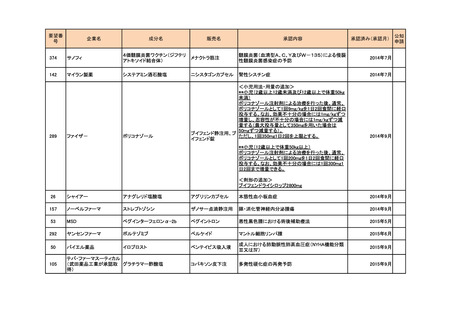
ファイザ-
エプレレノン
セララ錠
慢性心不全
200
日本臓器製薬
トラマドール塩酸塩
182
エーザイ
デニロイキン ジフチトクス(遺伝
レミトロ点滴静注用
子組換え)(JAN)
300µg
denileukin diftitox (INN)
公知
申請
2016年12月
ツートラム錠50mg、
経口徐放剤の剤形追加
ツートラム錠100mg、
慢性疼痛の効能追加
ツートラム錠150mg
再発又は難治性の末梢性T細胞リンパ腫
再発又は難治性の皮膚T細胞性リンパ腫
2020年9月
2021年3月
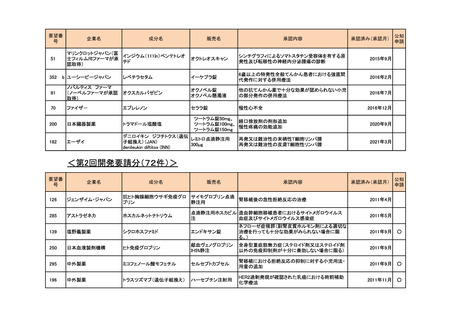
<第2回開発要請分(72件)>
要望番
号
企業名
成分名
販売名
承認内容
承認済み(承認月)
公知
申請
126
ジェンザイム・ジャパン
抗ヒト胸腺細胞ウサギ免疫グロ サイモグロブリン点滴
腎移植後の急性拒絶反応の治療
ブリン
静注用
285
アストラゼネカ
ホスカルネットナトリウム
点滴静注用ホスカビル 造血幹細胞移植患者におけるサイトメガロウイルス
注
血症及びサイトメガロウイルス感染症
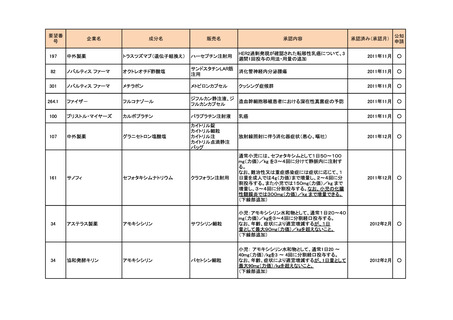
139
塩野義製薬
シクロホスファミド
エンドキサン錠
ネフローゼ症候群(副腎皮質ホルモン剤による適切な
治療を行っても十分な効果がみられない場合に限
る。)
2011年9月
250
日本血液製剤機構
ヒト免疫グロブリン
献血ヴェノグロブリン
IH5%静注
全身型重症筋無力症(ステロイド剤又はステロイド剤
以外の免疫抑制剤が十分に奏効しない場合に限る)
2011年9月
295
中外製薬
ミコフェノール酸モフェチル
セルセプトカプセル
腎移植における拒絶反応の抑制に対する小児用法・
用量の追加
2011年9月
○
196
中外製薬
トラスツズマブ(遺伝子組換え)
ハーセプチン注射用
HER2過剰発現が確認された乳癌における術前補助
化学療法
2011年11月
○
2011年4月
2011年5月
○
号
成分名
マリンクロットジャパン(富
インジウム(111In)ペンテトレオ
士フィルムRIファーマが承
チド
認取得)
51
352
企業名
b ユーシービージャパン
販売名
承認内容
承認済み(承認月)
オクトレオスキャン
シンチグラフィによるソマトスタチン受容体を有する原
発性及び転移性の神経内分泌腫瘍の診断
2015年9月
レベチラセタム
イーケプラ錠
6歳以上の特発性全般てんかん患者における強直間
代発作に対する併用療法
2016年2月
2016年7月
81
ノバルティス ファーマ
(ノーベルファーマが承認
取得)
オクスカルバゼピン
オクノベル錠
オクノベル懸濁液
他の抗てんかん薬で十分な効果が認められない小児
の部分発作の併用療法
70
ファイザ-
エプレレノン
セララ錠
慢性心不全
200
日本臓器製薬
トラマドール塩酸塩
182
エーザイ
デニロイキン ジフチトクス(遺伝
レミトロ点滴静注用
子組換え)(JAN)
300µg
denileukin diftitox (INN)
公知
申請
2016年12月
ツートラム錠50mg、
経口徐放剤の剤形追加
ツートラム錠100mg、
慢性疼痛の効能追加
ツートラム錠150mg
再発又は難治性の末梢性T細胞リンパ腫
再発又は難治性の皮膚T細胞性リンパ腫
2020年9月
2021年3月
<第2回開発要請分(72件)>
要望番
号
企業名
成分名
販売名
承認内容
承認済み(承認月)
公知
申請
126
ジェンザイム・ジャパン
抗ヒト胸腺細胞ウサギ免疫グロ サイモグロブリン点滴
腎移植後の急性拒絶反応の治療
ブリン
静注用
285
アストラゼネカ
ホスカルネットナトリウム
点滴静注用ホスカビル 造血幹細胞移植患者におけるサイトメガロウイルス
注
血症及びサイトメガロウイルス感染症
139
塩野義製薬
シクロホスファミド
エンドキサン錠
ネフローゼ症候群(副腎皮質ホルモン剤による適切な
治療を行っても十分な効果がみられない場合に限
る。)
2011年9月
250
日本血液製剤機構
ヒト免疫グロブリン
献血ヴェノグロブリン
IH5%静注
全身型重症筋無力症(ステロイド剤又はステロイド剤
以外の免疫抑制剤が十分に奏効しない場合に限る)
2011年9月
295
中外製薬
ミコフェノール酸モフェチル
セルセプトカプセル
腎移植における拒絶反応の抑制に対する小児用法・
用量の追加
2011年9月
○
196
中外製薬
トラスツズマブ(遺伝子組換え)
ハーセプチン注射用
HER2過剰発現が確認された乳癌における術前補助
化学療法
2011年11月
○
2011年4月
2011年5月
○