よむ、つかう、まなぶ。
総-6 条件及び期限付き承認を受けた再生医療等製品の保険適用について[774KB] (1 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_57671.html |
| 出典情報 | 中央社会保険医療協議会 総会(第608回 5/14)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
中医協
総-6
7 . 5 . 1 4
条件及び期限付き承認を受けた再生医療等製品の
保険適用について
1.背景
○
有効性評価が十分でない再生医療等製品については、新しい資本主義のグ
ランドデザイン及び実行計画 2024 年改訂版(令和6年6月 21 日)において、
国民皆保険の堅持とイノベーションの推進を両立させつつ、希望する患者が
保険診療の対象となるまで待つことなく利用できるよう、保険診療と保険外
診療の併用を認める保険外併用療養費制度の対象範囲を拡大すること、また、
患者の負担軽減・円滑なアクセスの観点から、民間保険の活用も考慮すること
とされている。
○
令和6年7月3日及び同年8月7日の中医協総会において、条件及び期限
付き承認を受けた再生医療等製品2品目(コラテジェン筋注用4mg及び
ハートシート)の薬価基準又は材料価格基準からの削除について報告した際、
条件及び期限付き承認を受けた再生医療等製品の保険適用のあり方について
次期制度改正に向けて検討が必要である旨の指摘がなされたところ。
2.保険適用が想定される品目の概要
○
今般、令和7年5月 13 日に次の再生医療等製品(本製品)が薬事承認(条
件・期限付き承認)された。
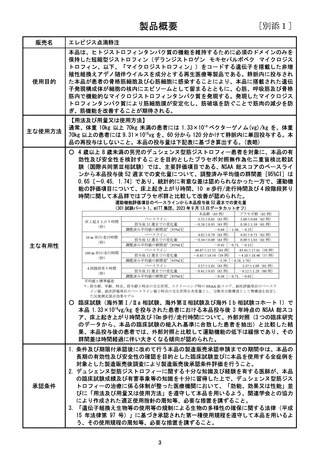
<エレビジス点滴静注>
製造販売業者
:中外製薬株式会社
一 般 的 名 称
:デランジストロゲン モキセパルボベク
適
:デュシェンヌ型筋ジストロフィー
応
症
ただし、以下のいずれも満たす場合に限る
・抗 AAVrh74 抗体が陰性の患者
・歩行可能な患者
・3 歳以上 8 歳未満の患者
用
法
外
国 価 格
:静脈に単回投与。再投与はしないこと。
:
(参考)米国 320 万米国ドル(WAC) (約4億 8,000 万円)
(1米ドル=150 円)
推 定 患 者 数
:上市後 2年度(ピーク時) 100名/年 程度
7年度以降
1
30名/年 程度
総-6
7 . 5 . 1 4
条件及び期限付き承認を受けた再生医療等製品の
保険適用について
1.背景
○
有効性評価が十分でない再生医療等製品については、新しい資本主義のグ
ランドデザイン及び実行計画 2024 年改訂版(令和6年6月 21 日)において、
国民皆保険の堅持とイノベーションの推進を両立させつつ、希望する患者が
保険診療の対象となるまで待つことなく利用できるよう、保険診療と保険外
診療の併用を認める保険外併用療養費制度の対象範囲を拡大すること、また、
患者の負担軽減・円滑なアクセスの観点から、民間保険の活用も考慮すること
とされている。
○
令和6年7月3日及び同年8月7日の中医協総会において、条件及び期限
付き承認を受けた再生医療等製品2品目(コラテジェン筋注用4mg及び
ハートシート)の薬価基準又は材料価格基準からの削除について報告した際、
条件及び期限付き承認を受けた再生医療等製品の保険適用のあり方について
次期制度改正に向けて検討が必要である旨の指摘がなされたところ。
2.保険適用が想定される品目の概要
○
今般、令和7年5月 13 日に次の再生医療等製品(本製品)が薬事承認(条
件・期限付き承認)された。
<エレビジス点滴静注>
製造販売業者
:中外製薬株式会社
一 般 的 名 称
:デランジストロゲン モキセパルボベク
適
:デュシェンヌ型筋ジストロフィー
応
症
ただし、以下のいずれも満たす場合に限る
・抗 AAVrh74 抗体が陰性の患者
・歩行可能な患者
・3 歳以上 8 歳未満の患者
用
法
外
国 価 格
:静脈に単回投与。再投与はしないこと。
:
(参考)米国 320 万米国ドル(WAC) (約4億 8,000 万円)
(1米ドル=150 円)
推 定 患 者 数
:上市後 2年度(ピーク時) 100名/年 程度
7年度以降
1
30名/年 程度