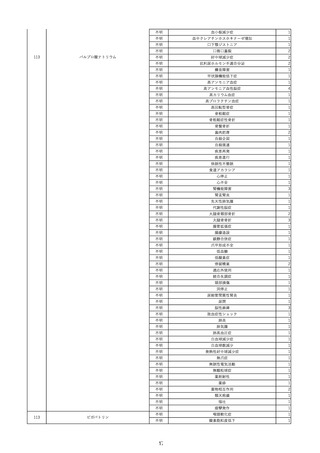
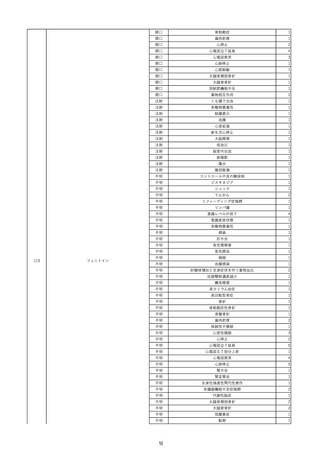
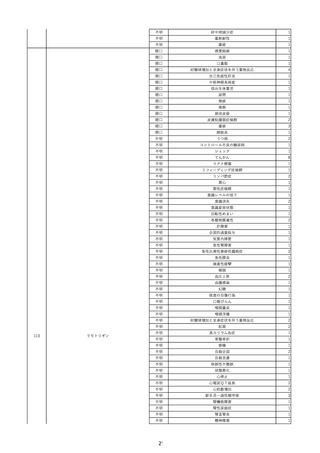
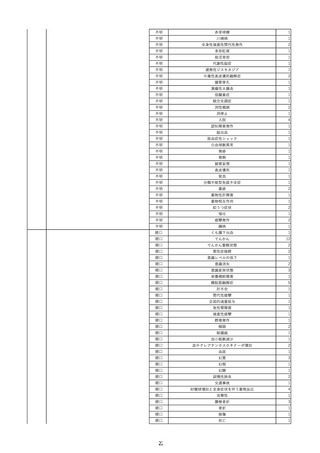
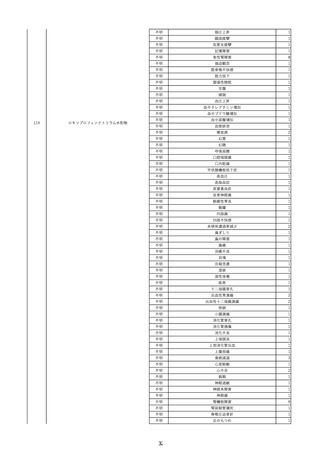
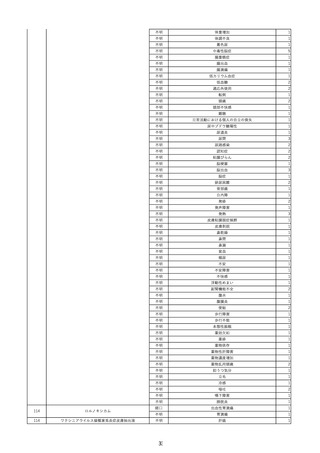
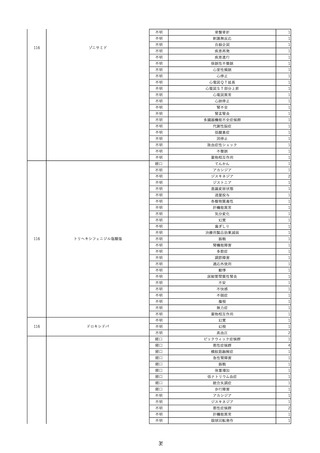
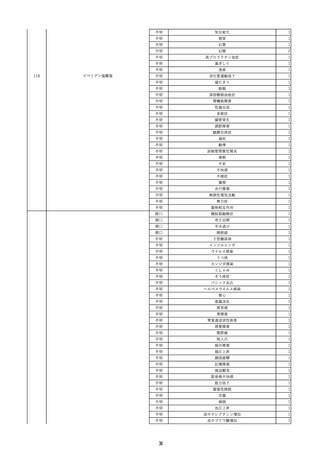
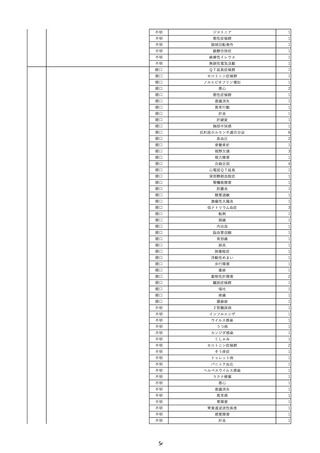
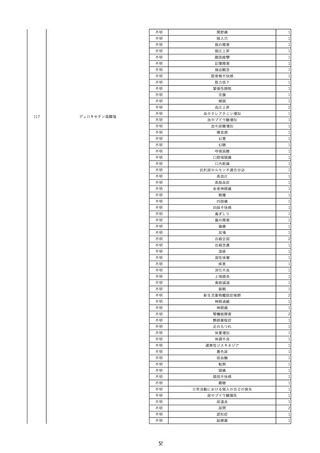
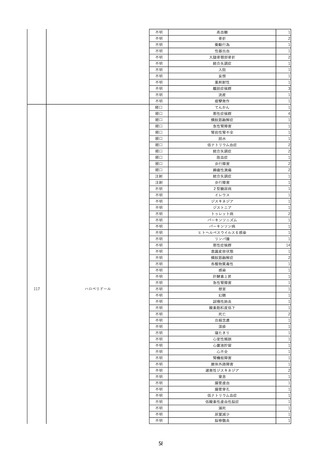
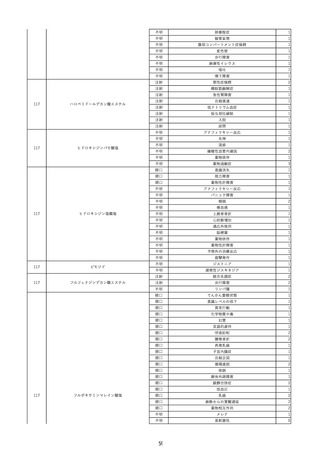
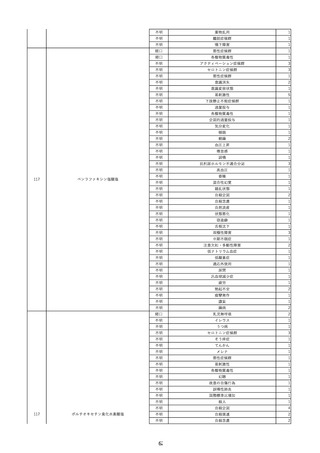
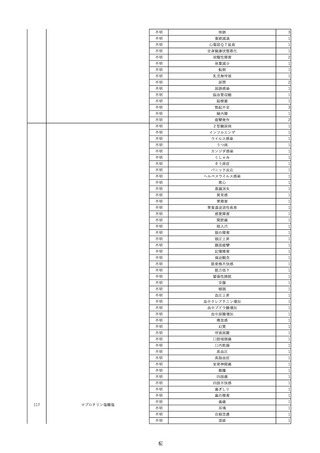
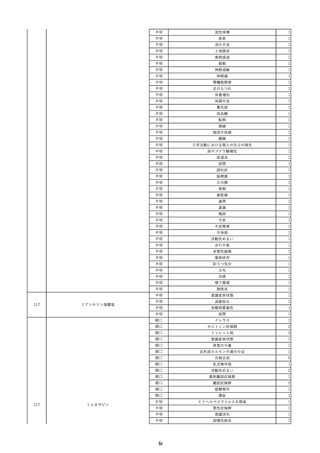
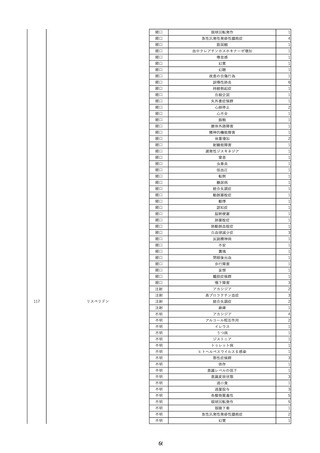
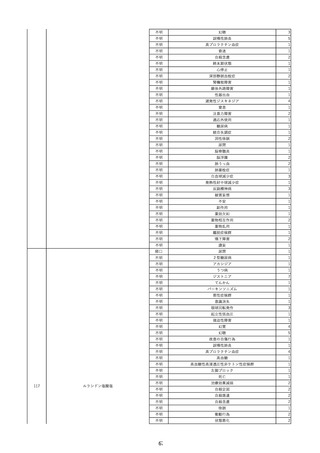
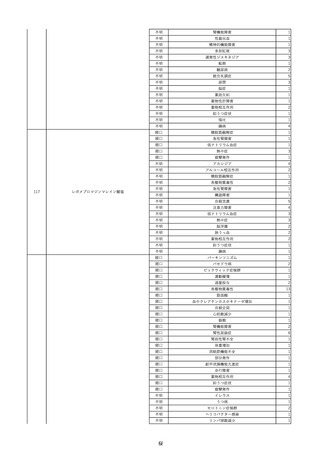
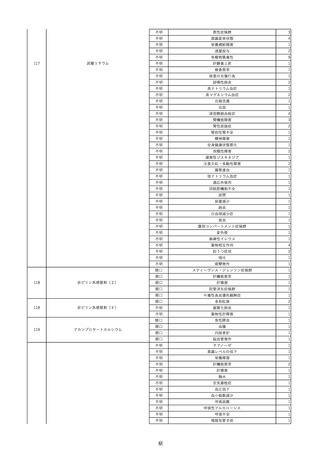
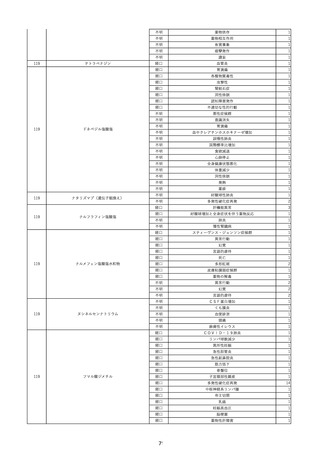
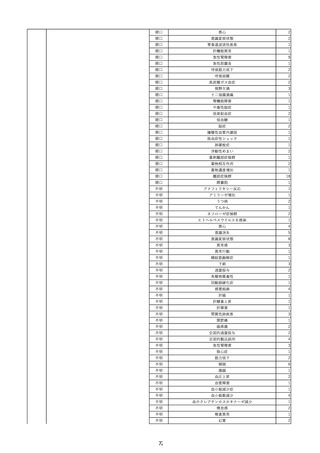
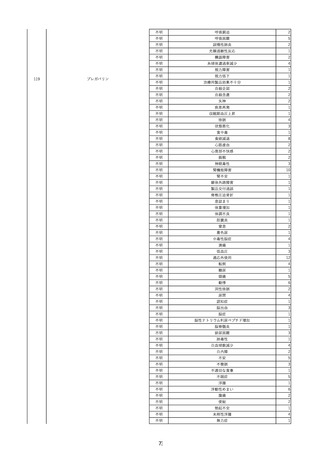
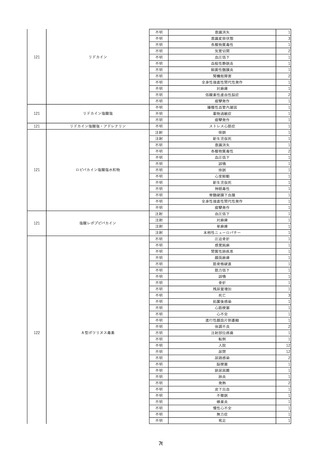
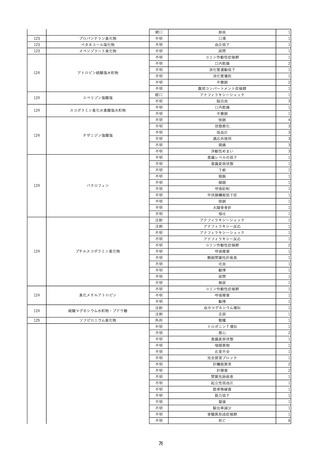
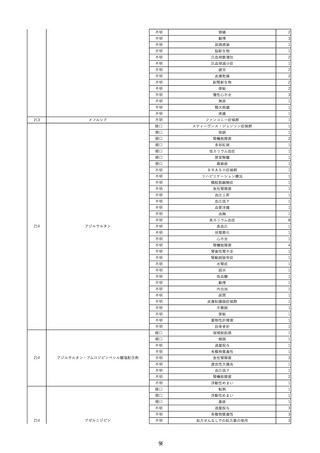
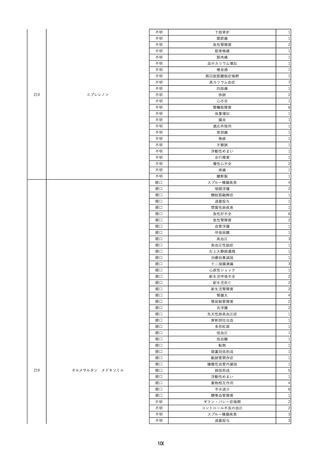
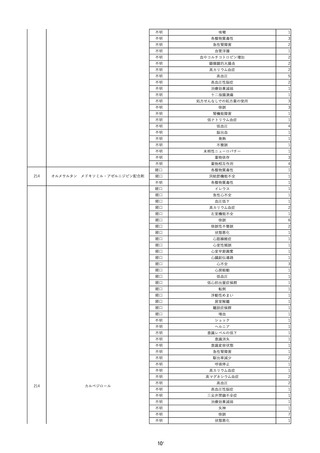
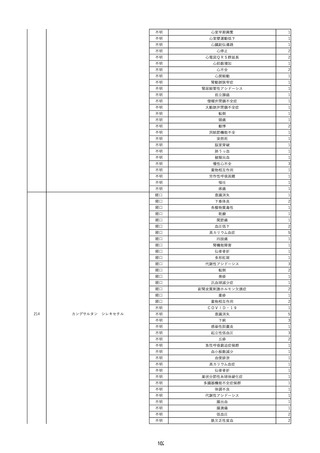
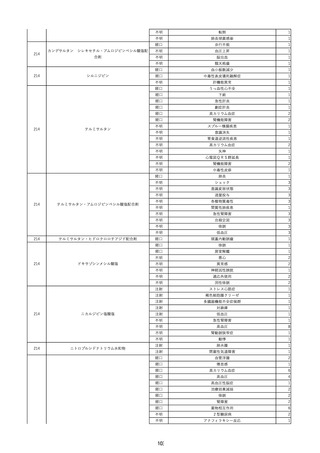
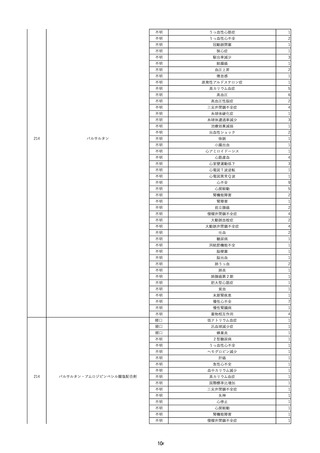
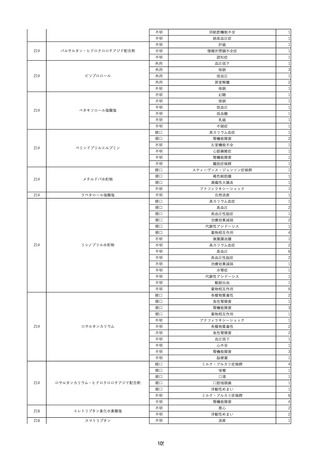
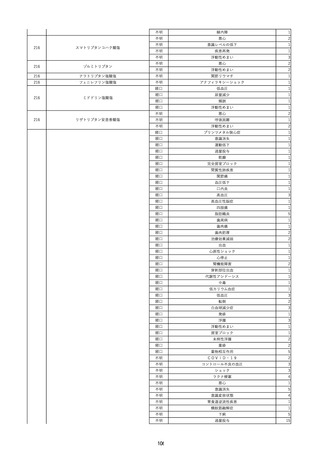
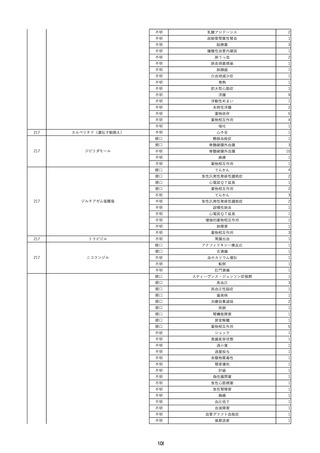
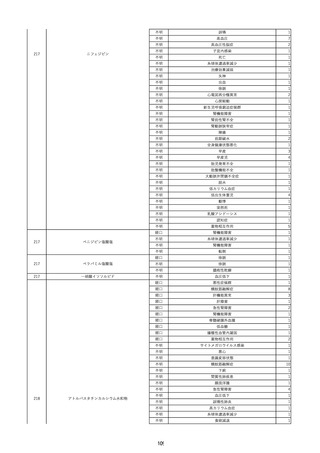
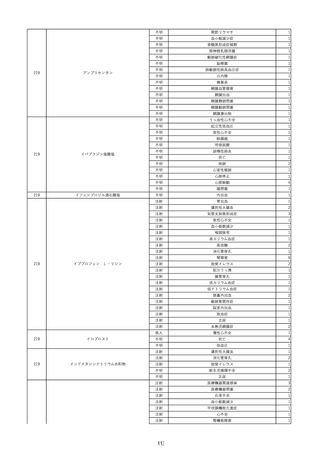
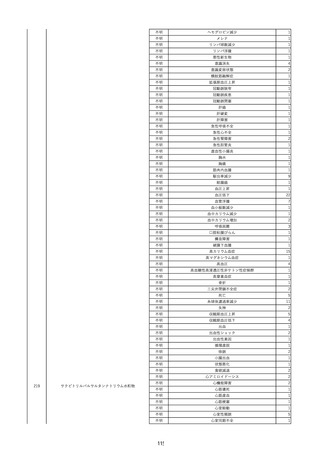
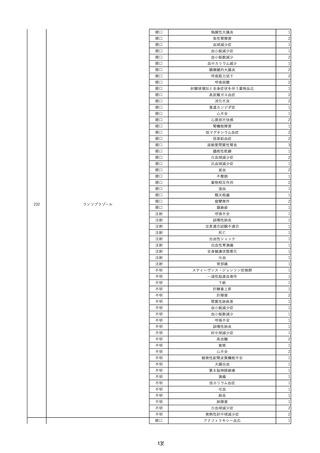
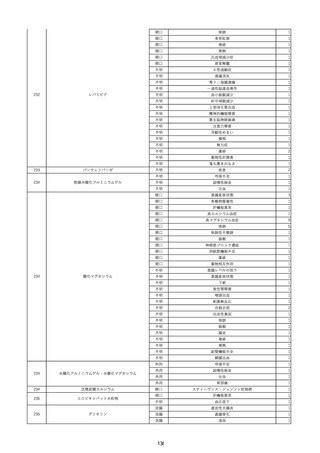
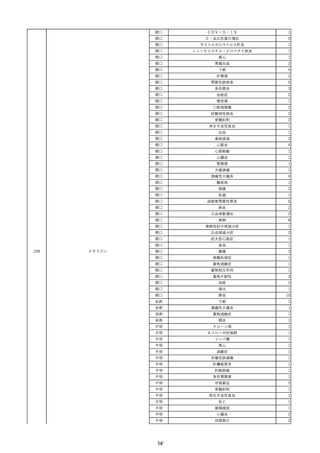
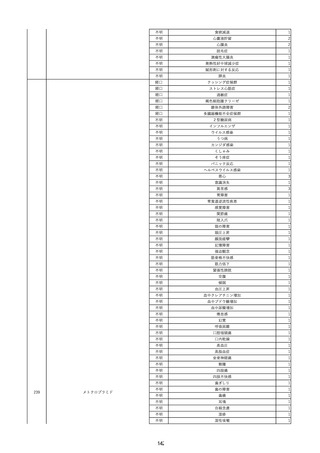
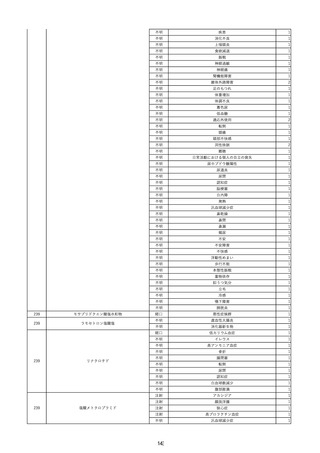
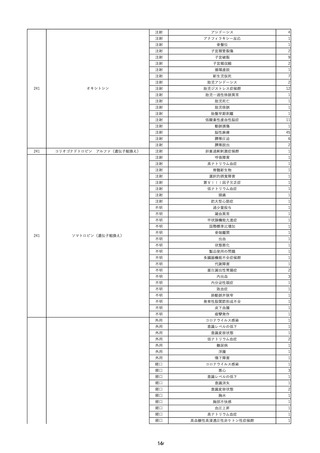
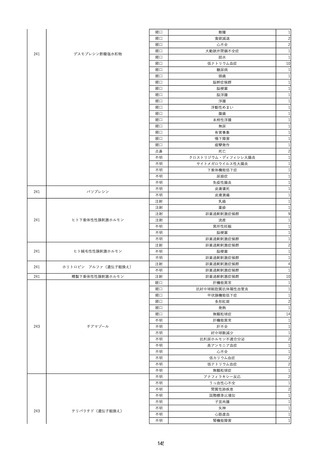
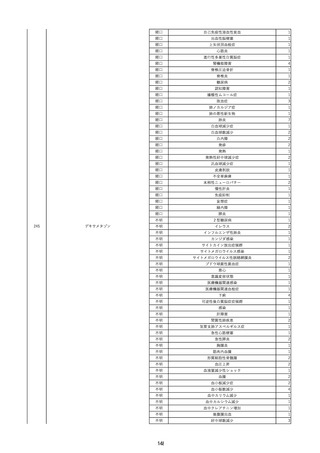
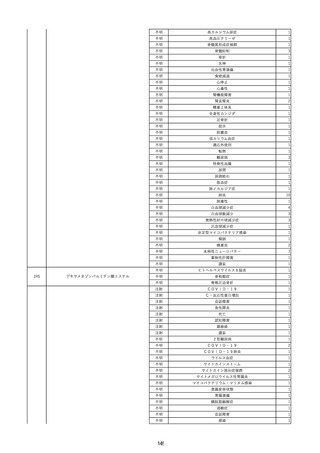
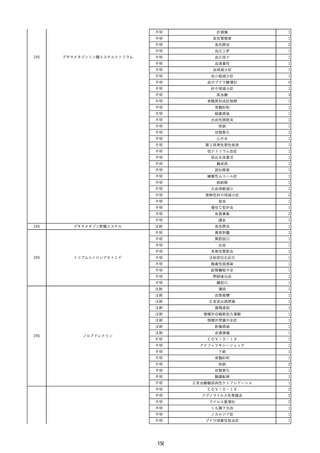
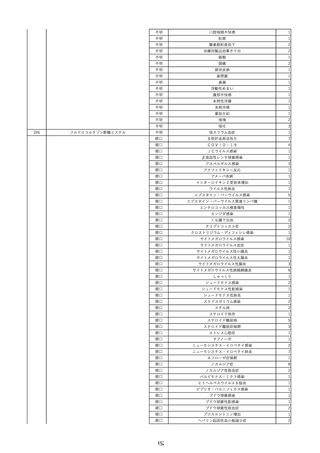
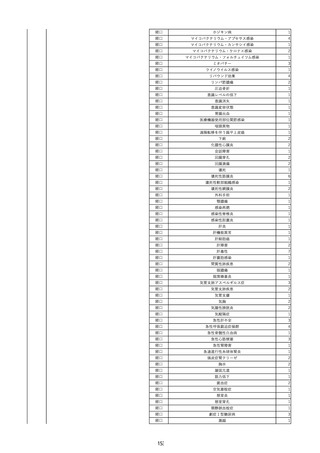
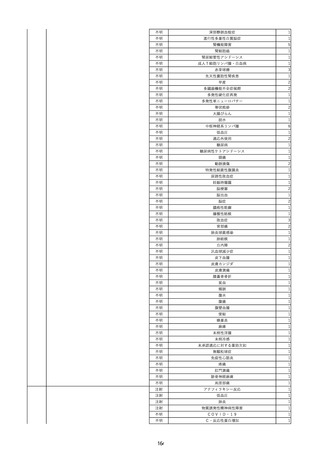
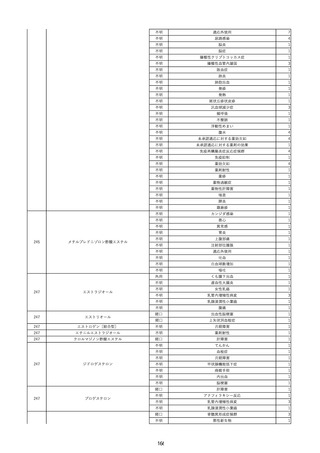
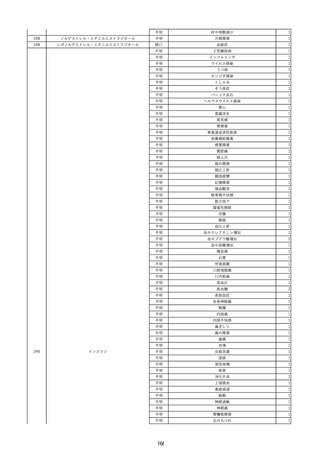
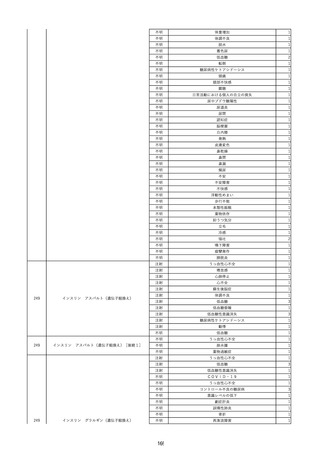
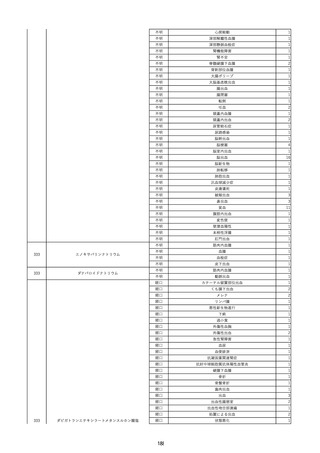
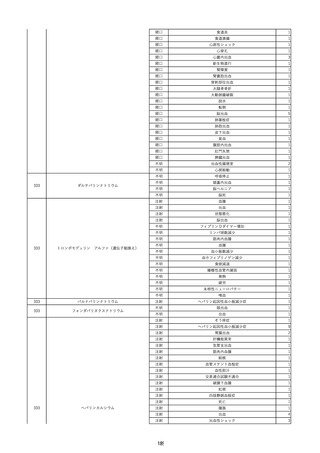
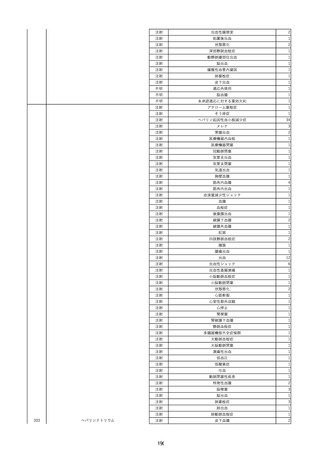
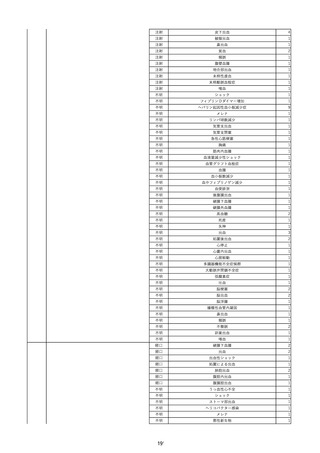
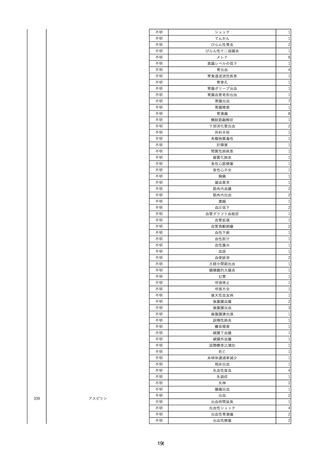
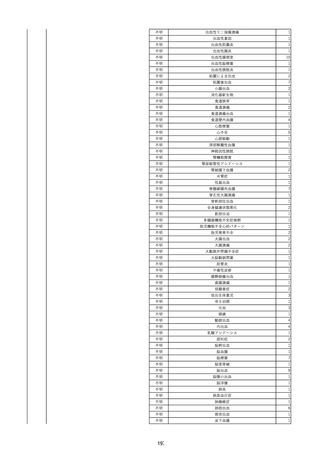
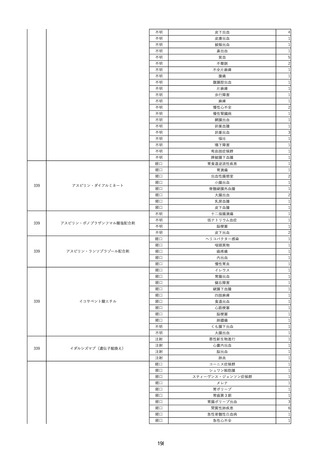
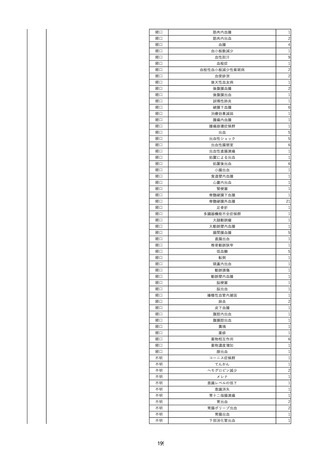
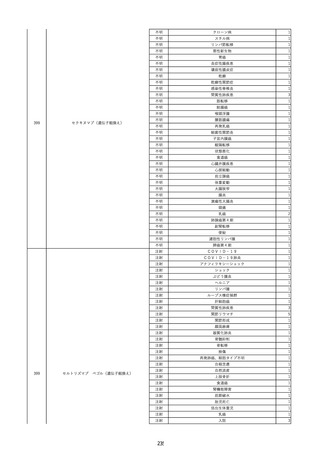
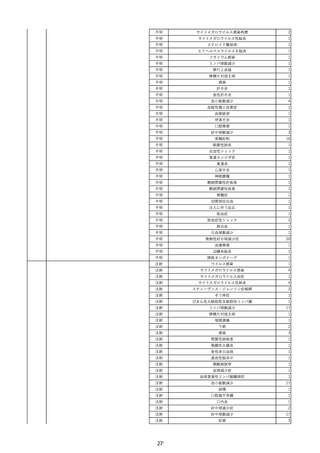
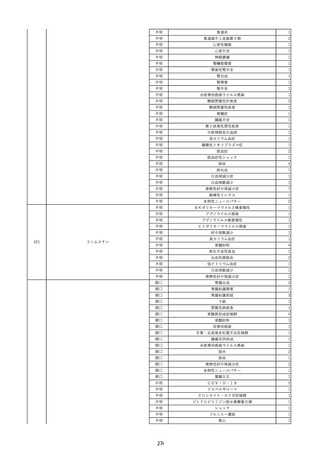
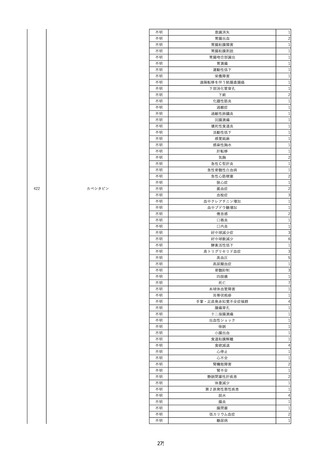
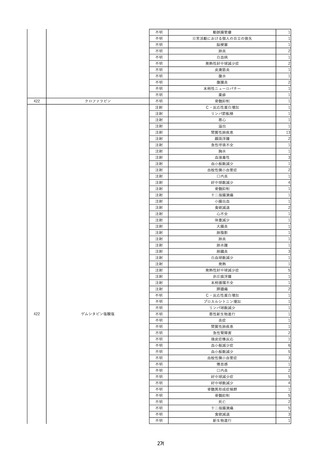
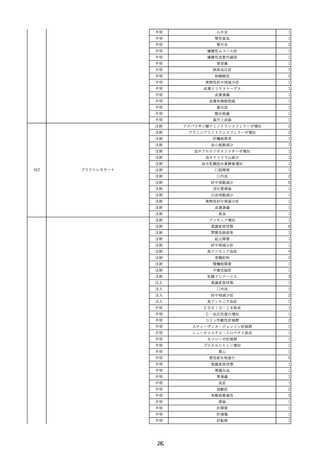
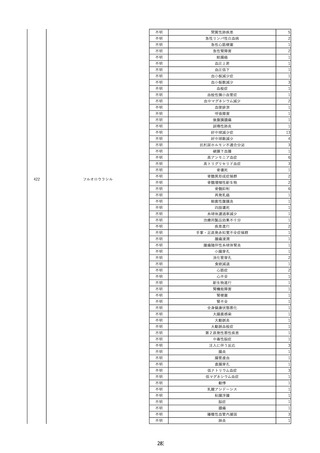
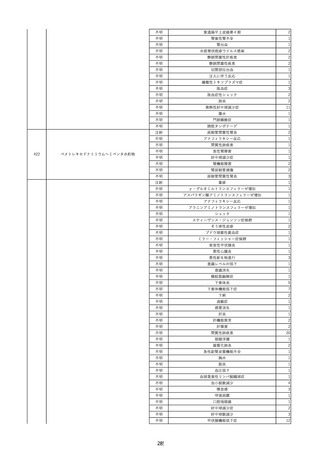
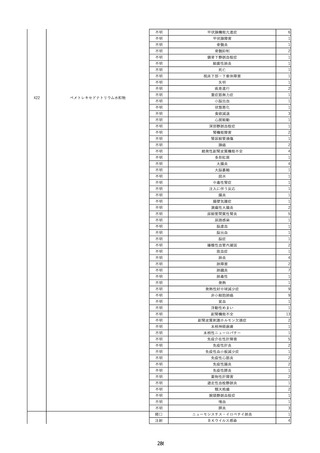
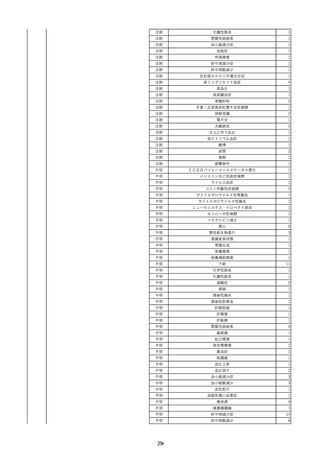
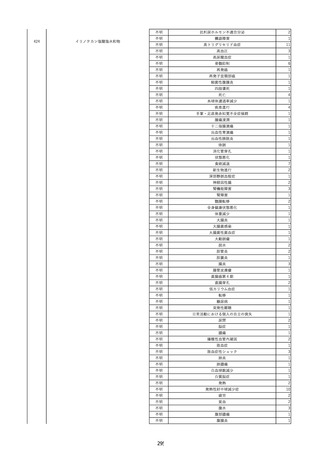
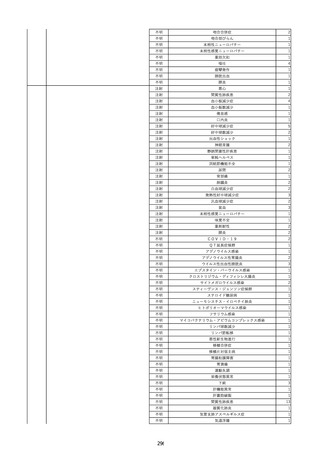
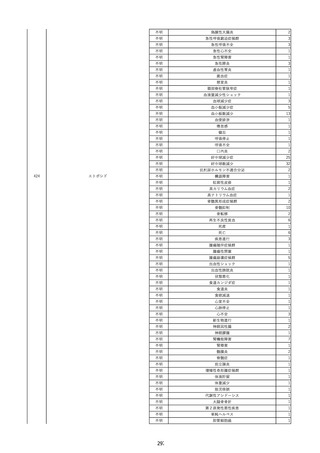
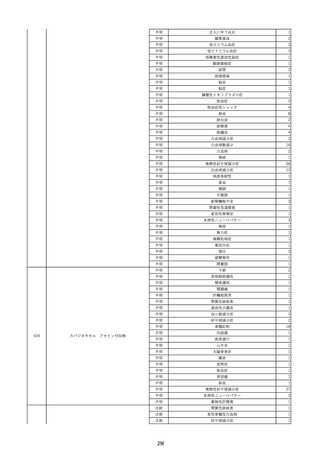
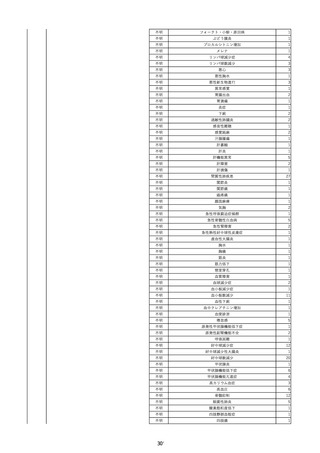
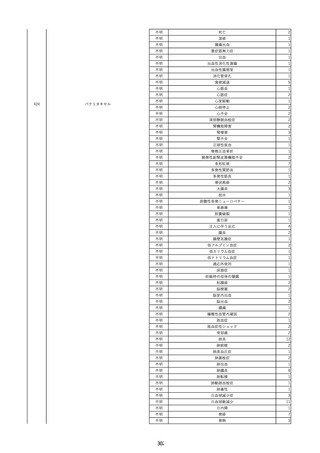
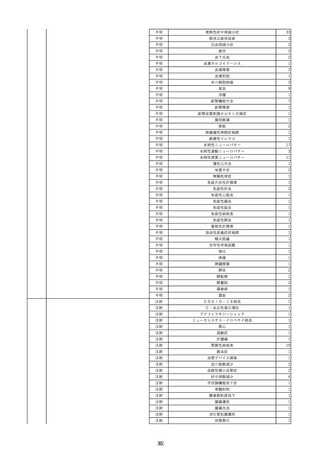
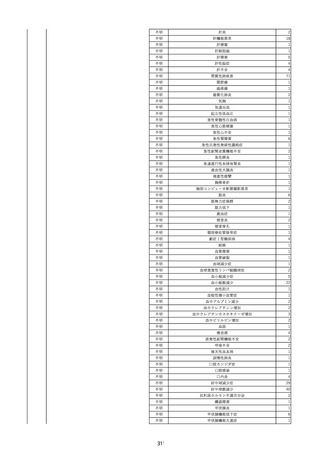
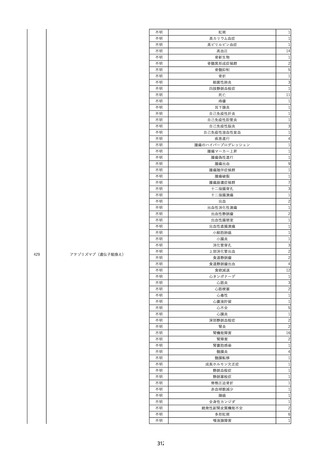
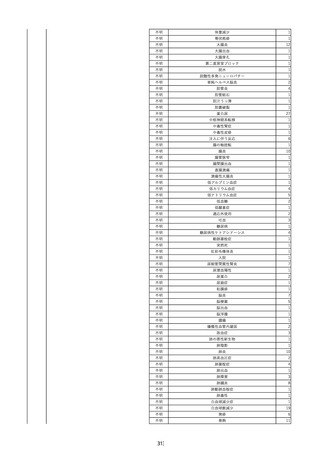
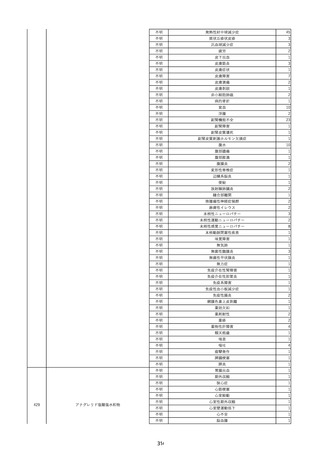
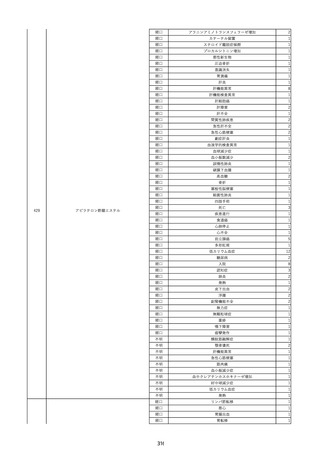
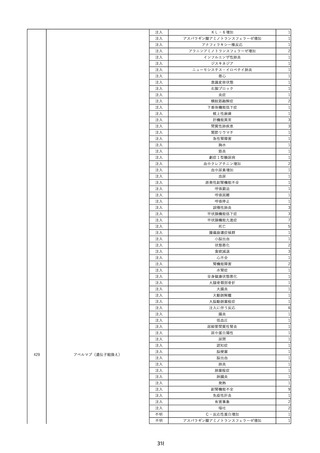
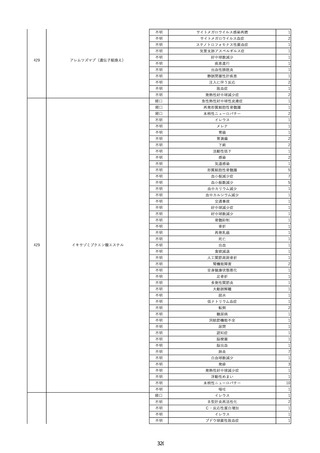
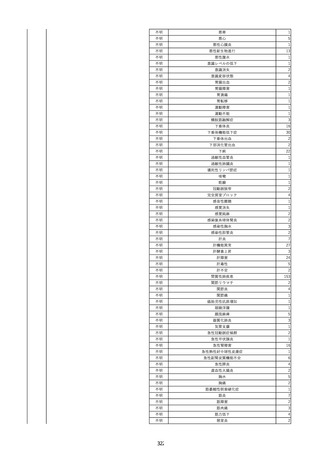
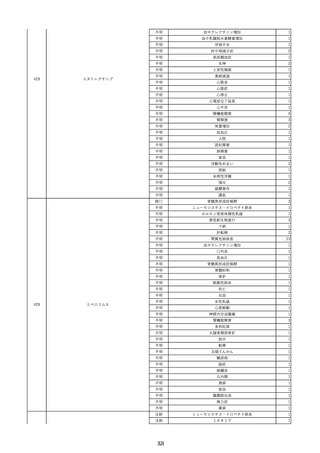
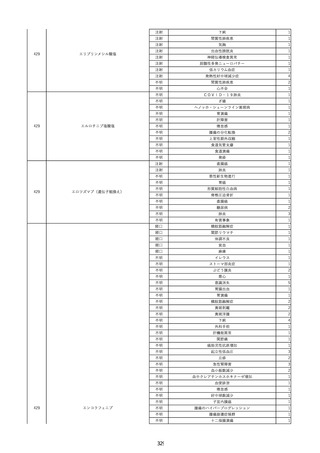
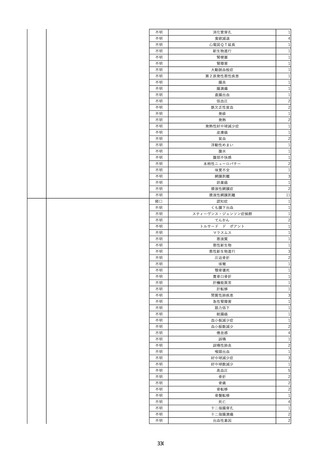
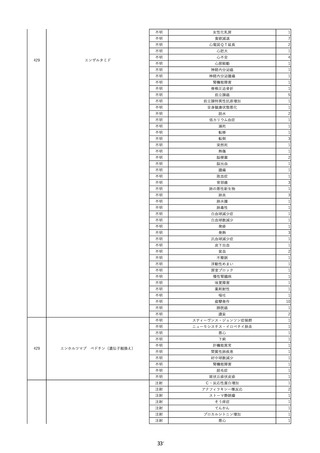
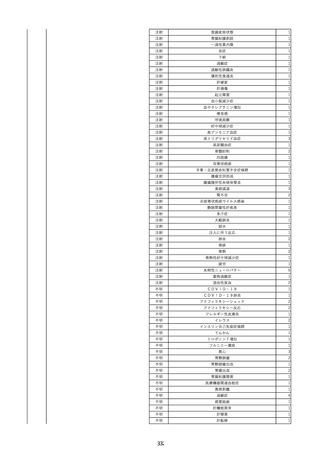
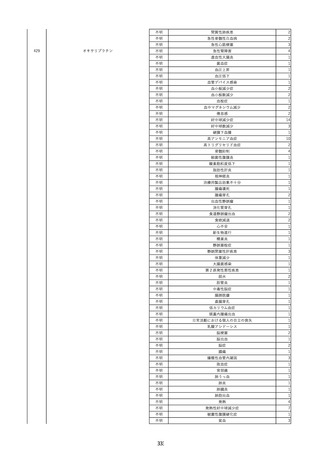
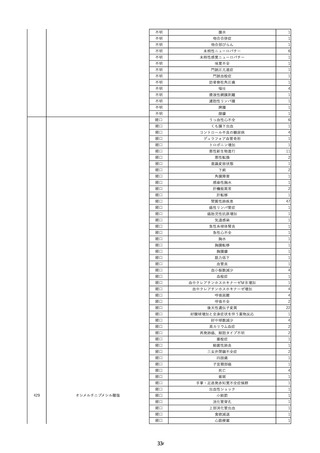
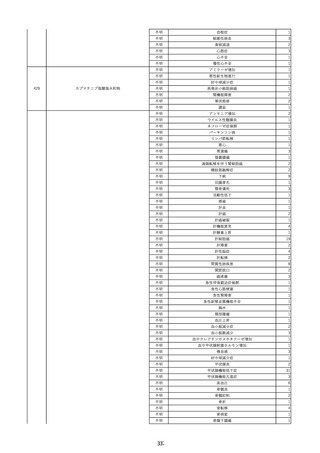
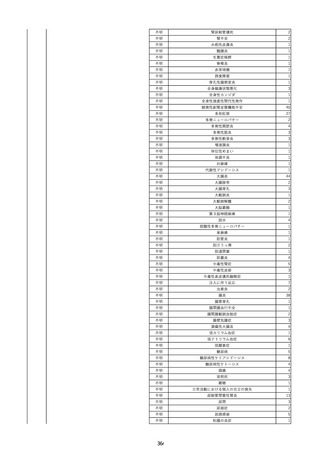
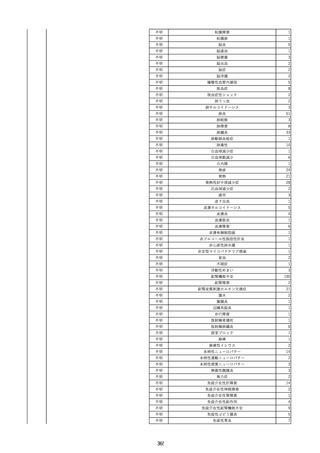
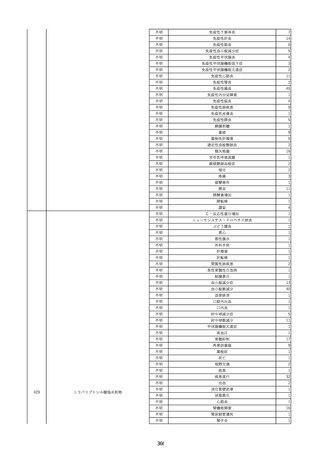
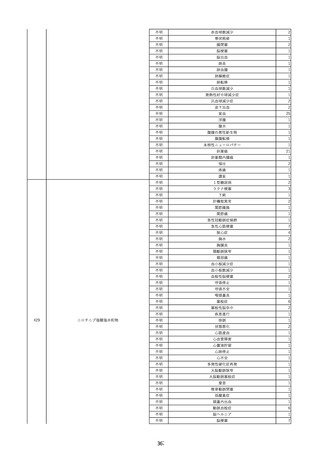
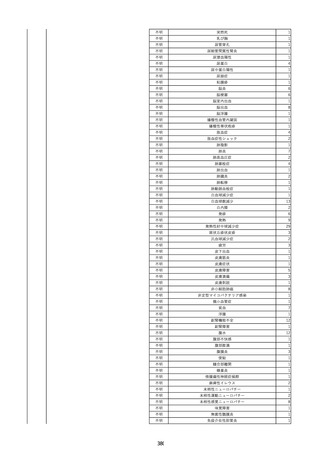
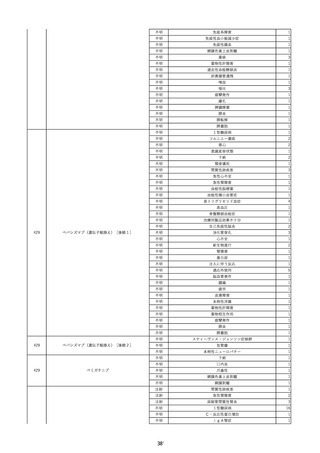
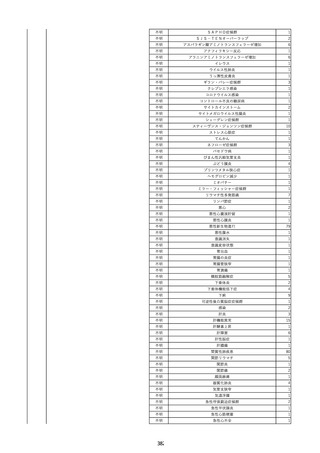
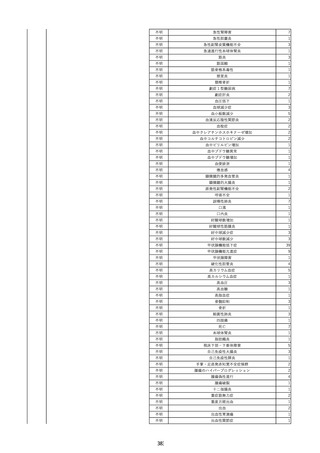
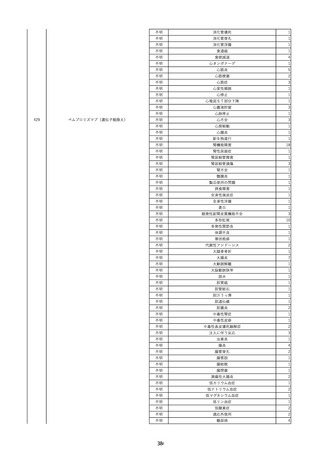
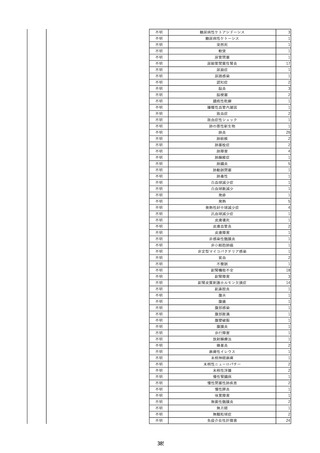
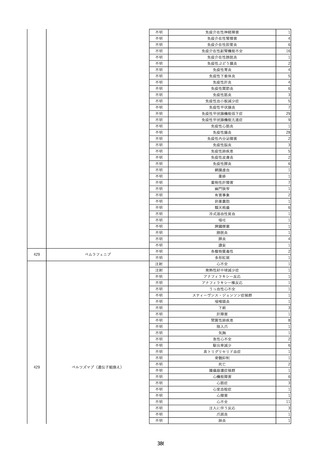
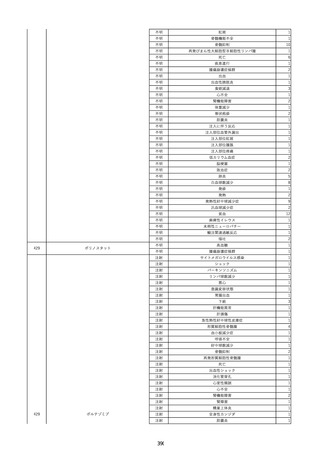
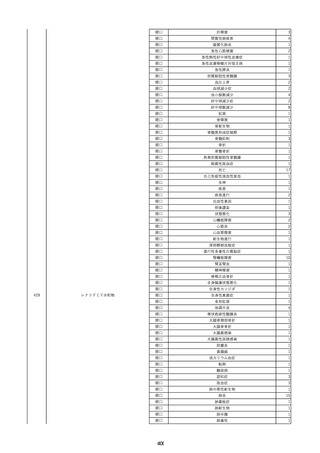
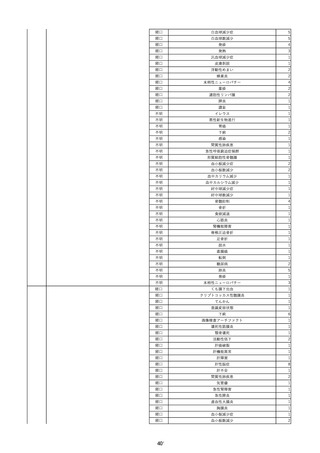
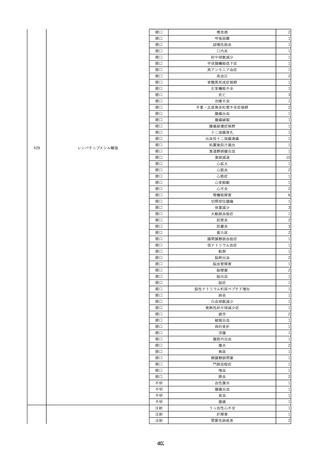
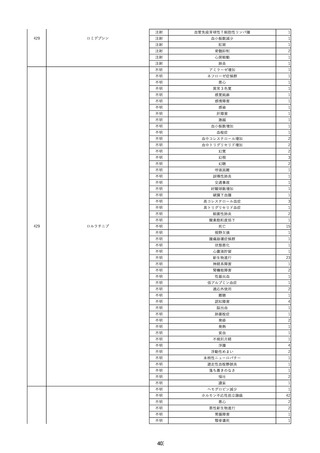
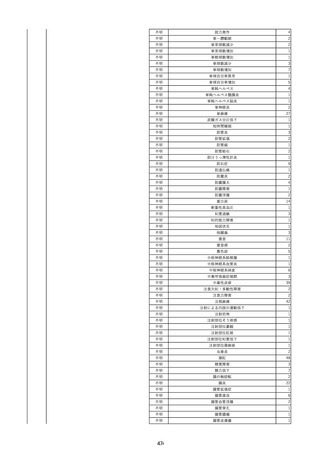
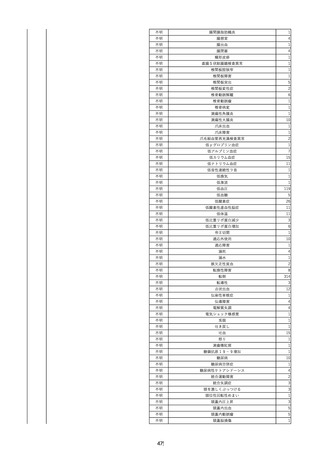
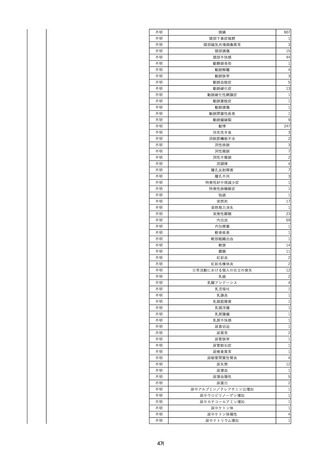
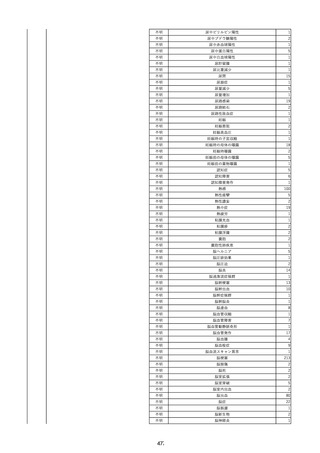
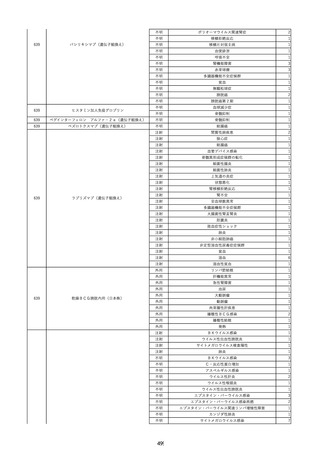
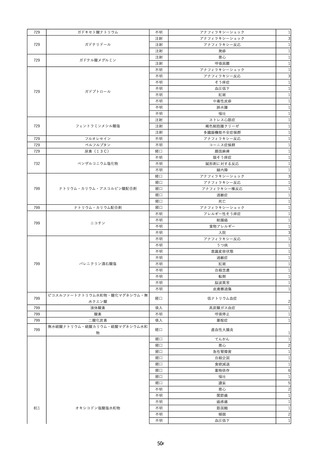
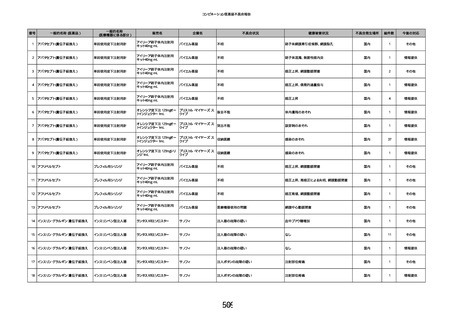
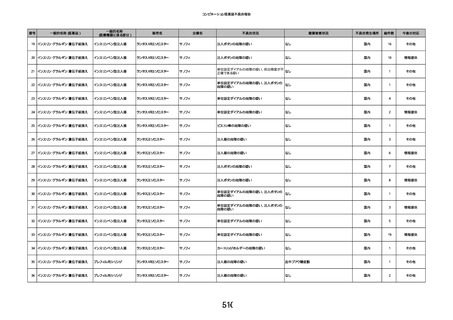
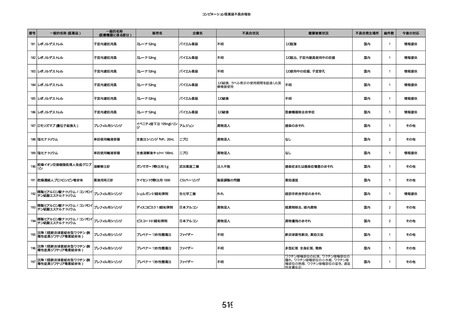
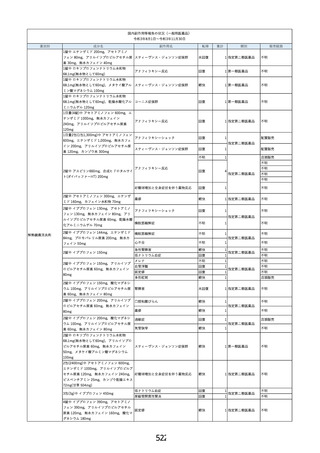
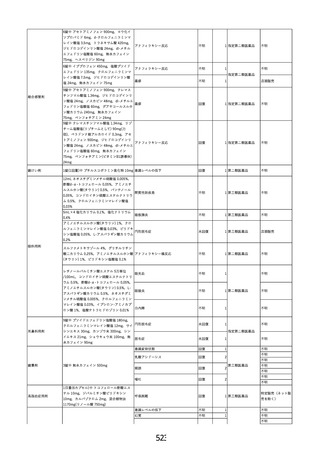
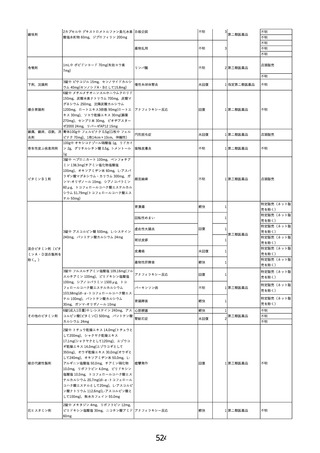
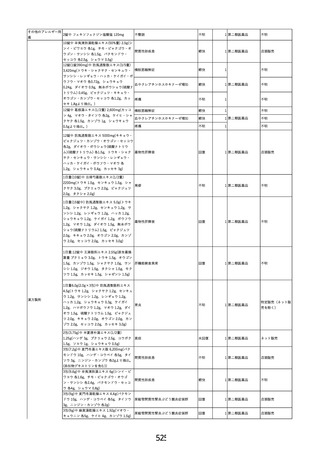
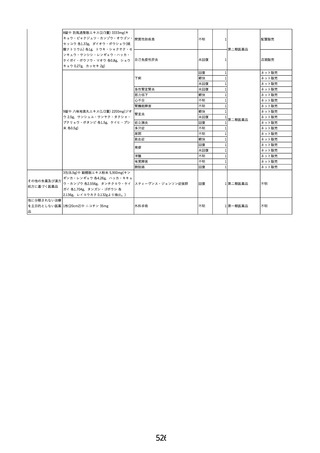
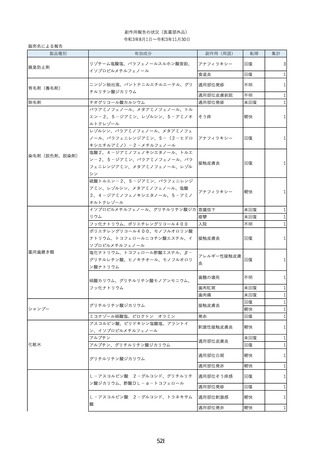
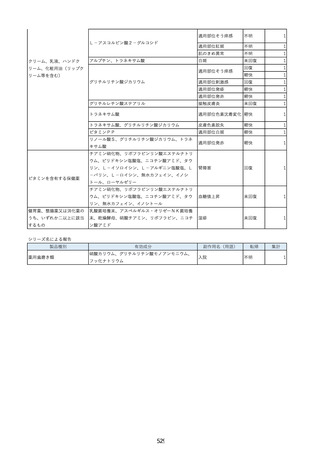
資料2-2 製造販売業者からの国内副作用等報告の状況 (536 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_24331.html |
| 出典情報 | 薬事・食品衛生審議会 薬事分科会医薬品等安全対策部会(令和3年度 第3回 3/11)《厚生労働省》 |
ページ画像
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
報告受領日
販売名(一般名)
患者性
年代
別
原疾患(簡略名)
感染症名
投与年月
投与前検査(年月)
企業投与前
検査
投与後検査(年月)
企業投与後
検査
受血者個別NAT
献血者個別NAT
備考
1本目輸血開始。
1本目輸血開始47分後 口唇浮腫、蕁麻疹出現。抗ヒスタミン薬+ステロイド投与。
アレルギー症状消失。
1本目輸血開始2時間27分後 輸血再開。
1本目輸血再開1時間25分後 1本目輸血終了。2本目輸血開始。
2本目輸血開始1時間41分後 BT 36.5℃、BP 117/80 mmHg、HR 71 /min、SpO2 98%。
2本目輸血開始2時間後 2本目輸血終了。
以降、アレルギー症状再燃なし。
13
2021/10/28
照射濃厚血小板-LR(人血小板濃厚
女
液(放射線照射))
50
その他の腫瘍
その他の疾患
細菌感染
21/10
輸血翌日 BT 39.7℃。発熱性好中球減少症としてメロペネム水和物投与開始。フィルグラスチム(遺伝子組換え)継続。
ロキソプロフェンナトリウム水和物+アセトアミノフェン投与。
体温測定7時間20分後 喀血あり。カルバゾクロムスルホン酸ナトリウム水和物+トラネキサム酸投与。
体温測定7時間59分後 BT 36.4℃。
NHF開始。
輸血開始6時間36分前 BT 36.5℃、BP
123/82 mmHg、HR 72 /min、SpO2 98%。 血液培養検査実施。
輸血開始24分前 BT 36.7℃、BP 109/68
輸血2日後 血小板減少(33,000 /µL)、気道出血持続あり。挿管。
mmHg、HR 67 /min、SpO2 96%。
挿管4時間15分後 頻脈傾向。ベラパミル塩酸塩開始。
挿管4時間23分後 BT 36.0℃、BP 75/43 mmHg、HR 145 /min、SpO2 94%(O2 NHF 30 L/min)。
挿管5時間10分後 2本輸血開始。
輸血開始2時間24分後 BT 36.9℃、BP 112/95 mmHg、HR 114 /min、SpO2 93%(FiO2 90%)。
輸血開始3時間55分後 2本輸血終了。アレルギー症状発現なく、呼吸状態も悪化なし。
輸血終了1時間50分後 BP、HR低下あり。自発呼吸減弱。
心臓マッサージで一時心拍再開。
輸血終了2時間10分後 BP 38/12 mmHg。
輸血終了2時間50分後 脈拍触知不能。蘇生再開も戻らず。
当該輸血用血液の使用済みバッグ内残渣にて細菌培養試験及びエンドトキ
シン試験を実施。
細菌培養試験:陰性。
エンドトキシン試験:基準値以下。
-
当該輸血用血液の残余にて細菌培養試験を実施し、陰性。
-
輸血3日後 胸腺腫による急性肺障害にて、患者死亡。剖検なし、輸血と死亡との関連性なし。
輸血4日後 輸血翌日実施の患者血液培養検査より、Pseudomonas aeruginosa を同定。
輸血開始35分後 膨疹出現。
輸血開始55分後 悪寒あり。酸素化不良出現。BT 36.9℃、BP 129/88 mmHg、HR 94 /min、SpO2 92%(O2 1 L/min)。
輸血開始1時間41分後 BT 38.2℃、BP 129/88 mmHg、HR 94 /min、SpO2 92%(O2 1 L/min)。
輸血開始4時間12分後 セフェピム塩酸塩水和物投与。
血液培養検査実施。
14
2021/11/1
照射濃厚血小板-LR(人血小板濃厚
女
液(放射線照射))
70 血液腫瘍
細菌感染
21/10
輸血開始2分前 BT 36.9℃、BP 104/74
mmHg、HR 78 /min、SpO2 97%。
輸血翌日 全身に癒合性の淡い紅斑出現。セフェピム塩酸塩水和物による薬疹の可能性を考え、メロペネム水和物に変更。
-
輸血2日後 BT 37.1℃、BP 93/48 mmHg、HR 89 /min、SpO2 94%。
解熱。
輸血5日後 輸血日実施の患者血液培養検査は陰性。
15
16
2021/11/4
新鮮凍結血漿-LR480(新鮮凍結人
男
血漿)
照射赤血球液-LR(人赤血球液(放
射線照射))
新鮮凍結血漿-LR(新鮮凍結人血
男
2021/11/22
漿)
照射濃厚血小板-LR(人血小板濃厚
液(放射線照射))
照射赤血球濃厚液-LR(人赤血球液
(放射線照射))
男
新鮮凍結血漿-LR(新鮮凍結人血
漿)
17
2021/11/26
18
2021/11/30 赤血球液-LR(人赤血球液)
女
70 腎・泌尿器系疾患
E型肝炎
21/07-21/08
80 循環器疾患
B型肝炎
21/05
-
HEV-IgA-Ab(+)
(21/10)
HBsAg(-)
(21/05)
HBsAg(+)
(21/10)
HBsAb(-)、HBcAb(-)
(21/05)
HBV-DNA(+)、HBsAg(+)、HBsAb(+)、HBcAb(+)
(21/11)
HCV-RNA(+)、HCV-Ab(+)
(21/11)
30 肝・胆・膵疾患
C型肝炎
12/01
HCV-Ab(-)
(12/01)
70 血液腫瘍
細菌感染
21/11
輸血前 BT 36.1℃。
輸血開始2時間40分後 BT 39.4℃。
血液培養検査実施。
HEV-RNA(-)、HEV-IgA-Ab(-)、 HEV-RNA(-)、HEV-IgA-Ab(+)、
陰性(輸血前)
HEV-IgM-Ab(-)、HEV-IgG-Ab(+) HEV-IgM-Ab(-)、HEV-IgG-Ab(+)
陰性(輸血後)
(21/10)
(21/07)
80名の個別NATはHEV-RNA
(-)
調査中
調査中
調査中
調査中
調査中
調査中
調査中
調査中
-
-
調査中
輸血日実施の患者血液培養検査より、Bacillus cereus を同定。
19
2021/9/21
コンコエイト-HT(乾燥濃縮人血液凝
男
固第8因子)
70 血液疾患
C型肝炎
-
-
血友病Aに対する非加熱血液凝固第Ⅷ因子製剤によりC型肝炎に感染した。
-
-
-
-
投与された非加熱血液凝固第Ⅷ因子製剤は過去の血液製剤であると考え
られ、現在の製剤による感染症報告ではない。
20
2021/10/13
コンコエイト-HT(乾燥濃縮人血液凝
男
固第8因子)
40 血液疾患
HIV感染
C型肝炎
-
-
血友病Aに対する過去の血液製剤使用によりHIV及びC型肝炎に感染した。
-
-
-
-
投与された血液凝固因子製剤は過去の血液製剤であると考えられ、現在の
製剤による感染症報告ではない。
21
エイフスチラ(ロノクトコグ アルファ
2021/10/22
(遺伝子組換え))
22
23
講演会の講演スライドで確認された症例。
当該製品の製造工程には、ウイルス除去ろ過等のウイルス除去・不活化工
程が組み込まれている。
また、製造工程におけるウイルス除去・不活化を確認するためにモデルウイ
ルスを用いたウイルスバリデーション試験を行い、一定のウイルスクリアラン
ス能を有することを確認している。
男
40 血液疾患
HIV感染
21/08
-
不明日、HIVに感染した。
-
-
-
-
2021/10/25
コンコエイト-HT(乾燥濃縮人血液凝
男
固第8因子)
60 血液疾患
HIV感染
C型肝炎
-
-
血友病Aに対する血液凝固因子製剤によりHIV及びC型肝炎に感染した。
-
-
-
-
投与された血液凝固因子製剤は過去の血液製剤であると考えられ、現在の
製剤による感染症報告ではない。
2021/11/9
コンコエイト-HT(乾燥濃縮人血液凝
男
固第8因子)
40 血液疾患
HIV感染
C型肝炎
-
-
血友病Aに対する非加熱の血液凝固因子製剤によりHIV及びC型肝炎に感染した。
-
-
-
-
投与された非加熱の血液凝固因子製剤は過去の血液凝固因子製剤である
と考えられ、現在の製剤による感染症報告ではない。
3
535