よむ、つかう、まなぶ。
別紙1○患者申出療養に係る新規技術の科学的評価等について (11 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000203222_00027.html |
| 出典情報 | 患者申出療養評価会議(第44回 10/19)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
様式第3号
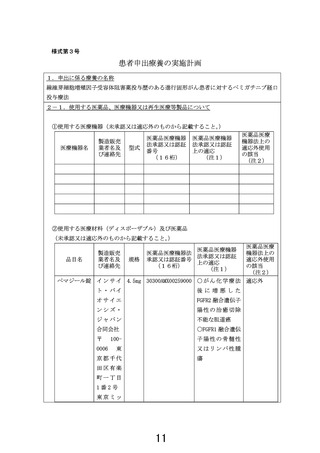
患者申出療養の実施計画
1.申出に係る療養の名称
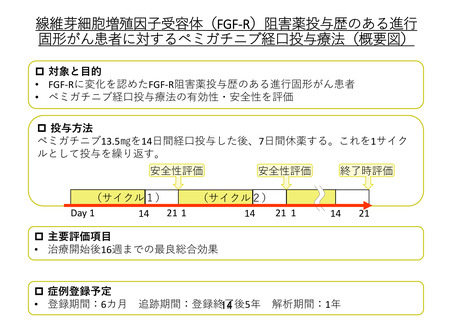
線維芽細胞増殖因子受容体阻害薬投与歴のある進行固形がん患者に対するペミガチニブ経口
投与療法
2-1.使用する医薬品、医療機器又は再生医療等製品について
①使用する医療機器(未承認又は適応外のものから記載すること。
)
医療機器名
製造販売
業者名及
び連絡先
型式
医薬品医療機器
法承認又は認証
番号
(16桁)
医薬品医療機器
法承認又は認証
上の適応
(注1)
医薬品医療
機器法上の
適応外使用
の該当
(注2)
②使用する医療材料(ディスポーザブル)及び医薬品
(未承認又は適応外のものから記載すること。
)
医薬品医療
機器法上の
品目名
規格
適応外使用
の該当
(注2)
ペマジール錠 イ ン サ イ 4.5mg 30300AMX00259000 ○ が ん 化 学 療 法 適応外
製造販売
業者名及
び連絡先
医薬品医療機器
医薬品医療機器法
法承認又は認証
承認又は認証番号
上の適応
(16桁)
(注1)
ト・バイ
後に増悪した
オサイエ
FGFR2 融合遺伝子
ンシズ・
陽性の治癒切除
ジャパン
不能な胆道癌
合同会社
○FGFR1 融合遺伝
〒
100-
子陽性の骨髄性
0006
東
又はリンパ性腫
京都千代
瘍
田区有楽
町一丁目
1番2号
東京ミッ
11
患者申出療養の実施計画
1.申出に係る療養の名称
線維芽細胞増殖因子受容体阻害薬投与歴のある進行固形がん患者に対するペミガチニブ経口
投与療法
2-1.使用する医薬品、医療機器又は再生医療等製品について
①使用する医療機器(未承認又は適応外のものから記載すること。
)
医療機器名
製造販売
業者名及
び連絡先
型式
医薬品医療機器
法承認又は認証
番号
(16桁)
医薬品医療機器
法承認又は認証
上の適応
(注1)
医薬品医療
機器法上の
適応外使用
の該当
(注2)
②使用する医療材料(ディスポーザブル)及び医薬品
(未承認又は適応外のものから記載すること。
)
医薬品医療
機器法上の
品目名
規格
適応外使用
の該当
(注2)
ペマジール錠 イ ン サ イ 4.5mg 30300AMX00259000 ○ が ん 化 学 療 法 適応外
製造販売
業者名及
び連絡先
医薬品医療機器
医薬品医療機器法
法承認又は認証
承認又は認証番号
上の適応
(16桁)
(注1)
ト・バイ
後に増悪した
オサイエ
FGFR2 融合遺伝子
ンシズ・
陽性の治癒切除
ジャパン
不能な胆道癌
合同会社
○FGFR1 融合遺伝
〒
100-
子陽性の骨髄性
0006
東
又はリンパ性腫
京都千代
瘍
田区有楽
町一丁目
1番2号
東京ミッ
11