よむ、つかう、まなぶ。
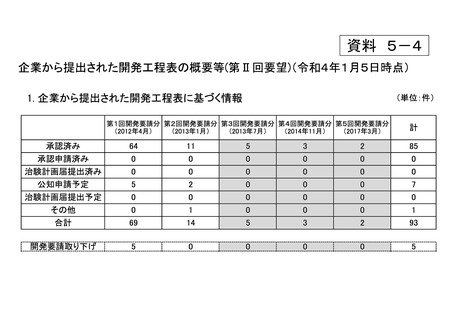
資料5-4 企業から提出された開発工程表の概要等(第II回要望) (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00022.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第50回 1/26)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
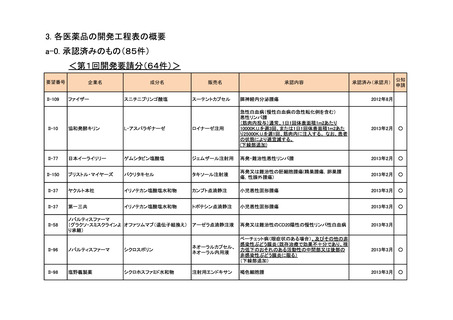
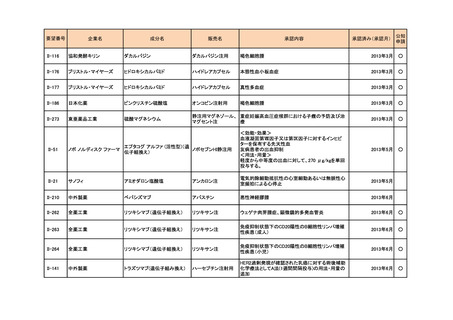
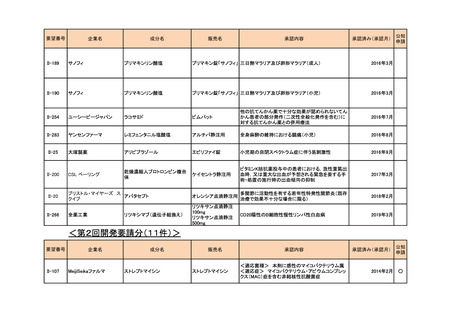
3. 各医薬品の開発工程表の概要
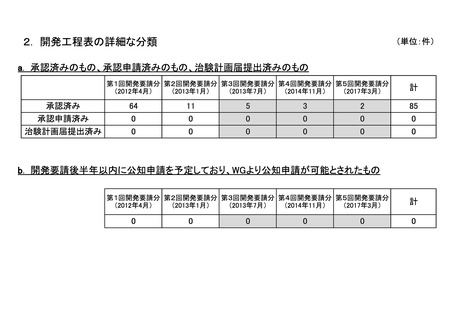
a-0. 承認済みのもの(85件)
<第1回開発要請分(64件)>
要望番号
II-109
企業名
ファイザー
成分名
スニチニブリンゴ酸塩
販売名
承認内容
承認済み(承認月)
公知
申請
スーテントカプセル
膵神経内分泌腫瘍
2012年8月
2013年2月
○
II-10
協和発酵キリン
L-アスパラギナーゼ
ロイナーゼ注用
急性白血病(慢性白血病の急性転化例を含む)
悪性リンパ腫
(筋肉内投与)通常、1日1回体表面積1m2あたり
10000K.U.を週3回、または1日1回体表面積1m2あた
り25000K.U.を週1回、筋肉内に注入する。 なお、患者
の状態により適宜減する。
(下線部追加)
II-77
日本イーライリリー
ゲムシタビン塩酸塩
ジェムザール注射用
再発・難治性悪性リンパ腫
2013年2月
○
II-150
ブリストル・マイヤーズ
パクリタキセル
タキソール注射液
再発又は難治性の胚細胞腫瘍(精巣腫瘍,卵巣腫
瘍,性腺外腫瘍)
2013年2月
○
II-37
ヤクルト本社
イリノテカン塩酸塩水和物
カンプト点滴静注
小児悪性固形腫瘍
2013年3月
○
II-37
第一三共
イリノテカン塩酸塩水和物
トポテシン点滴静注
小児悪性固形腫瘍
2013年3月
○
II-58
ノバルティスファーマ
(グラクソ・スミスクラインよ オファツムマブ(遺伝子組換え) アーゼラ点滴静注液
り承継)
再発又は難治性のCD20陽性の慢性リンパ性白血病
2013年3月
II-96
ノバルティスファーマ
シクロスポリン
ベーチェット病(眼症状のある場合)、及びその他の非
感染性ぶどう膜炎(既存治療で効果不十分であり、視
ネオーラルカプセル、
力低下のおそれのある活動性の中間部又は後部の
ネオーラル内用液
非感染性ぶどう膜炎に限る)
(下線部追加)
II-98
塩野義製薬
シクロホスファミド水和物
注射用エンドキサン
褐色細胞腫
2013年3月
○
2013年3月
○
a-0. 承認済みのもの(85件)
<第1回開発要請分(64件)>
要望番号
II-109
企業名
ファイザー
成分名
スニチニブリンゴ酸塩
販売名
承認内容
承認済み(承認月)
公知
申請
スーテントカプセル
膵神経内分泌腫瘍
2012年8月
2013年2月
○
II-10
協和発酵キリン
L-アスパラギナーゼ
ロイナーゼ注用
急性白血病(慢性白血病の急性転化例を含む)
悪性リンパ腫
(筋肉内投与)通常、1日1回体表面積1m2あたり
10000K.U.を週3回、または1日1回体表面積1m2あた
り25000K.U.を週1回、筋肉内に注入する。 なお、患者
の状態により適宜減する。
(下線部追加)
II-77
日本イーライリリー
ゲムシタビン塩酸塩
ジェムザール注射用
再発・難治性悪性リンパ腫
2013年2月
○
II-150
ブリストル・マイヤーズ
パクリタキセル
タキソール注射液
再発又は難治性の胚細胞腫瘍(精巣腫瘍,卵巣腫
瘍,性腺外腫瘍)
2013年2月
○
II-37
ヤクルト本社
イリノテカン塩酸塩水和物
カンプト点滴静注
小児悪性固形腫瘍
2013年3月
○
II-37
第一三共
イリノテカン塩酸塩水和物
トポテシン点滴静注
小児悪性固形腫瘍
2013年3月
○
II-58
ノバルティスファーマ
(グラクソ・スミスクラインよ オファツムマブ(遺伝子組換え) アーゼラ点滴静注液
り承継)
再発又は難治性のCD20陽性の慢性リンパ性白血病
2013年3月
II-96
ノバルティスファーマ
シクロスポリン
ベーチェット病(眼症状のある場合)、及びその他の非
感染性ぶどう膜炎(既存治療で効果不十分であり、視
ネオーラルカプセル、
力低下のおそれのある活動性の中間部又は後部の
ネオーラル内用液
非感染性ぶどう膜炎に限る)
(下線部追加)
II-98
塩野義製薬
シクロホスファミド水和物
注射用エンドキサン
褐色細胞腫
2013年3月
○
2013年3月
○