よむ、つかう、まなぶ。
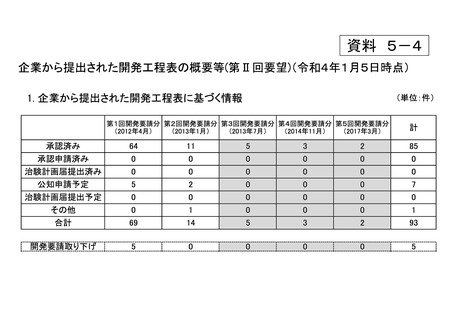
資料5-4 企業から提出された開発工程表の概要等(第II回要望) (13 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000198856_00022.html |
| 出典情報 | 医薬・生活衛生局が実施する検討会 医療上の必要性の高い未承認薬・適応外薬検討会議(第50回 1/26)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
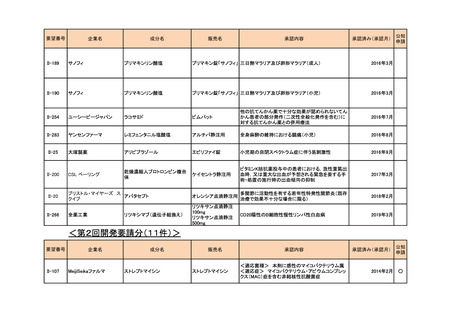
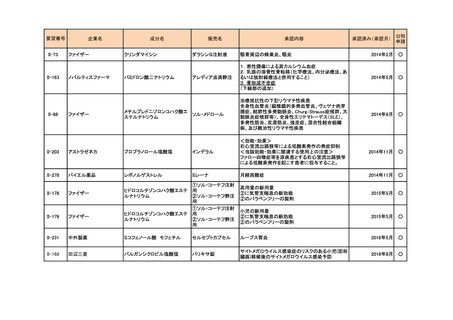
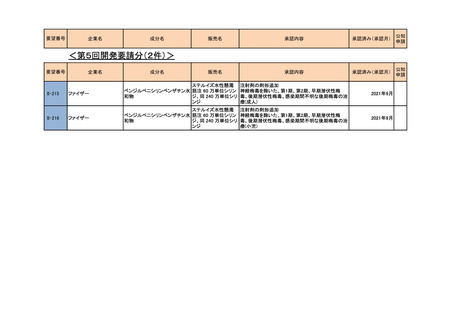
要望番号
企業名
成分名
販売名
承認内容
承認済み(承認月)
公知
申請
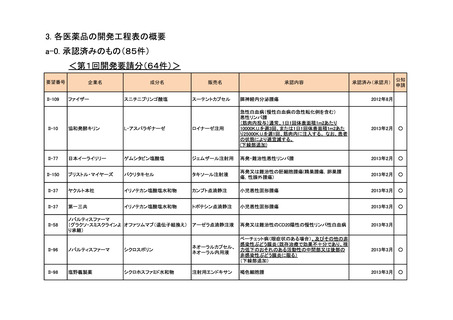
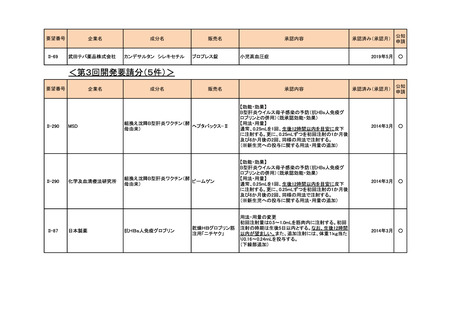
抗HBs人免疫グロブリン
用法・用量の変更
初回注射量は0.5~1.0mLを筋肉内に注射する。初回
注射の時期は生後5日以内とする。なお、生後12時間
抗HBs人免疫グロブリ 以内が望ましい。また、追加注射には、体重1kg当た
ン筋注「日赤」
り0.16~0.24mLを投与する。
(下線部追加)
2014年3月
○
抗HBs人免疫グロブリン
用法・用量の変更
初回注射量は0.5~1.0mLを筋肉内に注射する。初回
注射の時期は生後5日以内とする。なお、生後12時間
以内が望ましい。また、追加注射には、体重1kg当た
り0.16~0.24mLを投与する。
(下線部追加)
2014年3月
○
ヘブスブリン筋注用
II-87
II-87
日本血液製剤機構
化学及血清療法研究所
ヘパトセーラ
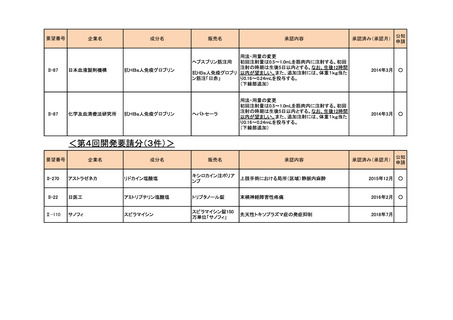
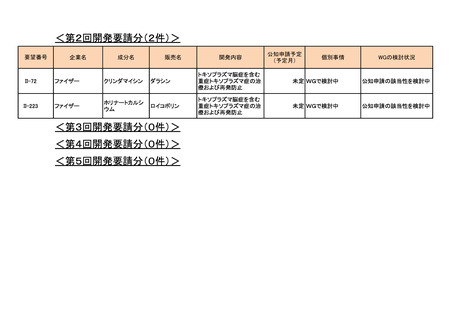
<第4回開発要請分(3件)>
要望番号
企業名
成分名
販売名
承認内容
II-270
アストラゼネカ
リドカイン塩酸塩
キシロカイン注ポリア
ンプ
上肢手術における局所(区域)静脈内麻酔
II-22
日医工
アミトリプチリン塩酸塩
トリプタノール錠
Ⅱ-110
サノフィ
スピラマイシン
スピラマイシン錠150
万単位「サノフィ」
承認済み(承認月)
公知
申請
2015年12月
○
末梢神経障害性疼痛
2016年2月
○
先天性トキソプラズマ症の発症抑制
2018年7月
企業名
成分名
販売名
承認内容
承認済み(承認月)
公知
申請
抗HBs人免疫グロブリン
用法・用量の変更
初回注射量は0.5~1.0mLを筋肉内に注射する。初回
注射の時期は生後5日以内とする。なお、生後12時間
抗HBs人免疫グロブリ 以内が望ましい。また、追加注射には、体重1kg当た
ン筋注「日赤」
り0.16~0.24mLを投与する。
(下線部追加)
2014年3月
○
抗HBs人免疫グロブリン
用法・用量の変更
初回注射量は0.5~1.0mLを筋肉内に注射する。初回
注射の時期は生後5日以内とする。なお、生後12時間
以内が望ましい。また、追加注射には、体重1kg当た
り0.16~0.24mLを投与する。
(下線部追加)
2014年3月
○
ヘブスブリン筋注用
II-87
II-87
日本血液製剤機構
化学及血清療法研究所
ヘパトセーラ
<第4回開発要請分(3件)>
要望番号
企業名
成分名
販売名
承認内容
II-270
アストラゼネカ
リドカイン塩酸塩
キシロカイン注ポリア
ンプ
上肢手術における局所(区域)静脈内麻酔
II-22
日医工
アミトリプチリン塩酸塩
トリプタノール錠
Ⅱ-110
サノフィ
スピラマイシン
スピラマイシン錠150
万単位「サノフィ」
承認済み(承認月)
公知
申請
2015年12月
○
末梢神経障害性疼痛
2016年2月
○
先天性トキソプラズマ症の発症抑制
2018年7月