よむ、つかう、まなぶ。
総-7参考4 (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_71462.html |
| 出典情報 | 中央社会保険医療協議会 総会(第648回 3/11)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
3.臨床成績
鼻茸を伴う慢性副鼻腔炎(既存治療で効果不十分な患者に限る)の承認時に評価を行った
臨床試験の成績を示す。
国際共同第Ⅲ相試験(D5242C00001 試験)
【試験の概要】
手術や全身性ステロイド薬によっても効果不十分な CRSwNP 患者 410 例(日本人患者 33
例を含む)を対象に、プラセボ対照無作為化二重盲検並行群間比較試験が実施された。
用法・用量は、本剤 210 mg 又はプラセボを 4 週間隔で 52 週間皮下投与することと設定
され、本邦の患者を除き、試験期間を通じてモメタゾンフランカルボン酸エステル鼻噴霧薬
又は同等量の鼻噴霧用ステロイド1)を一定用量で併用することと規定された2)。
有効性の主要評価項目として、投与 52 週時の鼻茸スコア及び鼻閉スコアのベースライン
からの変化量が設定され、2 つの主要評価項目でともに本剤群とプラセボ群の対比較におい
て統計学的に有意な差が認められた場合に本試験は成功とされた。
対象となる患者は、18 歳以上の CRSwNP 患者で、以下の基準を満たすこととされた。
(主な選択基準)
•
スクリーニング前 12 カ月以上にわたり、CRSwNP と診断され、以下の状態である
➢
スクリーニング時及び無作為化時に中央読影者が判定した要手術の状態[鼻茸ス
コアが 5 以上(各鼻腔におけるスコアは 2 以上)と定義]と重症度が一致する
➢
スクリーニング時及び無作為化時の鼻閉スコアが 2 以上
➢
スクリーニング前 8 週間超にわたり、鼻漏や嗅覚の減少又は消失といった鼻茸の
症状が継続して記録されている
•
スクリーニング時及び無作為化時の副鼻腔評価テスト-22 質問票(以下、
「SNOT-22」
)
の合計スコアが 30 以上
•
スクリーニング前 30 日以上にわたり、CRSwNP に対して何らかの標準治療を安定的に
受けている
•
スクリーニング前 3 カ月以内を除くスクリーニング前過去 12 カ月以内に、鼻茸増悪に
対する全身性ステロイドの 3 日以上連続した投与若しくは筋肉内デポ注射剤の単回投
与による治療歴の記録が確認できるか禁忌若しくは忍容性不良である、又は鼻茸手術
歴が確認できるか禁忌若しくは忍容性不良である
•
無作為化前 14 日間のうち 8 日以上で評価可能な日誌の日次データが得られている
(Day -13 から Day 0 までに収集された、ベースラインとなる 2 週間ごとの値)
【結果】
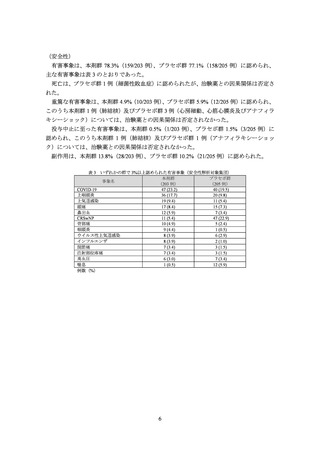
(有効性)
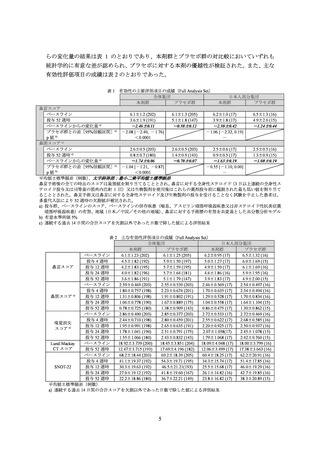
有効性の主要評価項目である投与 52 週時の鼻茸スコア及び鼻閉スコアのベースラインか
1)
2)
CRSwNP に対して各国又は地域で承認された鼻噴霧用ステロイドの最高用量
本邦の患者は試験期間中のモメタゾンフランカルボン酸エステル鼻噴霧薬又は同等量の鼻噴霧用ステロイドの投与は
必須とされなかった。
4
鼻茸を伴う慢性副鼻腔炎(既存治療で効果不十分な患者に限る)の承認時に評価を行った
臨床試験の成績を示す。
国際共同第Ⅲ相試験(D5242C00001 試験)
【試験の概要】
手術や全身性ステロイド薬によっても効果不十分な CRSwNP 患者 410 例(日本人患者 33
例を含む)を対象に、プラセボ対照無作為化二重盲検並行群間比較試験が実施された。
用法・用量は、本剤 210 mg 又はプラセボを 4 週間隔で 52 週間皮下投与することと設定
され、本邦の患者を除き、試験期間を通じてモメタゾンフランカルボン酸エステル鼻噴霧薬
又は同等量の鼻噴霧用ステロイド1)を一定用量で併用することと規定された2)。
有効性の主要評価項目として、投与 52 週時の鼻茸スコア及び鼻閉スコアのベースライン
からの変化量が設定され、2 つの主要評価項目でともに本剤群とプラセボ群の対比較におい
て統計学的に有意な差が認められた場合に本試験は成功とされた。
対象となる患者は、18 歳以上の CRSwNP 患者で、以下の基準を満たすこととされた。
(主な選択基準)
•
スクリーニング前 12 カ月以上にわたり、CRSwNP と診断され、以下の状態である
➢
スクリーニング時及び無作為化時に中央読影者が判定した要手術の状態[鼻茸ス
コアが 5 以上(各鼻腔におけるスコアは 2 以上)と定義]と重症度が一致する
➢
スクリーニング時及び無作為化時の鼻閉スコアが 2 以上
➢
スクリーニング前 8 週間超にわたり、鼻漏や嗅覚の減少又は消失といった鼻茸の
症状が継続して記録されている
•
スクリーニング時及び無作為化時の副鼻腔評価テスト-22 質問票(以下、
「SNOT-22」
)
の合計スコアが 30 以上
•
スクリーニング前 30 日以上にわたり、CRSwNP に対して何らかの標準治療を安定的に
受けている
•
スクリーニング前 3 カ月以内を除くスクリーニング前過去 12 カ月以内に、鼻茸増悪に
対する全身性ステロイドの 3 日以上連続した投与若しくは筋肉内デポ注射剤の単回投
与による治療歴の記録が確認できるか禁忌若しくは忍容性不良である、又は鼻茸手術
歴が確認できるか禁忌若しくは忍容性不良である
•
無作為化前 14 日間のうち 8 日以上で評価可能な日誌の日次データが得られている
(Day -13 から Day 0 までに収集された、ベースラインとなる 2 週間ごとの値)
【結果】
(有効性)
有効性の主要評価項目である投与 52 週時の鼻茸スコア及び鼻閉スコアのベースラインか
1)
2)
CRSwNP に対して各国又は地域で承認された鼻噴霧用ステロイドの最高用量
本邦の患者は試験期間中のモメタゾンフランカルボン酸エステル鼻噴霧薬又は同等量の鼻噴霧用ステロイドの投与は
必須とされなかった。
4