よむ、つかう、まなぶ。
薬-9日本バイオテク協議会[1.8MB] (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_59378.html |
| 出典情報 | 中央社会保険医療協議会 薬価専門部会(第236回 7/9)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
<具体的方策>
【医師主導治験により開発された医薬品の加算対象の見直し】
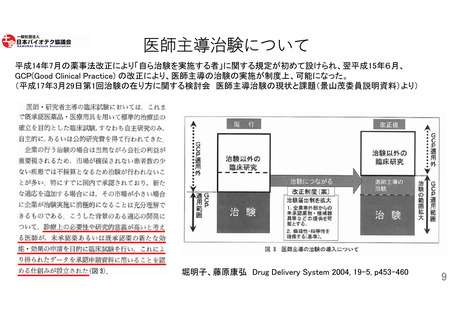
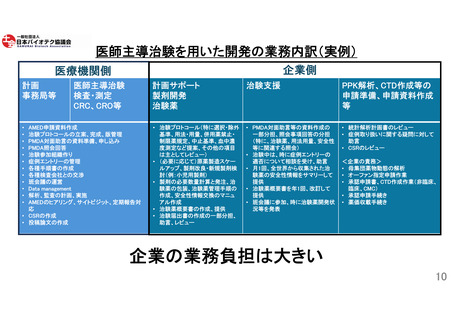
難病・希少疾病用薬の開発に医師主導治験の果たす役割は大きく(参照:9頁)、出口企業となる創薬ベン
チャーは医師主導治験を活用しているが、現行ルールでは必ずしも加算が認められていない(参照:11頁)。
大手製薬企業が手掛けない医薬品開発のイノベーション評価のために、加算要件を満たす場合は加算対
象とする。
【原価計算方式における原薬・製剤購入価格に関する開示度の取扱いの見直し】
高い革新性が有用性系加算として評価された新医薬品に対し、申請企業の努力だけではどうすることもで
きない開示度の低さだけで加算係数を一律 “0”とされてしまう現在の運用を見直していただきたい。
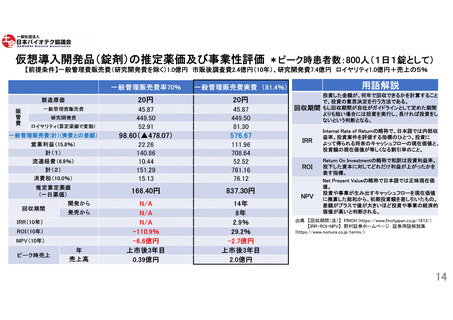
【低分子新薬の原価計算方式における一般管理販売費率の上限撤廃】
製造原価の安い低分子医薬品について、希少疾病用医薬品指定を受けている場合は、原価計算方式が適
用される場合、開発に要した経費を適切に薬価に反映していただけるよう、一般管理販売費率に上限を設
けない(参照:14頁)。
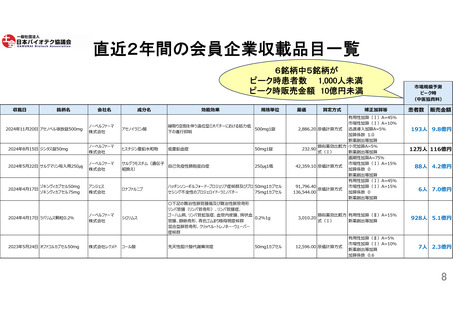
【ウルトラオーファン加算の新設】
大手製薬企業が手掛けない、希少疾病の中でも患者数が特に少ないウルトラオーファン(患者数1,000人未
満)の疾病に対する開発意欲が湧く薬価算定上の評価をする(参照:15頁)。
6
【医師主導治験により開発された医薬品の加算対象の見直し】
難病・希少疾病用薬の開発に医師主導治験の果たす役割は大きく(参照:9頁)、出口企業となる創薬ベン
チャーは医師主導治験を活用しているが、現行ルールでは必ずしも加算が認められていない(参照:11頁)。
大手製薬企業が手掛けない医薬品開発のイノベーション評価のために、加算要件を満たす場合は加算対
象とする。
【原価計算方式における原薬・製剤購入価格に関する開示度の取扱いの見直し】
高い革新性が有用性系加算として評価された新医薬品に対し、申請企業の努力だけではどうすることもで
きない開示度の低さだけで加算係数を一律 “0”とされてしまう現在の運用を見直していただきたい。
【低分子新薬の原価計算方式における一般管理販売費率の上限撤廃】
製造原価の安い低分子医薬品について、希少疾病用医薬品指定を受けている場合は、原価計算方式が適
用される場合、開発に要した経費を適切に薬価に反映していただけるよう、一般管理販売費率に上限を設
けない(参照:14頁)。
【ウルトラオーファン加算の新設】
大手製薬企業が手掛けない、希少疾病の中でも患者数が特に少ないウルトラオーファン(患者数1,000人未
満)の疾病に対する開発意欲が湧く薬価算定上の評価をする(参照:15頁)。
6