よむ、つかう、まなぶ。
薬-9日本バイオテク協議会[1.8MB] (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_59378.html |
| 出典情報 | 中央社会保険医療協議会 薬価専門部会(第236回 7/9)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
創薬ベンチャーの薬価算定における課題①
○医師主導治験を用いた開発
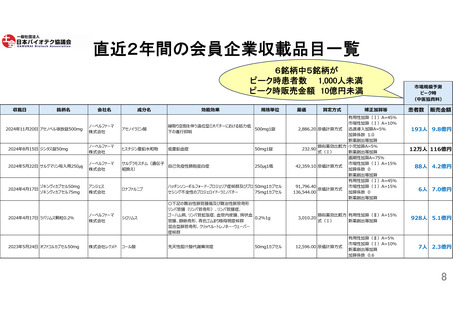
創薬ベンチャーは、医師主導治験を用いた開発を行うことが多い。既収載品の適応拡大
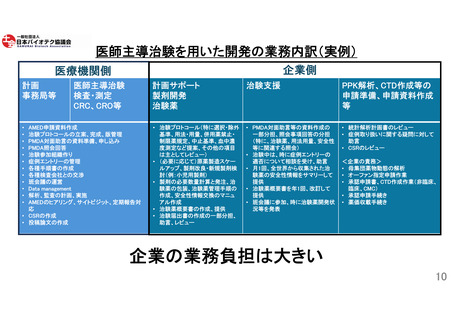
だけではなく、新規収載の新医薬品として開発する場合は、治験薬製造や物性データの
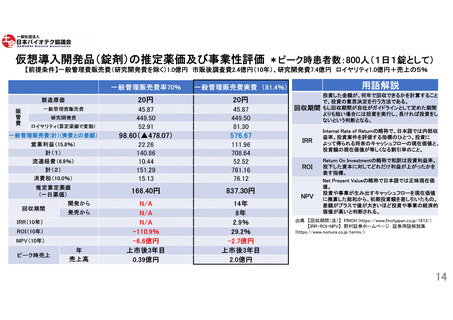
取得等、企業負担は大きい(参照:10頁)。しかしながら、現行ルールでは医師主導治験
を用いているというだけで補正加算の対象から外されてしまう場合がある(参照:11頁)。
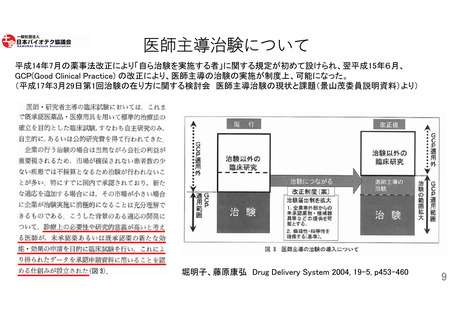
出口企業となる意欲は削がれ、難病・希少疾病用薬開発において不可欠(参照:9頁)と
なっている医師主導治験によるアカデミアの研究成果の社会実装を阻害する状況にある。
○原価計算方式における開示度の取扱い
原価計算方式における製品総原価の開示に当該企業は努力しているものの、独立企業
から原薬・製剤を購入する場合、購入先に原価を開示されるか否かは、申請企業の努力
にも限界がある(参照:12頁~13頁) 。革新的な医薬品として高い評価を受けた医薬品
について、申請企業の対処ではどうにもならない部分で薬価算定上の評価が皆無とされ
てしまうのは、医薬品の適切なイノベーション評価を阻害するものと考える。
4
○医師主導治験を用いた開発
創薬ベンチャーは、医師主導治験を用いた開発を行うことが多い。既収載品の適応拡大
だけではなく、新規収載の新医薬品として開発する場合は、治験薬製造や物性データの
取得等、企業負担は大きい(参照:10頁)。しかしながら、現行ルールでは医師主導治験
を用いているというだけで補正加算の対象から外されてしまう場合がある(参照:11頁)。
出口企業となる意欲は削がれ、難病・希少疾病用薬開発において不可欠(参照:9頁)と
なっている医師主導治験によるアカデミアの研究成果の社会実装を阻害する状況にある。
○原価計算方式における開示度の取扱い
原価計算方式における製品総原価の開示に当該企業は努力しているものの、独立企業
から原薬・製剤を購入する場合、購入先に原価を開示されるか否かは、申請企業の努力
にも限界がある(参照:12頁~13頁) 。革新的な医薬品として高い評価を受けた医薬品
について、申請企業の対処ではどうにもならない部分で薬価算定上の評価が皆無とされ
てしまうのは、医薬品の適切なイノベーション評価を阻害するものと考える。
4