よむ、つかう、まなぶ。
薬-9日本バイオテク協議会[1.8MB] (10 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_59378.html |
| 出典情報 | 中央社会保険医療協議会 薬価専門部会(第236回 7/9)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
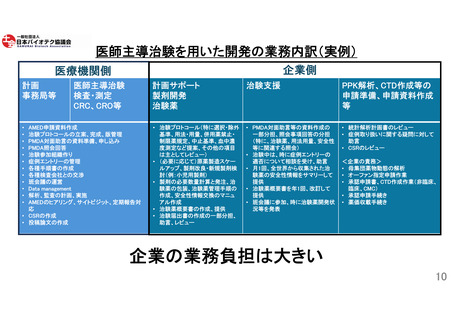
医師主導治験を用いた開発の業務内訳(実例)
企業側
医療機関側
計画
事務局等
医師主導治験
検査・測定
CRC、CRO等
AMED申請資料作成
治験プロトコールの立案、完成、版管理
PMDA対面助言の資料準備、申し込み
PMDA照会回答
治験参加組織作り
症例エントリーの管理
各種手順書の作成
各種検査会社との交渉
班会議の運営
Data management
解析、監査の計画、実施
AMEDのヒアリング、サイトビジット、定期報告対
応
• CSRの作成
• 投稿論文の作成
•
•
•
•
•
•
•
•
•
•
•
•
計画サポート
製剤開発
治験薬
治験支援
PPK解析、CTD作成等の
申請準備、申請資料作成
等
• 治験プロトコール(特に選択・除外
基準、用法・用量、併用薬禁止・
制限薬規定、中止基準、血中濃
度測定など提案、その他の項目
は主としてレビュー)
• (必要に応じて)原薬製造スケー
ルアップ、製剤改良・新規製剤検
討(例:小児用製剤)
• 製剤の必要数量計算と発注、治
験薬の包装、治験薬管理手順の
作成、安全性情報交換のマニュ
アル作成
• 治験薬概要書の作成、提供
• 治験届出書の作成の一部分担、
助言、レビュー
• PMDA対面助言等の資料作成の
一部分担、照会事項回答の分担
(特に、治験薬、用法用量、安全性
等に関連する照会)
• 治験中は、時に症例エントリーの
適否について相談を受け、助言
• 月1回、全世界から収集された治
験薬の安全性情報をサマリーして
提供
• 治験薬概要書を年1回、改訂して
提供
• 班会議に参加、時に治験薬開発状
況等を発表
• 統計解析計画書のレビュー
• 症例取り扱いに関する疑問に対して
助言
• CSRのレビュー
<企業の責務>
• 母集団薬物動態の解析
• オーファン指定申請作業
• 承認申請書、CTD作成作業(非臨床、
臨床、CMC)
• 承認申請手続き
• 薬価収載手続き
企業の業務負担は大きい
10
企業側
医療機関側
計画
事務局等
医師主導治験
検査・測定
CRC、CRO等
AMED申請資料作成
治験プロトコールの立案、完成、版管理
PMDA対面助言の資料準備、申し込み
PMDA照会回答
治験参加組織作り
症例エントリーの管理
各種手順書の作成
各種検査会社との交渉
班会議の運営
Data management
解析、監査の計画、実施
AMEDのヒアリング、サイトビジット、定期報告対
応
• CSRの作成
• 投稿論文の作成
•
•
•
•
•
•
•
•
•
•
•
•
計画サポート
製剤開発
治験薬
治験支援
PPK解析、CTD作成等の
申請準備、申請資料作成
等
• 治験プロトコール(特に選択・除外
基準、用法・用量、併用薬禁止・
制限薬規定、中止基準、血中濃
度測定など提案、その他の項目
は主としてレビュー)
• (必要に応じて)原薬製造スケー
ルアップ、製剤改良・新規製剤検
討(例:小児用製剤)
• 製剤の必要数量計算と発注、治
験薬の包装、治験薬管理手順の
作成、安全性情報交換のマニュ
アル作成
• 治験薬概要書の作成、提供
• 治験届出書の作成の一部分担、
助言、レビュー
• PMDA対面助言等の資料作成の
一部分担、照会事項回答の分担
(特に、治験薬、用法用量、安全性
等に関連する照会)
• 治験中は、時に症例エントリーの
適否について相談を受け、助言
• 月1回、全世界から収集された治
験薬の安全性情報をサマリーして
提供
• 治験薬概要書を年1回、改訂して
提供
• 班会議に参加、時に治験薬開発状
況等を発表
• 統計解析計画書のレビュー
• 症例取り扱いに関する疑問に対して
助言
• CSRのレビュー
<企業の責務>
• 母集団薬物動態の解析
• オーファン指定申請作業
• 承認申請書、CTD作成作業(非臨床、
臨床、CMC)
• 承認申請手続き
• 薬価収載手続き
企業の業務負担は大きい
10