よむ、つかう、まなぶ。
再生医療等の安全性の確保等に関する法律施行令第1条第2号ロの規定に基づき感染症の予防のために必要なものとして厚生労働大臣が定める核酸等に関する告示について[1.1MB] (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_58780.html |
| 出典情報 | 厚生科学審議会 再生医療等評価部会(第107回 5/13)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
別表
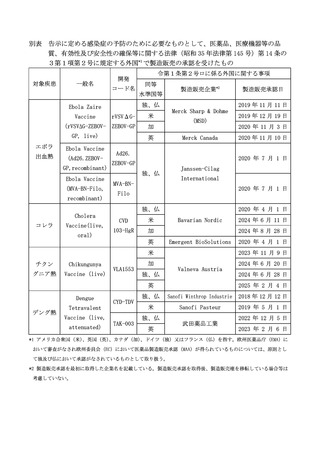
告示に定める感染症の予防のために必要なものとして、医薬品、医療機器等の品
質、有効性及び安全性の確保等に関する法律(昭和 35 年法律第 145 号)第 14 条の
3第1項第2号に規定する外国*1 で製造販売の承認を受けたもの
対象疾患
一般名
開発
コード名
令第1条第2号ロに係る外国に関する事項
同等
独、仏
Ebola Zaire
rVSVΔG-
米
(rVSV∆G-ZEBOV- ZEBOV-GP
加
Vaccine
GP, live)
エボラ
Ebola Vaccine
出血熱
(Ad26.ZEBOVGP,recombinant)
Ebola Vaccine
(MVA-BN-Filo,
recombinant)
製造販売企業*2
水準国等
2019 年 11 月 11 日
Merck Sharp & Dohme
(MSD)
コレラ
Vaccine(live,
oral)
英
Merck Canada
Ad26.
Janssen-Cilag
独、仏
International
MVA-BN-
2020 年 7 月 1 日
Filo
CVD
米
103-HgR
加
2020 年 4 月 1 日
Bavarian Nordic
グニア熱
Vaccine (live)
VLA1553
Emergent BioSolutions
デング熱
CYD-TDV
Tetravalent
Vaccine (live,
attenuated)
TAK-003
2020 年 4 月 1 日
2023 年 11 月 9 日
加
Valneva Austria
独、仏
英
Dengue
2024 年 6 月 11 日
2024 年 8 月 28 日
米
Chikungunya
2020 年 11 月 10 日
2020 年 7 月 1 日
ZEBOV-GP
英
チクン
2019 年 12 月 19 日
2020 年 11 月 3 日
独、仏
Cholera
製造販売承認日
2024 年 6 月 20 日
2024 年 6 月 28 日
2025 年 2 月 4 日
独、仏
Sanofi Winthrop Industrie
2018 年 12 月 12 日
米
Sanofi Pasteur
2019 年 5 月 1 日
独、仏
英
武田薬品工業
2022 年 12 月 5 日
2023 年 2 月 6 日
*1 アメリカ合衆国(米)
、英国(英)
、カナダ(加)
、ドイツ(独)又はフランス(仏)を指す。欧州医薬品庁(EMA)に
おいて審査がなされ欧州委員会(EC)において医薬品製造販売承認(MAA)が得られているものについては、原則とし
て独及び仏において承認がなされているものとして取り扱う。
*2 製造販売承認を最初に取得した企業名を記載している。製造販売承認を取得後、製造販売権を移転している場合等は
考慮していない。
告示に定める感染症の予防のために必要なものとして、医薬品、医療機器等の品
質、有効性及び安全性の確保等に関する法律(昭和 35 年法律第 145 号)第 14 条の
3第1項第2号に規定する外国*1 で製造販売の承認を受けたもの
対象疾患
一般名
開発
コード名
令第1条第2号ロに係る外国に関する事項
同等
独、仏
Ebola Zaire
rVSVΔG-
米
(rVSV∆G-ZEBOV- ZEBOV-GP
加
Vaccine
GP, live)
エボラ
Ebola Vaccine
出血熱
(Ad26.ZEBOVGP,recombinant)
Ebola Vaccine
(MVA-BN-Filo,
recombinant)
製造販売企業*2
水準国等
2019 年 11 月 11 日
Merck Sharp & Dohme
(MSD)
コレラ
Vaccine(live,
oral)
英
Merck Canada
Ad26.
Janssen-Cilag
独、仏
International
MVA-BN-
2020 年 7 月 1 日
Filo
CVD
米
103-HgR
加
2020 年 4 月 1 日
Bavarian Nordic
グニア熱
Vaccine (live)
VLA1553
Emergent BioSolutions
デング熱
CYD-TDV
Tetravalent
Vaccine (live,
attenuated)
TAK-003
2020 年 4 月 1 日
2023 年 11 月 9 日
加
Valneva Austria
独、仏
英
Dengue
2024 年 6 月 11 日
2024 年 8 月 28 日
米
Chikungunya
2020 年 11 月 10 日
2020 年 7 月 1 日
ZEBOV-GP
英
チクン
2019 年 12 月 19 日
2020 年 11 月 3 日
独、仏
Cholera
製造販売承認日
2024 年 6 月 20 日
2024 年 6 月 28 日
2025 年 2 月 4 日
独、仏
Sanofi Winthrop Industrie
2018 年 12 月 12 日
米
Sanofi Pasteur
2019 年 5 月 1 日
独、仏
英
武田薬品工業
2022 年 12 月 5 日
2023 年 2 月 6 日
*1 アメリカ合衆国(米)
、英国(英)
、カナダ(加)
、ドイツ(独)又はフランス(仏)を指す。欧州医薬品庁(EMA)に
おいて審査がなされ欧州委員会(EC)において医薬品製造販売承認(MAA)が得られているものについては、原則とし
て独及び仏において承認がなされているものとして取り扱う。
*2 製造販売承認を最初に取得した企業名を記載している。製造販売承認を取得後、製造販売権を移転している場合等は
考慮していない。