よむ、つかう、まなぶ。
資料1:臨床研究法の見直しに係る各論点について (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_24643.html |
| 出典情報 | 厚生科学審議会 臨床研究部会(第29回 3/24)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
1.いわゆる観察研究に関する臨床研究法の適用範囲について
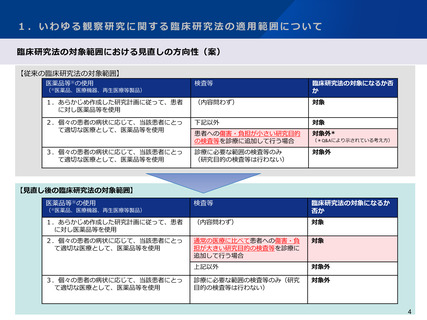
法における臨床研究の考え方及び観察研究の取扱いについて(案)
今後の整理
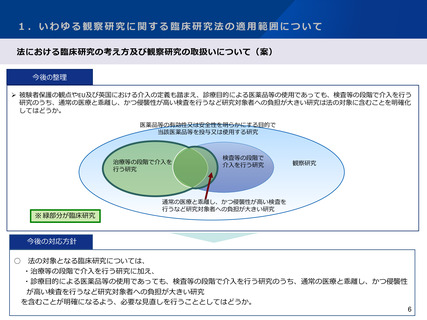
被験者保護の観点やEU及び英国における介入の定義も踏まえ、診療目的による医薬品等の使用であっても、検査等の段階で介入を行う
研究のうち、通常の医療と乖離し、かつ侵襲性が高い検査を行うなど研究対象者への負担が大きい研究は法の対象に含むことを明確化
してはどうか。
医薬品等の有効性又は安全性を明らかにする目的で
当該医薬品等を投与又は使用する研究
治療等の段階で介入を
行う研究
※ 緑部分が臨床研究
検査等の段階で
介入を行う研究
観察研究
通常の医療と乖離し、かつ侵襲性が高い検査を
行うなど研究対象者への負担が大きい研究
今後の対応方針
○ 法の対象となる臨床研究については、
・治療等の段階で介入を行う研究に加え、
・診療目的による医薬品等の使用であっても、検査等の段階で介入を行う研究のうち、通常の医療と乖離し、かつ侵襲性
が高い検査を行うなど研究対象者への負担が大きい研究
を含むことが明確になるよう、必要な見直しを行うこととしてはどうか。
6
法における臨床研究の考え方及び観察研究の取扱いについて(案)
今後の整理
被験者保護の観点やEU及び英国における介入の定義も踏まえ、診療目的による医薬品等の使用であっても、検査等の段階で介入を行う
研究のうち、通常の医療と乖離し、かつ侵襲性が高い検査を行うなど研究対象者への負担が大きい研究は法の対象に含むことを明確化
してはどうか。
医薬品等の有効性又は安全性を明らかにする目的で
当該医薬品等を投与又は使用する研究
治療等の段階で介入を
行う研究
※ 緑部分が臨床研究
検査等の段階で
介入を行う研究
観察研究
通常の医療と乖離し、かつ侵襲性が高い検査を
行うなど研究対象者への負担が大きい研究
今後の対応方針
○ 法の対象となる臨床研究については、
・治療等の段階で介入を行う研究に加え、
・診療目的による医薬品等の使用であっても、検査等の段階で介入を行う研究のうち、通常の医療と乖離し、かつ侵襲性
が高い検査を行うなど研究対象者への負担が大きい研究
を含むことが明確になるよう、必要な見直しを行うこととしてはどうか。
6