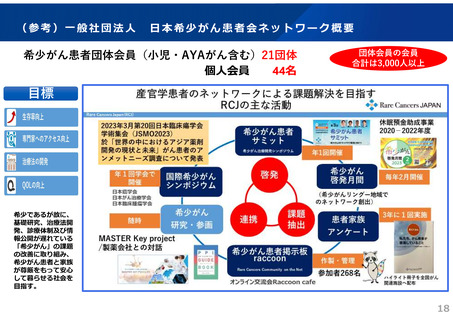
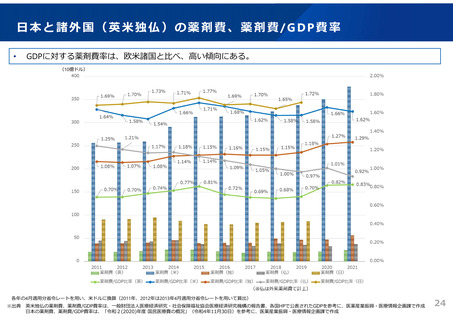
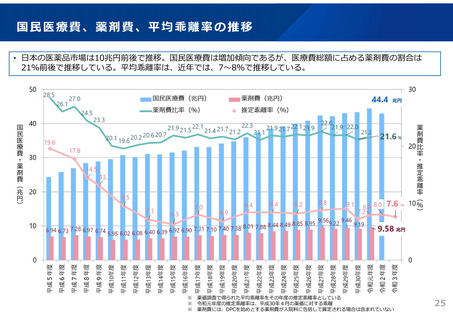
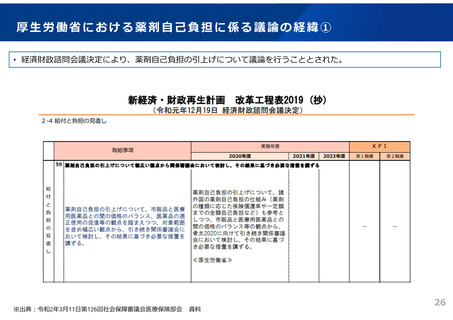
よむ、つかう、まなぶ。
【資料1】積み残しの論点等について (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_32480.html |
| 出典情報 | 医薬品の迅速・安定供給実現に向けた総合対策に関する有識者検討会(第11回 4/4)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
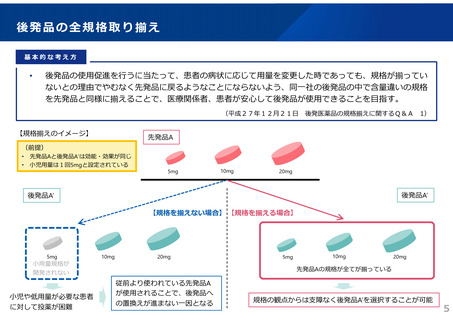
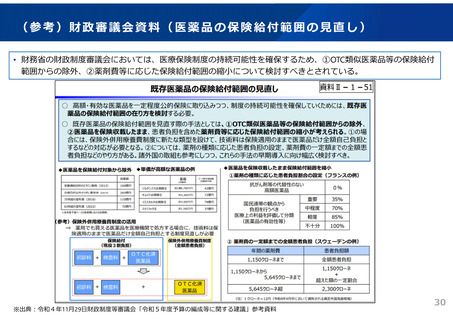
後発品の全規格取り揃え
基本的な考え方
•
後発品の使用促進を行うに当たって、患者の病状に応じて用量を変更した時であっても、規格が揃ってい
ないとの理由でやむなく先発品に戻るようなことにならないよう、同一社の後発品の中で含量違いの規格
を先発品と同様に揃えることで、医療関係者、患者が安心して後発品が使用できることを目指す。
(平成27年12月21日 後発医薬品の規格揃えに関するQ&A
【規格揃えのイメージ】
1)
先発品A
(前提)
•
•
先発品Aと後発品A’は効能・効果が同じ
小児用量は1回5mgと設定されている
5mg
10mg
20mg
後発品A’
後発品A’
【規格を揃えない場合】 【規格を揃える場合】
5mg
小用量規格が
開発されない
小児や低用量が必要な患者
に対して投薬が困難
10mg
20mg
5mg
10mg
20mg
先発品Aの規格が全てが揃っている
従前より使われている先発品A
が使用されることで、後発品へ
の置換えが進まない一因となる
規格の観点からは支障なく後発品A’を選択することが可能
5
基本的な考え方
•
後発品の使用促進を行うに当たって、患者の病状に応じて用量を変更した時であっても、規格が揃ってい
ないとの理由でやむなく先発品に戻るようなことにならないよう、同一社の後発品の中で含量違いの規格
を先発品と同様に揃えることで、医療関係者、患者が安心して後発品が使用できることを目指す。
(平成27年12月21日 後発医薬品の規格揃えに関するQ&A
【規格揃えのイメージ】
1)
先発品A
(前提)
•
•
先発品Aと後発品A’は効能・効果が同じ
小児用量は1回5mgと設定されている
5mg
10mg
20mg
後発品A’
後発品A’
【規格を揃えない場合】 【規格を揃える場合】
5mg
小用量規格が
開発されない
小児や低用量が必要な患者
に対して投薬が困難
10mg
20mg
5mg
10mg
20mg
先発品Aの規格が全てが揃っている
従前より使われている先発品A
が使用されることで、後発品へ
の置換えが進まない一因となる
規格の観点からは支障なく後発品A’を選択することが可能
5