よむ、つかう、まなぶ。
資料1-1 早期導入を要望する医療機器(放射性ビーズ(No. 2016-2))の品目追加に関する要望書 (6 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_32363.html |
| 出典情報 | 医療ニーズの高い医療機器等の早期導入に関する検討会(第35回 3/31)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
試験概要
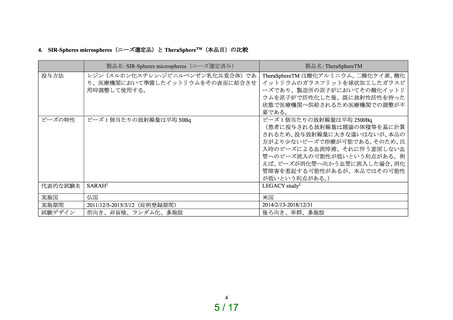
製品名: SIR-Spheres microspheres(ニーズ選定済み)
製品名: TheraSphereTM
年齢 18 歳以上、余命 3 ヶ月以上、Eastern Cooperative Oncology Group
(ECOG)パフォーマンスステータス 0 または 1、Child-Pugh 分類 A
または B スコア 7 以下で局所進行肝細胞癌(Barcelona Clinic Liver
Cancer [BCLC] stage C)患者、または切除、焼灼により根治後に切
除、移植、焼灼の適応とならない新たな病変を有する患者、2 回の
TACE で不応であった患者を対象。被験者はソラフェニブ投与群と
SIRT 群に 1:1 で割付けられた。主要評価項目は全生存期間(OS)で
あった。副次的評価項目として、無増悪生存期間(PFS)、奏効率、
QOL スコア(QLQ-C30)
、有害事象等が収集された。
切除不能な孤立性肝細胞がん患者において本治療法の局
所腫瘍コントロールと効果持続期間を評価。本試験に参
加した 3 施設で 2014/2/13 から 2017/12/22 の間に本品に
よる治療を受けた 162 例を対象とした。
主要評価項目は以下の複合エンドポイントの達成率とし
た。
Localized mRECIST(※)評価による ORR(奏効率)が
40%以上であること
効果がみられた患者の 60%以上において Localized
mRECIST(※)評価による DOR(効果持続期間)が 6
ヵ月以上であること
副次的評価として RECIST1.1(※)、mRECIST(※)による評
価、有害事象の収集も行った。
(※)RECIST 1.1 は腫瘍縮小効果を評価する上で一般的
に 用 い ら れ る 評 価 手 法 で あ る 。 mRECIST ( modified
RECIST)は造影剤による腫瘍濃染を評価することで、特
に肝細胞癌において多くみられる腫瘍の縮小を伴わない
細 胞 壊 死効 果を 確 認する た め に用 いら れ る。な お 、
RECIST は通常、全身の腫瘍のうち、大きなものから順に
最大 5 個が評価対象として選択されるが、本品は肝内病
変の治療を目的としているため肝内に限局(Localized)し
た評価を主要評価項目として設定している。
5
6 / 17
製品名: SIR-Spheres microspheres(ニーズ選定済み)
製品名: TheraSphereTM
年齢 18 歳以上、余命 3 ヶ月以上、Eastern Cooperative Oncology Group
(ECOG)パフォーマンスステータス 0 または 1、Child-Pugh 分類 A
または B スコア 7 以下で局所進行肝細胞癌(Barcelona Clinic Liver
Cancer [BCLC] stage C)患者、または切除、焼灼により根治後に切
除、移植、焼灼の適応とならない新たな病変を有する患者、2 回の
TACE で不応であった患者を対象。被験者はソラフェニブ投与群と
SIRT 群に 1:1 で割付けられた。主要評価項目は全生存期間(OS)で
あった。副次的評価項目として、無増悪生存期間(PFS)、奏効率、
QOL スコア(QLQ-C30)
、有害事象等が収集された。
切除不能な孤立性肝細胞がん患者において本治療法の局
所腫瘍コントロールと効果持続期間を評価。本試験に参
加した 3 施設で 2014/2/13 から 2017/12/22 の間に本品に
よる治療を受けた 162 例を対象とした。
主要評価項目は以下の複合エンドポイントの達成率とし
た。
Localized mRECIST(※)評価による ORR(奏効率)が
40%以上であること
効果がみられた患者の 60%以上において Localized
mRECIST(※)評価による DOR(効果持続期間)が 6
ヵ月以上であること
副次的評価として RECIST1.1(※)、mRECIST(※)による評
価、有害事象の収集も行った。
(※)RECIST 1.1 は腫瘍縮小効果を評価する上で一般的
に 用 い ら れ る 評 価 手 法 で あ る 。 mRECIST ( modified
RECIST)は造影剤による腫瘍濃染を評価することで、特
に肝細胞癌において多くみられる腫瘍の縮小を伴わない
細 胞 壊 死効 果を 確 認する た め に用 いら れ る。な お 、
RECIST は通常、全身の腫瘍のうち、大きなものから順に
最大 5 個が評価対象として選択されるが、本品は肝内病
変の治療を目的としているため肝内に限局(Localized)し
た評価を主要評価項目として設定している。
5
6 / 17