よむ、つかう、まなぶ。
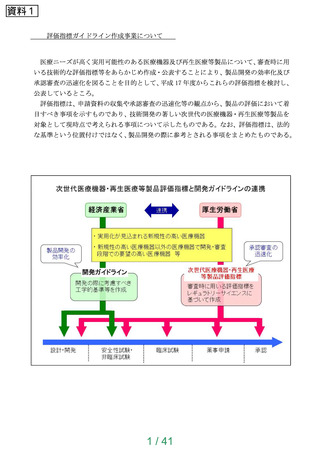
【資料1】次世代医療機器評価指標について (41 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_32218.html |
| 出典情報 | 薬事・食品衛生審議会 医療機器・体外診断薬部会(令和4年度第10回 3/27)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
equipment –
Electromagnetic disturbance characteristics –
Limits and
methods of measurement
7.IEC/TR 60878, Graphical symbols for electrical equipment in medical practice
8.IEC 62304, Medical device software –
Software life –
cycle processes
(その他)
1.FDA:Preparation and contents of application for ventricular assist devices
and total artificial hearts, FDA No. F89-33838 (1987)
2.NIH : Phased readiness testing of implantable total artificial hearts,
request for proposal, NHLBI-HV-92-28 (1992)
3.ASAIO-STS : Long-Term Mechanical Circulatory Support System Reliability
Recommendation (1998)
4.AAMI: TIR26:2000 心室補助および心臓置換システム(2000)
5.NEDO: 臨床応用に向けた体内埋め込み型人工心臓システム総合評価実験プロトコ
ール(NEDO プロジェクト)
(2001)
6.日本人工臓器学会:重症心不全に対する治療機器の臨床試験ガイドライン(案)
(2003)
7.ASTM F1841-97, Standard practice for Assessment of hemolysis in continuous
flow blood pumps
19
41 / 41
Electromagnetic disturbance characteristics –
Limits and
methods of measurement
7.IEC/TR 60878, Graphical symbols for electrical equipment in medical practice
8.IEC 62304, Medical device software –
Software life –
cycle processes
(その他)
1.FDA:Preparation and contents of application for ventricular assist devices
and total artificial hearts, FDA No. F89-33838 (1987)
2.NIH : Phased readiness testing of implantable total artificial hearts,
request for proposal, NHLBI-HV-92-28 (1992)
3.ASAIO-STS : Long-Term Mechanical Circulatory Support System Reliability
Recommendation (1998)
4.AAMI: TIR26:2000 心室補助および心臓置換システム(2000)
5.NEDO: 臨床応用に向けた体内埋め込み型人工心臓システム総合評価実験プロトコ
ール(NEDO プロジェクト)
(2001)
6.日本人工臓器学会:重症心不全に対する治療機器の臨床試験ガイドライン(案)
(2003)
7.ASTM F1841-97, Standard practice for Assessment of hemolysis in continuous
flow blood pumps
19
41 / 41