よむ、つかう、まなぶ。
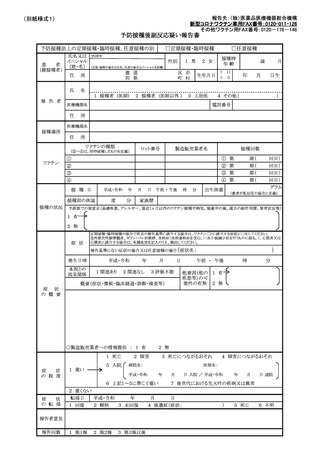
参考資料14 定期の予防接種等による副反応疑いの報告等の取扱いについて(平成25年3月30日付け健発0330第3号・薬食発0330第1号厚生労働省健康局長及び医薬食品局長連名通知。最終改正:令和4年10月24日) (4 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/shingi2/0000208910_00059.html |
| 出典情報 | 第92回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第27回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)(3/10)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
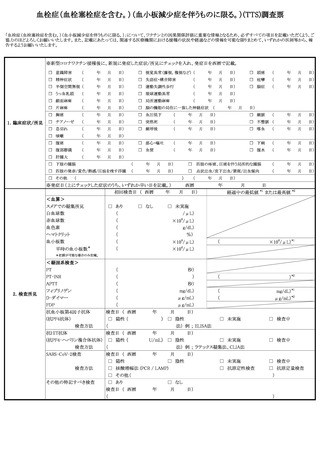
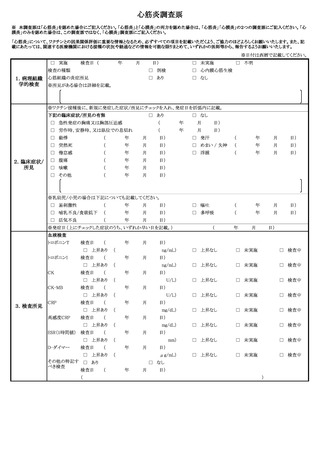
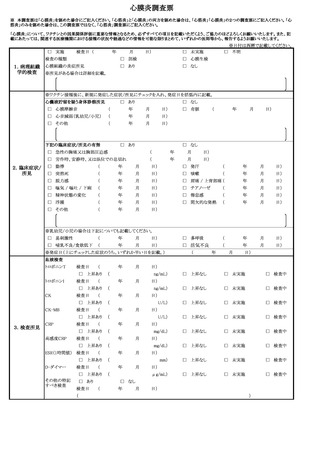
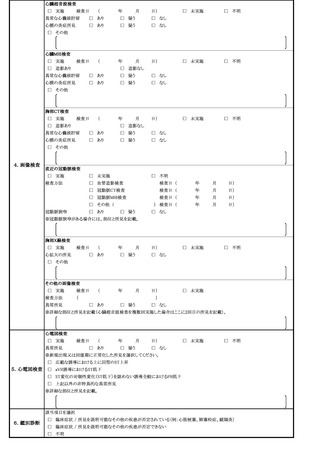
例についてはTTS調査票を、心筋炎が疑われる症例については心筋炎調査票を、心膜
炎が疑われる症例については心膜炎調査票を作成し、報告するものとすること。
3 製造販売業者等への情報提供及び製造販売業者等による情報収集への協力
厚生労働省において安全対策のため、1及び2により行われた報告の内容について
患者氏名(イニシャルを除く。)及び生年月日を除いた情報を当該予防接種ワクチンの
製造販売業者等に対し情報提供することがあるので、医師等は、医薬品、医療機器等の
品質、有効性及び安全性の確保等に関する法律第 68 条の2第2項に基づき、製造販売
業者等から副反応疑い報告に関する情報収集等の協力依頼がなされた際には、これに
協力すること。
また、1(9)の場合についても、ワクチンの製造販売業者等に対し同様に情報提供
することがあるので、市町村は、その旨あらかじめ保護者等に説明を行うこと。
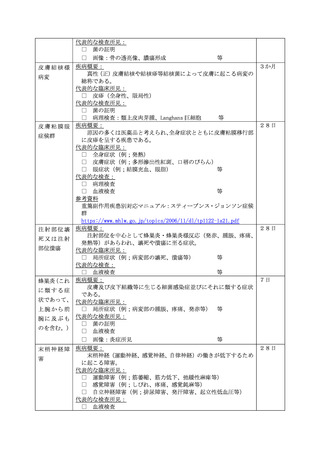
4 ヒトパピローマウイルス感染症の定期の予防接種又は任意接種に係る対応
(1)ヒトパピローマウイルス感染症の定期の予防接種には、ヒトパピローマウイルス
様粒子ワクチンの積極的勧奨の差控えにより接種機会を逃した方に対して、公平な
接種機会を確保する観点から、時限的に、従来の定期接種の対象年齢を超えて行う
接種(以下「キャッチアップ接種」という。)を含むこと。
(2) 広範な慢性の疼痛又は運動障害を中心とする多様な症状を呈する患者を診察し
た際には、医師はヒトパピローマウイルス感染症の定期の予防接種又は任意接種を
受けたかどうかを確認すること。
(3) ヒトパピローマウイルス感染症の定期の予防接種にあっては、接種後に広範な慢
性の疼痛又は運動障害を中心とする多様な症状が発生する場合があるため、医師が
これらの症状と接種との関連性を認めた場合、医師等は厚生労働大臣に対して1
(1)の規定による報告を行うこと。
(4) ヒトパピローマウイルス感染症の任意接種にあっては、接種後に広範な慢性の疼
痛又は運動障害を中心とする多様な症状が発生した場合、医薬品、医療機器等の品
質、有効性及び安全性の確保等に関する法律第 68 条の 10 第2項の規定に基づき、
薬局開設者、病院若しくは診療所の開設者又は医師、歯科医師、薬剤師その他の医
薬関係者は、2の規定による報告を行うこと。
(5) ヒトパピローマウイルス感染症のキャッチアップ接種にあっては、過去に接種
したヒトパピローマウイルス様粒子ワクチンの種類が不明の場合、結果として、異
なる種類のワクチンが接種される可能性があるため、ワクチンの互換性に関する安
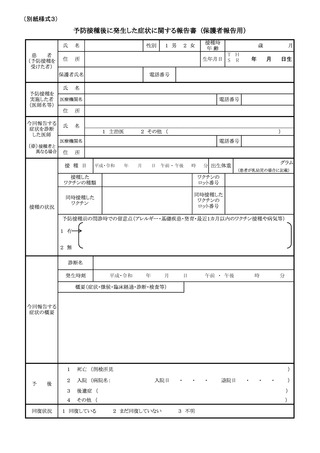
全性、免疫原性及び有効性についての情報収集の観点から、別紙様式1における予
診票での留意点にその旨明記すること。
(6)(3)及び(4)については、患者に接種を行った医師等以外の医師等において
も行うべきものであること。
炎が疑われる症例については心膜炎調査票を作成し、報告するものとすること。
3 製造販売業者等への情報提供及び製造販売業者等による情報収集への協力
厚生労働省において安全対策のため、1及び2により行われた報告の内容について
患者氏名(イニシャルを除く。)及び生年月日を除いた情報を当該予防接種ワクチンの
製造販売業者等に対し情報提供することがあるので、医師等は、医薬品、医療機器等の
品質、有効性及び安全性の確保等に関する法律第 68 条の2第2項に基づき、製造販売
業者等から副反応疑い報告に関する情報収集等の協力依頼がなされた際には、これに
協力すること。
また、1(9)の場合についても、ワクチンの製造販売業者等に対し同様に情報提供
することがあるので、市町村は、その旨あらかじめ保護者等に説明を行うこと。
4 ヒトパピローマウイルス感染症の定期の予防接種又は任意接種に係る対応
(1)ヒトパピローマウイルス感染症の定期の予防接種には、ヒトパピローマウイルス
様粒子ワクチンの積極的勧奨の差控えにより接種機会を逃した方に対して、公平な
接種機会を確保する観点から、時限的に、従来の定期接種の対象年齢を超えて行う
接種(以下「キャッチアップ接種」という。)を含むこと。
(2) 広範な慢性の疼痛又は運動障害を中心とする多様な症状を呈する患者を診察し
た際には、医師はヒトパピローマウイルス感染症の定期の予防接種又は任意接種を
受けたかどうかを確認すること。
(3) ヒトパピローマウイルス感染症の定期の予防接種にあっては、接種後に広範な慢
性の疼痛又は運動障害を中心とする多様な症状が発生する場合があるため、医師が
これらの症状と接種との関連性を認めた場合、医師等は厚生労働大臣に対して1
(1)の規定による報告を行うこと。
(4) ヒトパピローマウイルス感染症の任意接種にあっては、接種後に広範な慢性の疼
痛又は運動障害を中心とする多様な症状が発生した場合、医薬品、医療機器等の品
質、有効性及び安全性の確保等に関する法律第 68 条の 10 第2項の規定に基づき、
薬局開設者、病院若しくは診療所の開設者又は医師、歯科医師、薬剤師その他の医
薬関係者は、2の規定による報告を行うこと。
(5) ヒトパピローマウイルス感染症のキャッチアップ接種にあっては、過去に接種
したヒトパピローマウイルス様粒子ワクチンの種類が不明の場合、結果として、異
なる種類のワクチンが接種される可能性があるため、ワクチンの互換性に関する安
全性、免疫原性及び有効性についての情報収集の観点から、別紙様式1における予
診票での留意点にその旨明記すること。
(6)(3)及び(4)については、患者に接種を行った医師等以外の医師等において
も行うべきものであること。