よむ、つかう、まなぶ。
再生医療等安全性確保法施行5年後の見直しに係る検討 (5 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_23718.html |
| 出典情報 | 厚生科学審議会 再生医療等評価部会(第72回 2/2)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
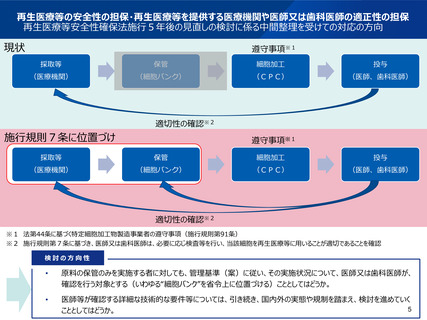
再生医療等の安全性の担保・再生医療等を提供する医療機関や医師又は歯科医師の適正性の担保
再生医療等安全性確保法施行5年後の見直しの検討に係る中間整理を受けての対応の方向
現状
遵守事項※1
採取等
保管
細胞加工
投与
(医療機関)
(細胞バンク)
(CPC)
(医師、歯科医師)
適切性の確認※2
施行規則7条に位置づけ
遵守事項※1
採取等
保管
細胞加工
投与
(医療機関)
(細胞バンク)
(CPC)
(医師、歯科医師)
適切性の確認※2
※1 法第44条に基づく特定細胞加工物製造事業者の遵守事項(施行規則第91条)
※2 施行規則第7条に基づき、医師又は歯科医師は、必要に応じ検査等を行い、当該細胞を再生医療等に用いることが適切であることを確認
検討の方向性
•
原料の保管のみを実施する者に対しても、管理基準(案)に従い、その実施状況について、医師又は歯科医師が、
確認を行う対象とする(いわゆる“細胞バンク”を省令上に位置づける)こととしてはどうか。
•
医師等が確認する詳細な技術的な要件等については、引き続き、国内外の実態や規制を踏まえ、検討を進めていく
5
こととしてはどうか。
再生医療等安全性確保法施行5年後の見直しの検討に係る中間整理を受けての対応の方向
現状
遵守事項※1
採取等
保管
細胞加工
投与
(医療機関)
(細胞バンク)
(CPC)
(医師、歯科医師)
適切性の確認※2
施行規則7条に位置づけ
遵守事項※1
採取等
保管
細胞加工
投与
(医療機関)
(細胞バンク)
(CPC)
(医師、歯科医師)
適切性の確認※2
※1 法第44条に基づく特定細胞加工物製造事業者の遵守事項(施行規則第91条)
※2 施行規則第7条に基づき、医師又は歯科医師は、必要に応じ検査等を行い、当該細胞を再生医療等に用いることが適切であることを確認
検討の方向性
•
原料の保管のみを実施する者に対しても、管理基準(案)に従い、その実施状況について、医師又は歯科医師が、
確認を行う対象とする(いわゆる“細胞バンク”を省令上に位置づける)こととしてはどうか。
•
医師等が確認する詳細な技術的な要件等については、引き続き、国内外の実態や規制を踏まえ、検討を進めていく
5
こととしてはどうか。