よむ、つかう、まなぶ。
総-4-2最適使用推進ガイドライン(デペモキマブ(鼻茸を伴う慢性副鼻腔炎)) (7 ページ)
出典
| 公開元URL | https://www.mhlw.go.jp/stf/newpage_72294.html |
| 出典情報 | 中央社会保険医療協議会 総会(第649回 4/8)《厚生労働省》 |
ページ画像
ダウンロードした画像を利用する際は「出典情報」を明記してください。
低解像度画像をダウンロード
プレーンテキスト
資料テキストはコンピュータによる自動処理で生成されており、完全に資料と一致しない場合があります。
テキストをコピーしてご利用いただく際は資料と付け合わせてご確認ください。
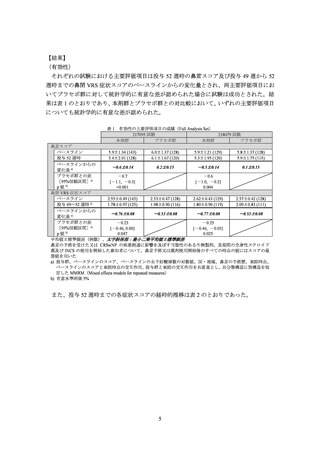
表 2 投与 52 週時までの各症状スコアの経時的推移(Full Analysis Set)
217095 試験
218079 試験
本剤群
プラセボ群
本剤群
プラセボ群
(143 例)
(128 例)
(129 例)
(128 例)
ベースライン値
5.9±1.3 (143)
6.0±1.4 (128)
5.9±1.2 (129)
5.8±1.4 (128)
鼻茸スコア
投与 26 週時
-0.7±1.6 (132)
0.1±1.6 (125)
-0.5±1.6 (125)
-0.1±1.2 (120)
ベースラインからの変化量
投与 52 週時
-0.5±2.0 (128)
0.2±1.6 (120)
-0.5±1.7 (120)
0.1±1.5 (115)
ベースライン値
2.6±0.5 (143)
2.5±0.5 (128)
2.6±0.4 (129)
2.6±0.4 (128)
鼻閉 VRS 症状
投与 21~24 週時
-0.7±0.9 (133)
-0.6±0.9 (124)
-0.8±0.8 (127)
-0.5±0.8 (118)
スコア
ベースラインからの変化量
投与 49~52 週時
-0.8±1.0 (125)
-0.5±1.0 (116)
-0.8±0.9 (119)
-0.5±0.9 (111)
ベースライン値
2.2±0.7 (143)
2.2±0.7 (128)
2.3±0.7 (129)
2.3±0.6 (128)
鼻汁 VRS 症状
投与 21~24 週時
-0.7±0.9 (133)
-0.6±0.8 (124)
-0.7±0.9 (127)
-0.6±0.8 (118)
スコア
ベースラインからの変化量
投与 49~52 週時
-0.7±1.0 (125)
-0.5±1.1 (116)
-0.8±1.0 (119) -0.5±0.9 (111)
ベースライン値
2.7±0.5 (143)
2.7±0.6 (128)
2,9±0.4 (129)
2.8±0.4 (128)
嗅覚消失 VRS
投与 21~24 週時
-0.5±0.8 (133)
-0.3±0.7 (124)
-0.5±0.7 (127)
-0.3±0.6 (118)
症状スコア
ベースラインからの変化量
投与 49~52 週時
-0.5±0.9 (125)
-0.3±0.7 (116)
-0.6±0.8 (119)
-0.3±0.7 (111)
18.4±4.2 (139)
19.0±4.0 (127)
19.6±3.8 (129)
18.2±4.5 (128)
Lund Mackay CT ベースライン値
スコア
ベースラインからの変化量 投与 52 週時
-2.7±5.5 (127)
-0.9±4.9 (119)
-3.6±5.1 (121)
-0.2±4.2 (111)
ベースライン値
58.2±22.6 (140)
56.6±21.7 (125)
60.1±21.5 (126)
60.1±18.3 (126)
SNOT-22
投与 26 週時
-18.0±29.6 (130) -11.6±31.1 (120) -19.6±27.5 (121) -12.3±27.1 (116)
総スコア
ベースラインからの変化量
投与 52 週時
-13.8±37.6 (125) -5.6±39.5 (116) -15.4±32.4 (119) -6.0±34.4 (113)
平均値±標準偏差(例数)
(安全性)
217095 試験及び 218079 試験において、有害事象は、本剤群 74.6%(203/272 例)、プラセ
ボ群 79.3%(203/256 例)に認められ、主な有害事象は表 3 のとおりであった。
死亡は、認められなかった。
重篤な有害事象は、本剤群 3.3%(9/272 例)
、プラセボ群 6.3%(16/256 例)に認められ、
いずれも治験薬との因果関係は否定された。
中止に至った有害事象は、プラセボ群 1.2%(3/256 例)に認められた。
副作用は、本剤群 6.3%(17/272 例)、プラセボ群 3.5%(9/256 例)に認められた。
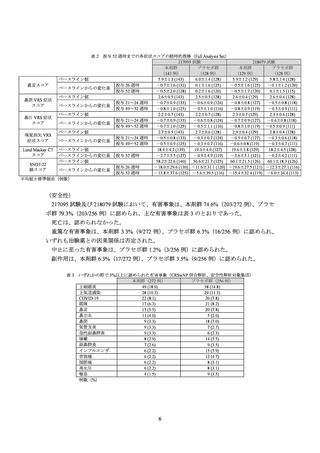
表 3 いずれかの群で 3%以上に認められた有害事象(CRSwNP 併合解析、安全性解析対象集団)
本剤群(272 例)
プラセボ群(256 例)
上咽頭炎
49 (18.0)
38 (14.8)
上気道感染
28 (10.3)
29 (11.3)
COVID-19
22 (8.1)
20 (7.8)
頭痛
17 (6.3)
21 (8.2)
鼻茸
15 (5.5)
20 (7.8)
鼻出血
11 (4.0)
5 (2.0)
鼻閉
9 (3.3)
18 (7.0)
気管支炎
9 (3.3)
7 (2.7)
急性副鼻腔炎
9 (3.3)
6 (2.3)
咳嗽
8 (2.9)
14 (5.5)
副鼻腔炎
7 (2.6)
9 (3.5)
インフルエンザ
6 (2.2)
15 (5.9)
背部痛
6 (2.2)
12 (4.7)
関節痛
6 (2.2)
8 (3.1)
高血圧
6 (2.2)
8 (3.1)
喘息
4 (1.5)
9 (3.5)
例数(%)
6
217095 試験
218079 試験
本剤群
プラセボ群
本剤群
プラセボ群
(143 例)
(128 例)
(129 例)
(128 例)
ベースライン値
5.9±1.3 (143)
6.0±1.4 (128)
5.9±1.2 (129)
5.8±1.4 (128)
鼻茸スコア
投与 26 週時
-0.7±1.6 (132)
0.1±1.6 (125)
-0.5±1.6 (125)
-0.1±1.2 (120)
ベースラインからの変化量
投与 52 週時
-0.5±2.0 (128)
0.2±1.6 (120)
-0.5±1.7 (120)
0.1±1.5 (115)
ベースライン値
2.6±0.5 (143)
2.5±0.5 (128)
2.6±0.4 (129)
2.6±0.4 (128)
鼻閉 VRS 症状
投与 21~24 週時
-0.7±0.9 (133)
-0.6±0.9 (124)
-0.8±0.8 (127)
-0.5±0.8 (118)
スコア
ベースラインからの変化量
投与 49~52 週時
-0.8±1.0 (125)
-0.5±1.0 (116)
-0.8±0.9 (119)
-0.5±0.9 (111)
ベースライン値
2.2±0.7 (143)
2.2±0.7 (128)
2.3±0.7 (129)
2.3±0.6 (128)
鼻汁 VRS 症状
投与 21~24 週時
-0.7±0.9 (133)
-0.6±0.8 (124)
-0.7±0.9 (127)
-0.6±0.8 (118)
スコア
ベースラインからの変化量
投与 49~52 週時
-0.7±1.0 (125)
-0.5±1.1 (116)
-0.8±1.0 (119) -0.5±0.9 (111)
ベースライン値
2.7±0.5 (143)
2.7±0.6 (128)
2,9±0.4 (129)
2.8±0.4 (128)
嗅覚消失 VRS
投与 21~24 週時
-0.5±0.8 (133)
-0.3±0.7 (124)
-0.5±0.7 (127)
-0.3±0.6 (118)
症状スコア
ベースラインからの変化量
投与 49~52 週時
-0.5±0.9 (125)
-0.3±0.7 (116)
-0.6±0.8 (119)
-0.3±0.7 (111)
18.4±4.2 (139)
19.0±4.0 (127)
19.6±3.8 (129)
18.2±4.5 (128)
Lund Mackay CT ベースライン値
スコア
ベースラインからの変化量 投与 52 週時
-2.7±5.5 (127)
-0.9±4.9 (119)
-3.6±5.1 (121)
-0.2±4.2 (111)
ベースライン値
58.2±22.6 (140)
56.6±21.7 (125)
60.1±21.5 (126)
60.1±18.3 (126)
SNOT-22
投与 26 週時
-18.0±29.6 (130) -11.6±31.1 (120) -19.6±27.5 (121) -12.3±27.1 (116)
総スコア
ベースラインからの変化量
投与 52 週時
-13.8±37.6 (125) -5.6±39.5 (116) -15.4±32.4 (119) -6.0±34.4 (113)
平均値±標準偏差(例数)
(安全性)
217095 試験及び 218079 試験において、有害事象は、本剤群 74.6%(203/272 例)、プラセ
ボ群 79.3%(203/256 例)に認められ、主な有害事象は表 3 のとおりであった。
死亡は、認められなかった。
重篤な有害事象は、本剤群 3.3%(9/272 例)
、プラセボ群 6.3%(16/256 例)に認められ、
いずれも治験薬との因果関係は否定された。
中止に至った有害事象は、プラセボ群 1.2%(3/256 例)に認められた。
副作用は、本剤群 6.3%(17/272 例)、プラセボ群 3.5%(9/256 例)に認められた。
表 3 いずれかの群で 3%以上に認められた有害事象(CRSwNP 併合解析、安全性解析対象集団)
本剤群(272 例)
プラセボ群(256 例)
上咽頭炎
49 (18.0)
38 (14.8)
上気道感染
28 (10.3)
29 (11.3)
COVID-19
22 (8.1)
20 (7.8)
頭痛
17 (6.3)
21 (8.2)
鼻茸
15 (5.5)
20 (7.8)
鼻出血
11 (4.0)
5 (2.0)
鼻閉
9 (3.3)
18 (7.0)
気管支炎
9 (3.3)
7 (2.7)
急性副鼻腔炎
9 (3.3)
6 (2.3)
咳嗽
8 (2.9)
14 (5.5)
副鼻腔炎
7 (2.6)
9 (3.5)
インフルエンザ
6 (2.2)
15 (5.9)
背部痛
6 (2.2)
12 (4.7)
関節痛
6 (2.2)
8 (3.1)
高血圧
6 (2.2)
8 (3.1)
喘息
4 (1.5)
9 (3.5)
例数(%)
6